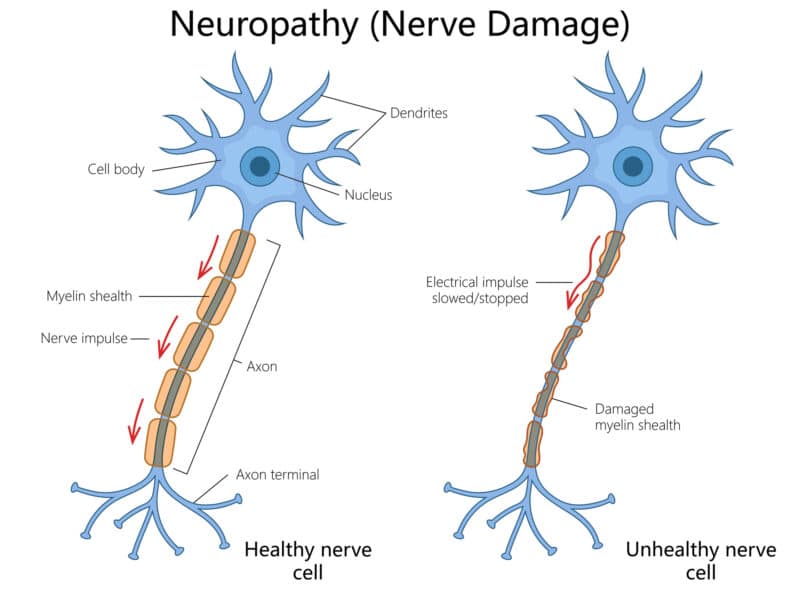
אקסוזומים טעונים ב-siRNA נגד PTEN, שפותחו בטכניון ובאוניברסיטת תל אביב, מיועדים להפחית דלקת ולעודד רגנרציה במערכת העצבים המרכזית – תחום שרלוונטי גם לנזקי מיאלין כמו בטרשת נפוצה
ד"ר ליאור שאלתיאל, מנכ"ל חברת NurExone מאז 2021, מתאר את החברה כמי שמפתחת טיפולים רגנרטיביים המבוססים על אקסוזומים – "שליחים" ביולוגיים זעירים שהגוף משתמש בהם כדי לתקשר בין תאים ורקמות. מדובר בננו-חלקיקים טבעיים עם יכולת תקשורת בין-תאית ותכונות רגנרטיביות, שניתן לרתום גם להעברת "מטען" תרפויטי ישירות לרקמה פגועה.
החברה היא ספין-אוף של הטכניון ואוניברסיטת תל אביב, מבוססת על מחקר משותף של פרופ' שולמית לבנברג מהטכניון ופרופ' דני אופן מתל אביב. שני החוקרים עבדו מאז 2015 על פרויקט שמטרתו רגנרציה של נוירונים במערכת העצבים המרכזית, תחום שבו הגוף מתקשה לחדש תאי עצב ולשקם תפקוד מלא לאחר טראומה.
איך עובדת פלטפורמת ExoTherapy
בלב הפיתוח נמצאת פלטפורמה בשם ExoTherapy, שמטרתה "להטעין" אקסוזומים במולקולות טיפוליות ולהפוך אותם לתרופה ממוקדת-יעד. אקסוזומים נוצרים כאשר תאי גזע מתרבים, והם מפגינים יכולת "Homing" – הגעה מועדפת לרקמות מסוימות ולמוקדי דלקת. החברה משתמשת בהם כמעין "טילים מונחים", שניתן להעמיס עליהם מגוון מטענים תרפויטיים.
המוצר המוביל נקרא ExoPTEN, ומבוסס על אקסוזומים שמובילים מטען siRNA (RNA קצר המשתק ביטוי גנים) שמדכא את ביטוי החלבון PTEN – יעד ביולוגי שנחקר בהקשרים של צמיחה והתחדשות עצבית. לפי שאלתיאל, האקסוזומים פועלים בשני מנגנונים מקבילים: הורדת דלקת באזור הפגיעה ועידוד רגנרציה טבעית של רקמת העצב.
הגישה "ללא תאים חיים" אמורה להפחית סיכונים שמקושרים להשתלות תאים, כמו דחייה חיסונית. בנוסף, החברה טוענת שאקסוזומים יכולים לחצות את מחסום דם-מוח ולהגיע לאתרי פגיעה. מאפיין נוסף הוא האפשרות לייצר מוצר "מדף" – קל יותר לייצור, להפצה ולמתן, לעומת טיפולים שמחייבים תהליך מותאם-אישית לכל מטופל.
היישומים הראשונים כוללים פגיעות חוט שדרה, פגיעות עצב הראייה (אופטיק נרב), עצבים פריפריאליים, ופגיעות מוח טראומטיות (TBI). במחקרים הפרה-קליניים, החברה השתמשה במודלים של חתך מלא של חוט השדרה בחולדות, עם מתן אינטרנזלי (דרך האף) או הזרקה לנוזל חוט השדרה.
למה הם יכולים "פתאום" למכור גם את הבסיס של הטכנולוגיה
הנקודה העסקית החשובה היא שלא מדובר רק בתרופה עתידית אחת, אלא גם ביכולת ייצור של "החומר הבסיסי": אקסוזומים "נאיביים" (כלומר, לפני הטענה במטען תרופתי ייעודי). נורקסון מקימה חברת-בת אמריקנית בשם Exo-Top כדי לייצר "אקסוזומים בדרגת-טיפול" (Therapeutic-Grade) מתוך Master Cell Bank ייחודי של תאי גזע מזנכימליים (MSCs).
כאן מגיע ההסבר ליכולת "למכור את הבסיס": אותו קו ייצור שמשרת את צנרת התרופות יכול לייצר גם אקסוזומים שאינם מוגדרים כתרופה ספציפית, אלא כמוצר לשימושים שאינם תרופתיים. החברה מציגה זאת כמודל "שימוש כפול": האקסוזומים המיוצרים ב-Exo-Top מיועדים גם לשמש כנשא לצנרת הטיפולית, וגם להזין שוק "אקסוזומים רגנרטיביים" שצומח במהירות בתחומי אסתטיקה, דרמטולוגיה, רפואת כאב ולונג'ביטי.
במילים פשוטות: בביוטק רגיל, הכנסות מגיעות רק אחרי ניסויים קליניים ואישור רגולטורי. כאן, החברה מנסה לייצר הכנסה מוקדמת ממכירת "חומר גלם ביולוגי" איכותי עוד לפני שהתרופה עצמה מגיעה לשוק. החברה מציינת יעד לתחילת מכירות מסחריות במהלך 2026.
שאלתיאל מצביע על שינוי רגולטורי משמעותי בארה"ב: מיולי 2025, מדינת פלורידה הודיעה שניתן לבצע טיפולים תאיים וטיפולים מבוססי-אקסוזומים לשלוש אינדיקציות (כאב, אורתופדיה ואיחוי פצעים) ללא ניסוי קליני מלא של FDA, אך ורק על בסיס בדיקות רעילות. גם יוטה ונבדה נקטו צעדים דומים, במה שנתפס כחלק מהמאמץ לעודד טיפולים רגנרטיביים בארה"ב במקום שאזרחים אמריקאים יטוסו למרכז אמריקה או למזרח הרחוק לביצוע טיפולים אלה.
מה הלאה: IND וניסוי ראשון באדם
החברה נמצאת בשלב פרה-קליני ועובדת על הכנת תיק IND (Investigational New Drug) מול FDA. לפי שאלתיאל, השאיפה היא להתחיל ניסויים קליניים בבני אדם בתחילת 2027. החברה שוקלת גם הגשת בקשות לטיפולי חמלה (Compassionate Use) בישראל, במיוחד לחולים עם פגיעות חוט שדרה או גלאוקומה קיצונית שאין להם אלטרנטיבה טיפולית.
חשוב להדגיש: אקסוזומים טיפוליים מסוג זה עדיין אינם טיפול מאושר לשימוש שגרתי בפגיעות חוט שדרה או גלאוקומה; אלה כיווני פיתוח שמבוססים על מחקר פרה-קליני ותכנון רגולטורי.
הפן הבורסאי והמימון
נורקסון היא חברה ציבורית הנסחרת בבורסה הקנדית מאז יוני 2022. שאלתיאל מתאר את הבחירה להיות חברה ציבורית כבר בשלבים מוקדמים כ"דיסרפשן" בדרך המימון של ביוטק. בדרך כלל חברות ביוטק פועלות כחברות פרטיות עד לאירוע מימון משמעותי או אקזיט, אך נורקסון בחרה בנתיב הציבורי כבר בשלב מוקדם.
היתרון, לטענתו, הוא שמשקיעים יכולים להנזיל את ההשקעה שלהם אחרי תקופת חסימה של ארבעה חודשים בלבד, במקום לחכות שנים לאירוע אקזיט. "משקיע שאוהב ביוטק והוא יודע שהוא יכול להנזיל את הכסף אחרי תקופה קצרה ולא לחכות שנים, זה דבר מאוד משמעותי," הוא מסביר.
הגיוס האחרון של החברה היה בנובמבר 2025, כאשר נכנסו לחברה 3.2 מיליון דולר קנדי דרך כתבי אופציה של משקיעים קיימים. המשקיעים בחברה הם בעיקר משקיעים פרטיים ומשפחות עשירות (Family Offices), ולא קרנות הון סיכון מסורתיות. החברה מתכננת מעבר לבורסה אמריקאית (NASDAQ או NYSE) בעתיד הקרוב.
כ-86% מהכסף שמגויס דרך החברה הקנדית מגיע לישראל. החברה מעסיקה 22 עובדים, רובם בחיפה ובצפון הארץ, ופועלת מתוך הטכניון כחלק מחברות הספין-אוף של האוניברסיטה. חלק מהפטנטים שייכים לחברה, וחלק בלייסנס אקסקלוסיבי מהטכניון ומאוניברסיטת תל אביב.
שאלתיאל מדגיש את החשיבות של מימון חברות ביוטק ישראליות: "יש לנו שתי בעיות בישראל: חסר לנו כסף וחסר לנו הון אנושי. או שיהיה לנו הון אנושי טוב שיעשה תעשייה, לא רק מדע." הוא גם מנהל תכנית MBA בניהול ביורפואי באוניברסיטה העברית, שמטרתה להכשיר את דור הניהול הבא של תעשיית הביוטק הישראלית.
הסביבה העסקית של השנים האחרונות הייתה מאתגרת במיוחד לחברות ביוטק. לדבריו, "אם בזמנו כל חמש פגישות יכולת להביא השקעה, עכשיו כל 20 פגישות אתה תביא השקעה." הוא מציין שחברות שחושבות "מחוץ לקופסה" במימון – כמו גיוס המונים, מימון קריפטו, או מודלים היברידיים – הן אלה שהצליחו לשרוד את המשבר.
אזהרה: המידע במאמר זה הוא למטרות מידע בלבד ואינו מהווה המלצה רפואית או השקעתית. טיפולים מבוססי אקסוזומים עדיין בשלבי מחקר ופיתוח, ואינם מאושרים לשימוש קליני שגרתי ברוב האינדיקציות.
עוד בנושא באתר הידען:
ד"ר ליאור שאלתיאל יציג בכנס NANO.IL הבינלאומי שייערך בבנייני האומה בירושלים ( 8-10 במרץ ). בכנס ייחשפו מיטב המדענים והיזמים הישראלים שלקחו את הננו-טכנולוגיה ושילבו אותה ביישומים פורצי דרך במגוון תחומים: בטחון, רפואה, תעשייה, כימיה ועוד
