הגידול המודפס מסוג גליובלסטומה, הסוג הקטלני ביותר של גידולי סרטן המוח, מודפס מרקמות אנושיות ומכיל את כל מרכיביו של הגידול הסרטני * החוקרים מעריכים כי ניתן יהיה בעתיד לחזות במהירות את הטיפול המתאים ביותר עבור המטופל ובמקביל לפתח תרופות חדשות בקצב מהיר בהרבה מזה שקיים היום

הישג מדעי לחוקרים מאוניברסיטת תל אביב שהצליחו להדפיס במדפסת תלת-מימד גידול סרטני שלם ופעיל מסוג גליובלסטומה. הגידול המודפס כולל מערכת מסועפת של צינוריות דמויות-כלי דם שניתן להזרים דרכן תאי דם ותרופות באופן המדמה את הגידול האמיתי.
המחקר נערך בהובלת פרופ' רונית סצ'י-פאינרו מהפקולטה לרפואה ע"ש סאקלר וביה"ס סגול למדעי המוח, העומדת בראש המרכז לחקר הביולוגיה של הסרטן, המעבדה לחקר סרטן וננו-רפואה והמיזם להדפסת תלת-מימד לחקר סרטן ע"ש מוריס קאהן באוניברסיטת תל אביב. את הטכנולוגיה החדשה פיתחה הדוקטורנטית לנה נויפלדיחד עם חברי המעבדה עילם ייני, נעה רייזמן, יעל שטילרמן, ד"ר דקלה בן-שושן, סבינה פוצי, ד"ר גליה טירם, ד"ר ענת אלדר-בוק, וד"ר שירן פרבר.
הדפסת הגידול מתבססת על דגימות של חולים שנלקחו הישר מחדרי הניתוח במחלקה הנוירוכירורגית בבית החולים סוראסקי שבתל אביב. תוצאות המחקר החדש מתפרסמות היום בכתב העת היוקרתי Science Advances.
"גליובלסטומה הוא הסוג הקטלני ביותר של גידולי סרטן במערכת העצבים המרכזית, והוא מהווה את מרבית הגידולים הממאירים שמקורם במוח", אומרת פרופ' סצ'י-פאינרו. "במחקר קודם שלנו זיהינו לראשונה חלבון בשם P-Selectin , שמופרש במפגש בין תאי סרטן מסוג גליובלסטומה לתאים מסוג מיקרוגליה, תאי המערכת החיסונית במוח שלנו. מצאנו שחלבון זה אחראי לכשל בתאי המיקרוגליה אשר במקום לתקוף את תאי הסרטן, מעודדים את התפשטותו של סרטן קטלני זה. אלא שאת החלבון הזה זיהינו בגידולים שהוסרו בניתוח מחולים – אבל לא בתאי גליובלסטומה שגידלנו במעבדה שלי, בדו-מימד על צלחות פטרי. הסיבה היא שסרטן, כמו כל רקמה, מתנהג שונה מאוד על משטח פלסטיק קשיח לעומת התנהגותו כשהוא גדל בגוף האדם. 90% מהתרופות נופלות בשלב הניסויים הקליניים כי לא מצליחים לשחזר בבני אדם את ההצלחה שהושגה במעבדה".
לשם כך, צוות החוקרים בהובלת פרופ' סצ'י-פאינרו יחד עם הדוקטורנטית לנה נויפלד, זוכת מלגת דן דוד היוקרתית, יצר את המודל התלת-ממדי המודפס הראשון של סרטן מסוג גליובלסטומה הכולל רקמה סרטנית תלת-ממדית, המוקפת במטריקס חוץ-תאי ומתקשרת עם סביבתה באמצעות כלי דם מתפקדים וזורמים.
"זה לא רק תאי הסרטן עצמם", מסבירה פרופ' סצ'י-פאינרו, "אלא גם תאי המיקרו-סביבה במוח, האסטרוציטים, המיקרוגליה וכלי דם המחוברים למערכת מיקרופלואידית – כלומר מערכת שמאפשרת להזרים לגידול חומרים כמו תאי דם ותרופות. כל מודל מודפס בתוך ביוראקטור שייצרנו במעבדה, באמצעות ג'ל שדגמנו ושכפלנו מהמטריקס החוץ-תאי שנלקח מהחולה, ובכך מדמה את הרקמה עצמה. הרי למוח אין את אותן התכונות הפיזיקליות והמכניות של איברים אחרים כגון עור, שד או עצם. רקמת שד היא בעיקר שומן, רקמת עצם היא בעיקר סידן; לכל רקמה יש תכונות אחרות, והתכונות הללו משפיעות על התנהגות תאי הסרטן ועל היכולת שלהם להגיב לתרופות. לגדל את כל סוגי הסרטן על משטח פלסטיק זהה – רחוק מלדמות את המצב הקליני באופן מיטבי".
לאחר שהדפיסו בהצלחה את הגידול התלת-ממדי, פרופ' סצ'י-פאינרו ועמיתיה הראו שבעזרת המודל, ניתן יהיה לחזות במהירות וביעילות את הטיפול המתאים ביותר עבור חולה ספציפי, בניגוד לתאים סרטניים הגדלים בצלחות פטרי.
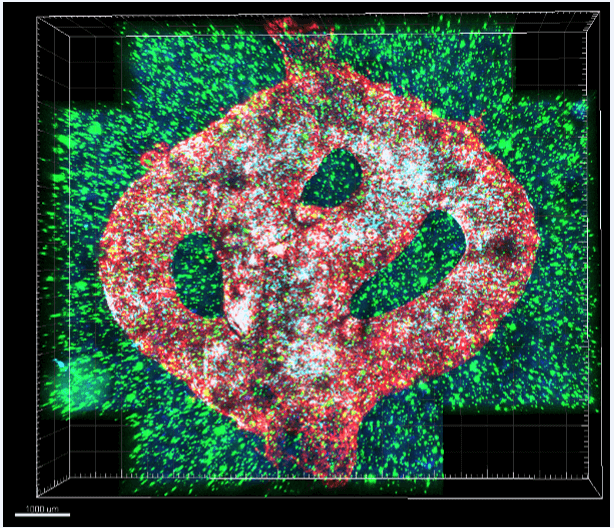
"אנחנו הוכחנו שהמודל התלת-ממדי שלנו מתאים יותר לניבוי ולפיתוח תרופות בשלוש דרכים שונות. ראשית, בדקנו חומר שעיכב את החלבון שמצאנו, P-Selectin, על תרביות תאי גליובלסטומה בצלחות פטרי דו-ממדיות, ולא ראינו כל שינוי בחלוקת או בנדידת התאים שטופלו לעומת תאי הביקורת שלא טופלו. לעומת זאת, בחיות מודל ובמודלים התלת-ממדיים המודפסים, שבהם כן מצאנו ביטוי גבוה של החלבון, הצלחנו לעכב את התקדמות הגליובלסטומה על ידי חסימת החלבון P-Selectin. הניסוי הזה הוכיח לנו כמה תרופות פוטנציאליות לא מגיעות לקליניקה כי הן נכשלו בבדיקות על מודלים דו-ממדיים, ולהפך: כמה מקרים שנחשבו להצלחה מסחררת במעבדה, נכשלו במבחנים הקליניים.
בנוסף, בשיתוף פעולה עם המעבדה של ד"ר אסף מדי מהמחלקה לפתולוגיה בפקולטה לרפואה באוניברסיטת תל אביב, ריצפנו גנטית את התאים הסרטניים שגידלנו במודל התלת-ממדי והשווינו אותם לתאים סרטניים שגדלו על פלסטיק דו-ממדי ולתאים שריצפנו מחולים, והראינו שהגידולים שהודפסו בתלת-מימד היו דומים הרבה יותר לתאי סרטן המוח בסביבתם הטבעית. לאורך זמן, תאי הסרטן שגדלו על פלסטיק, הלכו והשתנו עד שאיבדו כל קשר לתאי הסרטן במוח של החולה. לבסוף, ההוכחה השלישית הייתה ע"י מדידת קצב צמיחת הגידולים. גליובלסטומה היא מחלה אלימה בין היתר כי היא לא צפויה: אם מזריקים בנפרד את התאים הסרטניים ההטרוגניים לחיות מודל, אצל חלקן, הגידול יהיה רדום ואצל חלקן, יתפתח במהירות גידול פעיל. זה הגיוני מאוד כי אנחנו בני האדם יכולים למות בשיבה טובה מבלי לדעת בכלל שהיו לנו גידולים 'רדומים' שכאלה. לעומת זאת, על צלחת הפלסטיק במעבדה, כל הגידולים גדלים באותו הקצב ומתפשטים באותו האופן. בגידול שהדפסנו במדפסת התלת-מימד, קצב התפתחות הגידול תואמת להתפתחות שאנחנו רואים בחולים או בחיות מודל".

לדברי פרופ' סצ'י-פאינרו, זוהי גישה חדשנית שתאפשר גם לפתח תרופות חדשות וכן לגלות מטרות חדשות לתרופות מתאימות בקצב מהיר בהרבה מזה שקיים היום. בתקווה שבעתיד, טכנולוגיה זו תאפשר רפואה מותאמת-אישית לחולים.
"אם אני לוקחת דגימה מרקמה של חולה, יחד עם המטריקס החוץ-תאי שלו, אני יכולה להדפיס מהדגימה הזאת מאה גידולים שונים ולבדוק תרופות רבות ובשילובים שונים כדי לגלות איזו תרופה או משלב תרופות מתאימים יותר לגידול הספציפי הזה. לחלופין, הפיתוח מאפשר לנו לבדוק המון תרכובות שונות על גידול שהודפס במדפסת תלת-מימד, ולהחליט באיזו תרכובת כדאי להשקיע את המשאבים כדי לנסות ולפתח הלאה כתרופה עד לשלב הקליני. אבל אולי החלק המרגש ביותר הוא מציאת חלבוני-המטרה וגני-המטרה בתאים הסרטניים, דבר שקשה מאוד לעשותו בגידולים הנמצאים במוחות של חולים או של חיות מודל. הפיתוח החדשני מעניק לנו גישה חסרת-תקדים, ולא מוגבלת בזמן, לבחון לעומק גידול תלת-ממדי המחקה את הגידול שאנו מוצאים אצל החולים בצורה המיטבית".
המחקר מומן על ידי קרן מוריס קאהן, הקרן לחקר הסרטן בישראל (ICRF), מועצת המחקר האירופית (ERC), האגודה למלחמה בסרטן, הקרן הלאומית למדע וצ'ק פוינט טכנולוגיות תוכנה בע"מ.
עוד בנושא באתר הידען:

תגובה אחת
חסרה אינפורמציה חשובה
כיצד בעצם מדפיסים את הגידול במדפסת? עם איזה חומרים? או שאולי מדפיסים רק את השלד החיצוני של הרקמות ואז נותנים לגידול להפתח בו לבד ילד עם הרקמות הבריאות?