הידען > מדעים ביומולקולריים
מדעים ביומולקולריים
- מכון ויצמן
הממצאים עשויים לשפוך אור חדש על שיבושים בשעון הביולוגי בזמן מחזור, בהריון ובגיל המעבר
- מכון ויצמן
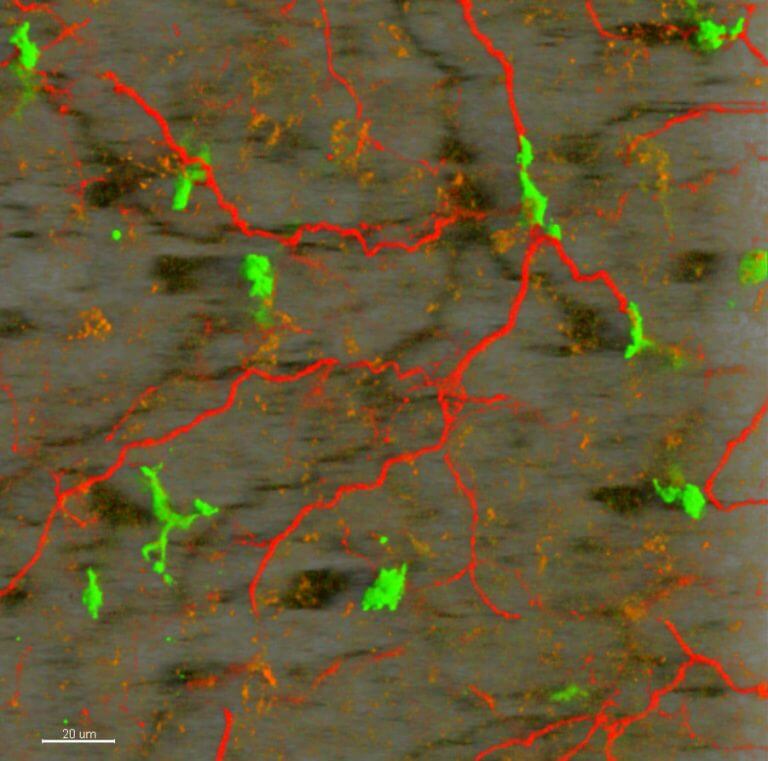
אלפי חלבונים תלויים בזנבותיהם כדי להתמקם בקרומי התא ולהוציא לפועל את תפקידיהם החיוניים. שינויים בזנבות עלולים להוביל למחלות גנטיות נדירות
- מכון ויצמן
כך שומרים על דיאטה מאוזנת של אברוני האוטופאגיה – מנגנון האכילה העצמית בתאי גופנו המרחיק פסולת ומתחזק את בריאותנו
- מכון ויצמן
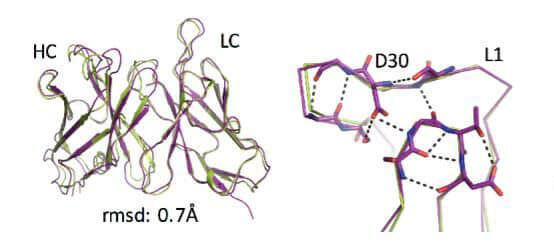
אלגוריתם שפיתחו מדעני המכון מבשר קפיצת מדרגה בתחום האנשת הנוגדנים ועשוי לאפשר פיתוח מהיר, יעיל וזול יותר של תרופות חדשות. המפתח: יציבות
- amcohen
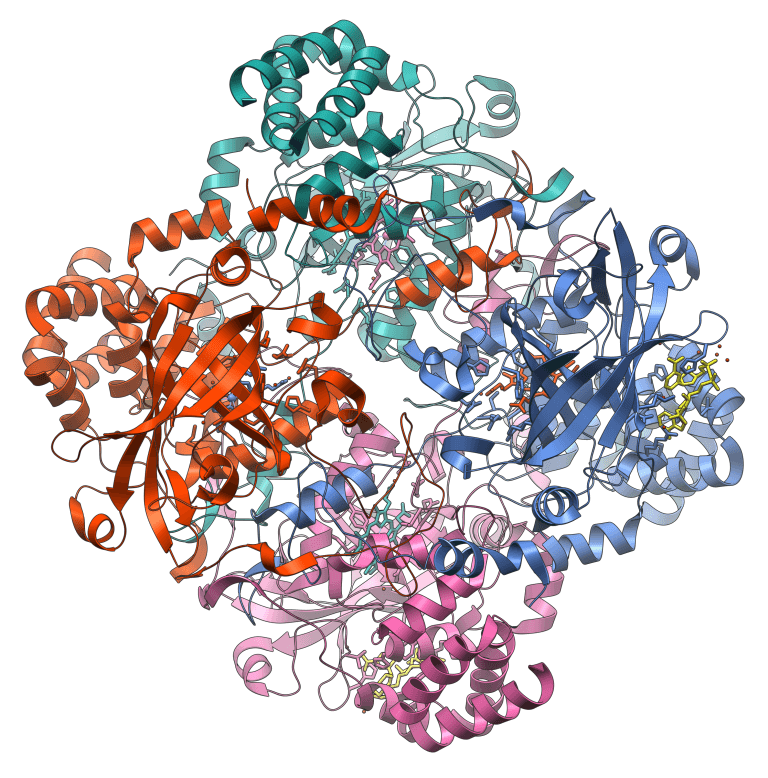
באמצעות התחקות אחר אבולוציה של חלבונים, שרטטו מדעני מכון ויצמן למדע את תולדות זמינות החמצן בכדור-הארץ ופתרו חידה מדעית ארוכת שנים
- מכון ויצמן
- 3 תגובות
- מכון ויצמן
- 6 תגובות
- אבי בליזובסקי
- אין תגובות
- מכון ויצמן
- 2 תגובות
- מכון ויצמן
- 4 תגובות
- מכון ויצמן
- תגובה אחת
- מכון ויצמן
- תגובה אחת
- מכון ויצמן
- 2 תגובות
- מכון ויצמן
- תגובה אחת
- מכון ויצמן
- 3 תגובות
- מכון ויצמן
- אין תגובות
- מכון ויצמן
- אין תגובות
- מכון ויצמן
- אין תגובות
- מכון ויצמן
- 3 תגובות
- מכון ויצמן
- אין תגובות
- מכון ויצמן
- אין תגובות
- מכון ויצמן
- 2 תגובות
- מכון ויצמן
- אין תגובות
- מכון ויצמן
- אין תגובות