מדעני מכון ויצמן למדע גילו מנגנון עצבי שלא היה מוכר עד כה; הממצאים עשויים לסלול דרך לטיפולים חדשים בהפרעות חרדה
הפרעות חרדה הן השכיחות ביותר מבין ההפרעות הנפשיות: על פי הערכות, כל אדם שלישי עלול לסבול מהפרעת חרדה חמורה מסוג זה או אחר במהלך חייו. מדעני מכון ויצמן למדע גילו מנגנון חרדה עצבי שלא היה מוכר עד כה. הממצאים שמתפרסמים היום בכתב-העת המדעי Cell Reports עשויים לאפשר לפתח טיפולים חדשים בהפרעות חרדה.
המעבדה של פרופ' מייק פיינזילבר במחלקה למדעים ביומולקולריים חוקרת כבר כמעט שני עשורים "חלבוני יבוא" (אימפורטינים). חלבונים אלה מובילים מולקולות אל תוך גרעין התא בכל סוגי התאים. המעבדה חוקרת את תפקידם של האימפורטינים בתאי עצב, ועד לאחרונה התמקדה במערכת העצבים ההיקפית. בשנת 2012 הצטרף למעבדה החוקר הבתר-דוקטוריאלי ד"ר ניקולאס פאניוטיס שהתמקד בתפקיד האימפורטינים במערכת העצבים המרכזית, כלומר המוח וחוט השדרה.
ד"ר פאניוטיס ועמיתיו חקרו חמש "שושלות" של עכברים שהונדסו גנטית במעבדתו של פרופ' מיכאל באדר במרכז מקס דלברוק לרפואה מולקולרית שבברלין. לעכברים בכל שושלת היה חסר גן מסוים מתת-משפחה של האימפורטינים המכונה תת-משפחה אלפא. החוקרים ערכו לעכברים אלה ניסויים התנהגותיים וגילו כי רק העכברים שחסרו את הגן אימפורטין אלפא-5 בלטו בתכונה ייחודית: הם לא הפגינו חרדה במצבים מלחיצים – למשל, כאשר הונחו בחלל פתוח או על משטח גבוה במיוחד.
התרופות נוגדות החרדה הזמינות כיום מוגבלות מבחינת היעילות שלהן או גורמות לתופעות לוואי שמגבילות את התועלת שבהן. הממצאים שלנו מצביעים על אפשרות לפתח תרופות שיאפשרו להתגבר על מגבלות אלה"
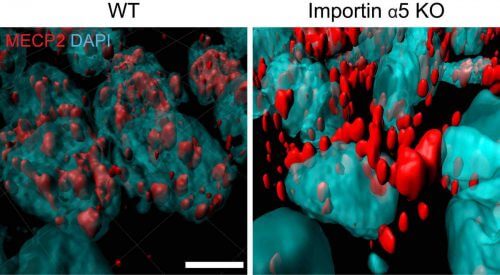
החוקרים בדקו במה נבדלו העכברים ה"רגועים" מעכברים רגילים מבחינת ביטוי גנים באזורי מוח המעורבים בבקרה על חרדה. ניתוחים חישוביים הצביעו על הבדלים בביטוי כמה גנים המבוקרים על ידי הגן MeCP2, הידוע כבעל תפקיד בבקרה על התנהגויות חרדתיות. בעקבות ממצאים אלה, התברר כי אימפורטין אלפא-5 הינו חיוני לכניסת MeCP2 לגרעין התא, וכי כאשר רמות ה- MeCP2 בגרעין משתנות, משתנה גם ביטוי האנזים המעורב בהפקת מולקולת איתות S1P. במלים אחרות, בעכברים שהיה חסר בהם האימפורטין אלפא-5, ה-MeCP2 לא נכנס לגרעין תאי העצב השולטים בחרדה, והדבר הוביל לירידה באיתות ה-S1P ובעקבות כך להפחתת החרדה.
לאחר ניסויים נוספים שנועדו לאשר כי אכן התגלה מסלול עצבי חדש במוח, החלו המדענים לבחון מולקולות המשפיעות על מסלול זה. החוקרים גילו כי קיימות בשוק תרופות המשפיעות על איתות ה-S1P. אחת מהן, פינגולימוד (fingolimod), משמשת כתרופה לטרשת נפוצה. כאשר בדקו המדענים את השפעת פינגולימוד על עכברים רגילים, הם גילו כי עכברים אלה היו פחות חרדתיים בנסיבות מלחיצות, בדומה לעכברים מהונדסים גנטית ללא הגן אימפורטין אלפא-5. במחקר קליני שפורסם בעבר דווח כי לפינגולימוד אכן ישנה השפעה מרגיעה על חולי טרשת נפוצה הנוטלים את התרופה; ייתכן שהממצאים החדשים מספקים הסבר להשפעה מרגיעה זו.
"הממצאים שלנו פותחים כיוון חדש לחקר מנגנוני החרדה", אומר ד"ר פאניוטיס. "אם נבין כיצד בדיוק המנגנונים שגילינו שולטים בחרדה, הבנה זו עשויה לעזור לפתח תרופות חדשות או לאפשר שימוש בתרופות קיימות, על מנת להקל על תסמיני החרדה".
אומר פרופ' פיינזילבר: "התרופות נוגדות החרדה הזמינות כיום מוגבלות מבחינת היעילות שלהן או גורמות לתופעות לוואי שמגבילות את התועלת שבהן. הממצאים שלנו מצביעים על אפשרות לפתח תרופות שיאפשרו להתגבר על מגבלות אלה. למעשה, זיהינו כבר כמה מולקולות שמשפיעות על המנגנון העצבי שהתגלה במחקר, ולפיכך עשויות להיות מועמדות לשמש כתרופות".
בנוסף, הממצאים שופכים אור חדש על מחלות גנטיות נדירות המאופיינות במוטציות בגן ה-MeCP2: תסמונת רט (Rett) ותסמונת הכפלת ה-MeCP2; בשתיהן, חרדה היא אחד התסמינים. זיהוי מנגנונים מדויקים האחראים לכניסת ה- MeCP2 לגרעיני תאי העצב עשוי לאפשר בעתיד לפתח תרופות לשתי מחלות אלה.
במחקר השתתפו ד"ר שחר דגן, אנה משצ'ריאקוב, ד"ר סנדיפ קוליי, ד"ר לטיציה מרבלדי, דידי אנדרס סונג ופרופ' איתן ראובני מהמחלקה למדעים ביומולקולריים של המכון; ד"ר אנטון שיינין מאוניברסיטת תל אביב; פרופ' יצחק מיכאלבסקי מאוניברסיטת אריאל בשומרון; ד"ר מיכאל מנחם צורי מהמחלקה למשאבים וטרינריים של מכון ויצמן למדע; ד"ר פרנצ'סקה רוטר, פרופ' אנו הרטמן ופרופ' מיכאל באדר ממרכז מקס דלברוק לרפואה מולקולרית בברלין; וד"ר מאיור ואדהווני ופרופ' בריטה אייקהולט מבית ספר לרפואה שאריטה, גם הוא בברלין.
