בעזרת טכנולוגיות חדשניות זיהו החוקרים כבר בשלב מוקדם של המחלה, משקעים קטנים ורעילים של חלבון המתרבים והולכים עם התקדמות
חוקרים באוניברסיטת תל אביב, בהובלת פרופ' אורי אשרי, ראש בית הספר סגול למדעי המוח, פיתחו שיטה חדשה לאבחון מחלת פרקינסון, שעשויה לאפשר אבחון ואף טיפול כבר בשלביה המוקדמים של המחלה. השיטה מתבססת על טכניקה מיקרוסקופית חדשנית המכונה סופר-רזולוציה, המאפשרת זיהוי משקעי חלבון האופייניים למחלה עוד כשהם קטנים מאוד.
המחקר בוצע על ידי ד"ר דנה בר-און, בשיתוף עם מעבדות באוניברסיטת קיימברידג' באנגליה, במכון מקס פלאנק בגוטינגן, ובאוניברסיטת לודויג מאקסימיליאן במינכן שבגרמניה. המאמר יתפרסם ביום רביעי 5.6.19 בכתב העת Acta Neuropathologica הנחשב למוביל בתחום המחלות הנוירולוגיות.
"מוחם של חולי פרקינסון מתאפיין בהיווצרות משקעים גדולים של חלבון בשם 'אלפא-סינוקלאין'” מסביר פרופ' אשרי. "משקעים אלה קשורים לתהליך הדרגתי שבו מתים תאים באזור 'החומר השחור' שבמוח האמצעי (substantia nigra). מות התאים גורם לירידה בשחרור המוליך העצבי דופמין במוח, וכתוצאה מכך לבעיות מוטוריות ובהמשך קוגניטיביות. הבעיה היא שבאמצעים המקובלים ניתן להבחין במשקעים אלו רק כשהם גדולים יחסית, כלומר בשלב מתקדם של המחלה, כש-75% מתאי החומר השחור כבר מתו, ולמעשה כבר לא ניתן לטפל בה. אנחנו חיפשנו דרך לאבחן את מחלת פרקינסון בשלב מוקדם הרבה יותר, וגם בדקנו טיפול אפשרי למחלה הקשה, שנחשבת היום לחשוכת מרפא."
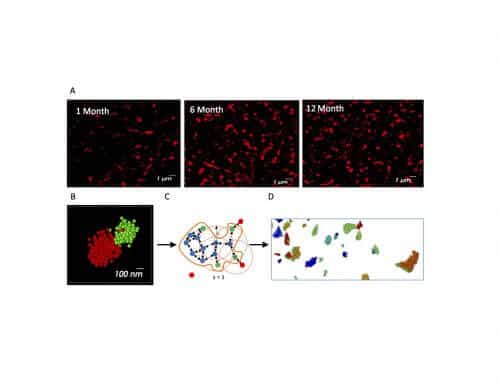
במהלך המחקר, יצרו השותפים בקיימברידג' עכברי מודל למחלת פרקינסון, המבטאים את החלבון אלפא-סינוקלאין האנושי עם מוטציה שגורמת באופן ספונטני ליצירת משקעים – צורה זו של החלבון נמצאה במשקעים של חולים פוסט מורטם. כשעכברים אלה הגיעו לגיל 9-6 חודשים נצפו אצלם תסמיני פרקינסון. בשלב זה נעזרו החוקרים בטכנולוגיה מיקרוסקופית מתקדמת של סופר-רזולוציה כדי לבחון חתכים ממוחם של העכברים. "גילינו כי כבר בשלב מוקדם של המחלה מופיעים בתאי החומר השחור משקעים קטנים של החלבון אלפא-סינוקלאין," אומרת ד"ר בר-און. "עוד מצאנו שהמשקעים הקטנים הולכים ומתרבים עם התפתחות המחלה, בניגוד למשקעים הגדולים שהיכרנו, שמספרם נותר קבוע. מכך היסקנו כי המשקעים הקטנים הם החומר הרעיל הגורם למחלה. יותר מכך, הצענו השערה שייתכן כי המשקעים הגדולים הינם רק מנגנון פיצוי של המוח במאבקו נגד המשקעים הקטנים הרעילים."

בעקבות התגלית, שותף למחקר ממכון מקס פלאנק בגרמניה, המתמחה בפיתוח חומרים נוגדי משקעים, הצליח לפתח חומר בשם Anle 138b, המונע את הצטברות משקעי האלפא-סינוקלאין. עכברי המודל טופלו בחומר, ומצבם השתפר משמעותית: חלה עלייה בשחרור הדופמין במוחם, והתנהגותם שבה לנורמה. במקביל מצאנו שהתרופה גרמה לפירוק המשקעים הקטנים של החלבון, שככל הנראה הפחית את רעילותם.
"במחקר גילינו מנגנון מרכזי של מחלת פרקינסון, שלא היה מוכר עד כה, ומצאנו חומר המנטרל את המנגנון, שעשוי לשמש בסיס לפיתוח תרופה," מסכם פרופ' אשרי. "כיום נמצאת התרופה הפוטנציאלית בשלב הניסויים הקליניים. כמו כן אנחנו מחפשים דרך לאתר משקעי אלפא-סינוקלאין קטנים, כבר בשלב מוקדם של המחלה, אצל בני אדם. מכיוון שלא ניתן לחדור לשם כך למוח, אנחנו מחפשים את המשקעים הללו ברקמות/הפרשות נגישות יותר בגוף – בדגימות עור, ובעתיד אולי אף בדמעות של חולים וחולים פוטנציאליים."

תגובה אחת
במחקר אחר באוניברסיטת תל אביב (פרופ' אהוד גזית) נמצא כי המניטול הוא חומר שעשוי "לפרק" את אות משקעים. האם יש קשר בין שניהחומרים מפרקי המשקעים?