מחקר חדש מגלה כי החזרת פעילותו של גן קדום מאפשר לעכברים לחדש רקמות פגועות באוזן – ממצא שעשוי לסלול את הדרך לפריצות דרך ברפואה רגנרטיבית
מחקר חדש בראשות המכון הלאומי למדעי הביולוגיה בבייג'ינג מגלה כי הפעלת גן רדום בודד מאפשרת לעכברים לחדש רקמה באוזן – יכולת שנחשבה לאבידה ביונקים.
בעוד שחלק מבעלי החוליות, כמו סלמנדרות ודגים, מסוגלים לשקם מבנים מורכבים בגופם בדיוק מרשים – כולל גפיים, לב ועיניים – יונקים לרוב חסרים תכונה זו. אף על פי כן, גם בקרב יונקים קיימות דוגמאות להתחדשות חלקית: עכברים יכולים לחדש קצות אצבעות, קרני צבאים ועזים גדלות מחדש לאחר נשירתן, והכבד האנושי מסוגל להתחדש כמעט לגודלו המלא גם לאחר הסרה של עד 70% מנפחו.
עם זאת, ברוב המקרים החליפו היונקים את היכולת האבולוציונית להתחדשות בתגובה של יצירת צלקות – פתרון מיידי להישרדות, אך חסר את יכולת השחזור המלא של הרקמה.
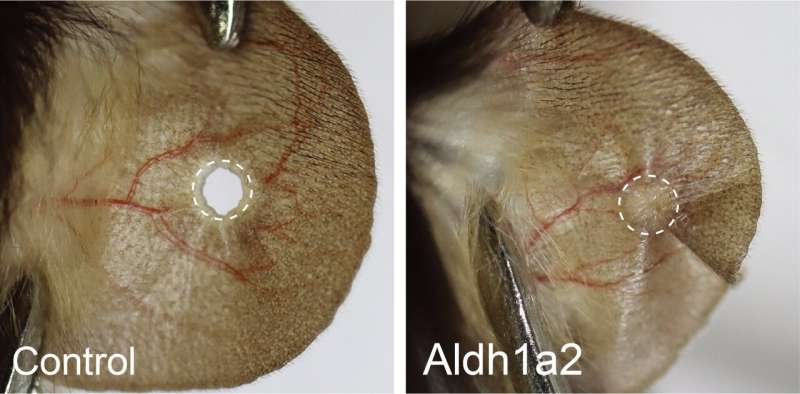
במחקר הנוכחי נבחנו עכברים מזן מעבדה רגיל, שאינם מתחדשים, לעומת זנים יוצאי דופן כמו עכברי מרפי רוטס גדולים, המסוגלים לסגור חורים באוזן בקוטר 2 מ"מ מבלי להותיר צלקת. עכברים אלו מחדשים סחוס, עור, זקיקי שיער ואף עצבים – ואף הפגינו יכולת מסוימת לתיקון נזקי לב. גם בארנבות התגלתה יכולת זו של התחדשות רקמת האוזן, מה שמרמז על כך שהיכולת נבעה מאב קדמון משותף.
למרות התפצלות אבולוציונית לפני כ-90 מיליון שנה, התגלה כי הגן Aldh1a2 – האחראי לסינתזת חומצה רטינואית (RA) – שמר על נוכחותו גם במינים שאיבדו את היכולת להתחדש. עם זאת, חיווט רגולטורי שונה כיבה את התגובה ההתחדשותית ברוב המכרסמים, בעוד שהיא נותרה פעילה בשושלות מסוימות של עכברים וארנבים.
יונקים בעלי יכולת התחדשות וכאלה שרק מפתחים צלקת
המחקר, שפורסם בכתב העת Science תחת הכותרת "Reactivation of mammalian regeneration by turning on an evolutionarily disabled genetic switch", השווה גנומית בין יונקים בעלי יכולת התחדשות (כמו ארנבות, עיזים ועכברים קוצניים אפריקאים) ליונקים שאינם מתחדשים (עכברים וחולדות רגילים). החוקרים השתמשו במגוון טכניקות מתקדמות, בהן ריצוף RNA של תאים בודדים, ריצוף RNA בכמות גדולה, ChIP-seq, ATAC-seq ו-Micro-C, כדי לנתח את פעילות הגנים בפיברובלסטים – תאים חיוניים לריפוי רקמות.
המחקר העלה כי הארנבות יצרו חומצה רטינואית (RA) באמצעות האנזים Aldh1a2 מיד לאחר פציעה, דבר שהוביל להתחדשות מוצלחת של רקמות האוזן. לעומת זאת, בעכברים רמת האנזים הייתה נמוכה מדי ולא הספיקה ליצור חומצה רטינואית בכמות הדרושה לשיקום.
כאשר החוקרים הזריקו לעכברים חומצה רטינואית באופן ישיר – או את הקדם שלה, רטינול – הם הצליחו לגרום להתחדשות מלאה של הסחוס והעצבים הפגועים באוזן. לעומת זאת, עיכוב יצירת החומצה בארנבות עיכב את ההתחדשות, מה שמחזק את תפקידה המכריע של RA בתהליך.
עוד נמצא כי הכנסת משפר רגולטורי שמקורו בגנום הארנבת – המכונה AE1 – לעכברים טרנסגניים גרמה להגברת הביטוי של Aldh1a2 לאחר פציעה ולהתחדשות חלקית של רקמות. אף על פי שצמיחה זו הייתה פחות שלמה מהשפעת RA ישירה, היא מהווה עדות לכך שדי באלמנט רגולטורי אחד כדי להפעיל מחדש מסלול התחדשות עתיק.
המחקר גם זיהה רצפי DNA רגולטוריים אשר נדרשים להתחדשות לאחר פציעה, אך הפכו בלתי פעילים ביונקים שאינם מתחדשים. הפעלתם המחודשת עוררה תהליכי התחדשות, בעוד שהזרקת RA דילגה לחלוטין על הצורך בפעולה הגנטית – והובילה לתוצאות טובות אף יותר.
תגליות אלו צפויות לעורר עניין רב בתחום הרפואה הרגנרטיבית, ולפתוח אפיקים חדשים בטיפול בפציעות חמורות, מחלות עור, פגיעות עצביות ואף קרחות – על ידי הפעלת מנגנונים ביולוגיים רדומים שכבר קיימים בגוף.
עוד בנושא באתר הידען:
