השיטה שפיתחו חוקרים באוניברסיטת תל אביב מתבססת על טכניקת האלקטרופורציה שמגדילה את חדירות התאים באמצעות שדה חשמלי * פרופ' אלכס גולברג: השיטה החדשה עשויה לסייע בקידום הגישה של רפואה מותאמת אישית
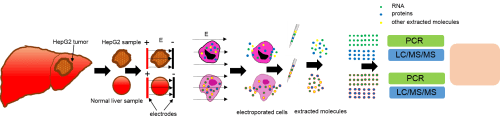
חוקרים באוניברסיטת תל אביב, בהובלת פרופ' אלכס גולברג מבית הספר ללימודי הסביבה, ובשיתוף עם קבוצתו של פרופ' זהר יכיני מהמרכז הבינתחומי הרצליה ומהטכניון, פיתחו שיטה חדשנית לדגימת רקמות, העשויה לחסוך מהחולים את הכאב והסיכון שבביופסיות חוזרות בגישה המסורתית. השיטה החדשנית מסתמכת על הטכניקה הפיזיקלית של אלקטרופורציה – הגדלת חדירות התאים בעזרת שדה חשמלי – במטרה לדגום נוזלים תוך תאיים בלבד (לא רקמה שלמה).
במחקר השתתפה החוקרת יוליה שביריוב ממעבדתו של פרופ' גולברג. המאמר התפרסם לאחרונה בכתב העת Scientific Reports .
"דגימת רקמות בכלל ורקמות מגידולים סרטניים ומסביבתם בפרט היא הליך נפוץ ברפואה, ויש לה חשיבות מיוחדת ברפואה מותאמת אישית," מסביר פרופ' יכיני. "הדגימות משמשות לאבחון ולאיפיון מבני ומולקולרי, במטרה לזהות את סוג הגידול ולצפות מראש את תגובתו לטיפולים שונים. כיום מבוצעות הדגימות בעיקר באמצעות ביופסיה – חיתוך והוצאה של פיסת רקמה, אך לשיטה זו יש מספר חסרונות: היא גורמת לפציעה ולדימום ואף לדלקת וכאב במקום הביופסיה, וחשוב מכך, הדגימה שנלקחת בדרך זו היא מקומית, ואינה מספקת מיפוי מקיף על הגידול כולו. אנחנו ביקשנו לפתח שיטה חלופית שעשויה להרחיב את המידע המופק מההליך, על ידי דיגום נוזלים מהרקמה בעזרת שדה חשמלי."

לדברי פרופ' גולברג, מדובר בטכניקה פיזיקלית בשם אלקטרופורציה, שבה משתמשים בשדה חשמלי כדי להגדיל את החדירות של קרום התא. עד היום שימשה טכנולוגיה זו בעיקר להחדרת מולקולות (כמו DNA או תרופות) לתוך התא, למשל בהליכים של הנדסה גנטית, או למיצוי מולקולות מצמחים בתעשיית המזון.
החוקרים נטלו דגימות מכליה וכבד של עכברים בריאים ומסרטן כבד אנושי שהושתל בעכברים, וחשפו את הרקמות לשילוב של פולסים חשמליים – 50 פולסים קצרים במתח גבוה של 500 וולט ו-50 פולסים ארוכים במתח נמוך של 50 וולט. ההליך הפיק מהרקמה נוזל, שממנו הופקו לאחר מכן מולקולות של חלבונים ו-RNA. איפיון החלבונים שמוצו מהרקמות העלה כי הפרופיל המולקולרי של הדגימות שנמדדו בדרך זו דומה לפרופילים המוכרים מהספרות המדעית שהדרך להשגו היתה ביופסיה שלמה של הרקמה, ומספק מידע אמין ומדויק יחסית על הרקמות הנבדקות.
"במחקר שלנו פיתחנו שיטה חדשנית לנטילת דגימות מולקולריות מרקמות, על ידי חשיפתן לשדות חשמליים, " מסכם פרופ' גולברג."מיצוי מולקולות עם פולסים חשמלים מאפשר זיהוי רקמות סרטניות לעומת רקמות רגילות" לגישה שלנו יש מספר יתרונות על שיטות הביופסיה המקובלות: היא אינה פוגעת ברקמה עצמה – פגיעה שעלולה לייצר דלקת ואף לעודד היווצרות גרורות; היא יכולה לזהות הימצאות של גידול סרטני באיבר מסוים גם כשמקומו המדויק של הגידול אינו ידוע; והיא יכולה לאפשר דגימה ממקומות שונים ומיפוי מקיף של הרקמה או הגידול. הממצאים שלנו עשויים לשמש בסיס לפיתוח גישה חדשה לנטילת דגימות לאיפיון גידולים סרטניים בבני אדם, שתסייע מאוד לרפואה המותאמת אישית."
