מדענים הצליחו לפתח שיטה חדשנית שבעזרתה ניתן "להסתכל" על חלבונים בעודם מתקפלים – בפחות מאלפית השנייה – לצורות המשוכללות והמפותלות הקובעות את פעילותם.
לבני-האדם יש כשלושים אלפי גנים, האחראיים ליצירתם של יותר משני מיליוני חלבונים. מולקולות החלבונים הן אלה המבצעות את רוב העבודה בתאים.
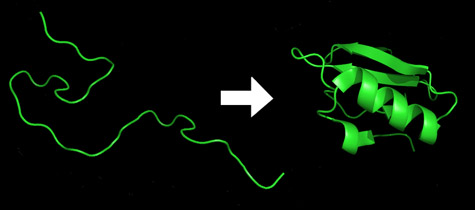
חלבונים מתקבלים כשרשראות ישרות של חומצות אמינו המתקפלות באופן עצמאי למה שמכונה "הצורה הטבעית" שלהם תוך מספר מילי-שניות/שניות. פעילותו של החלבון תלויה באופן חד בצורתו הסופית. לדוגמא, אנזימים והמולקולות שעוברות שינוי בעזרתם מתוארים תכופות כמתאימים אחד לשנייה כעין מנעול והמפתח שלו. על-פי אותו היגיון, חלבונים בעלי קיפול שגוי הם האחראיים למספר מחלות נוירו-ניווניות מהסוג הנורא ביותר, כגון מחלת אלצהיימר, פרקינסון והפרה המשוגעת.
שיטות בדיקה קיימות אינן מסוגלות להשתוות למהירות שבה החלבונים מתקפלים. חיזוי צורת הקיפול של החלבונים ללא ידע קודם מחייב שימוש במחשבי-על עוצמתיים או בשיטה של "מחשוב ענן" (ניצול כוח המחשוב המשותף של מספר רב של מחשבים ביתיים). כך או כך, חיזוי מהווה שיטה ממושכת ולעיתים בלתי-מדויקת, ובעקבות כך, העיכוב בהבנת התלות שבין חלבון לבין המבנה שלו מאט את ניצול המידע של רצף הדנ"א בתחומי הרפואה והביוטכנולוגיה. שיטה מתוחכמת לצפייה בתהליכים בהם חלבונים מתקפלים ונפרשים תוכל אולי, בסופו של דבר, לספק את סוג הפרטים הדרוש על-מנת לשפר את איכות חיזוי מבנה החלבונים.
בגיליון האחרון של גרסת הרשת של כתב העת המדעי Journal of the American Chemical Society, שלושה מדענים, בראשות ד"ר Michael L. Gross, פרופסור לכימיה באוניברסיטת וושינגטון שבסנט-לואיס, מתארים מחקר ראשוני שבו הם השתמשו בגישה חדשנית על-מנת לצפות בקיפולם של חלבונים קטנים המכונים barstar.
השיטה שלהם דומה, בצורה כללית, לשיטה שבה מצלמים כיום קליעים עפים או בלונים מתפקעים באמצעות סטרובוסקופ (מכשיר למעקב אחר עצמים בתנועה מחזורית) ומצלמה מהירת-פעילות. המדענים מנצלים גירסה מקבילה של שיטה מוכרת זו בכדי "לצפות" בחלבונים מתקפלים. "אור הסטרובוסקופ" במקרה זה הינו קפיצה בטמפרטורה ו"המצלמה" הינה תגובה כימית שתוצאתה נמדדת באמצעות ספקטרומטר-מסות רגיש.
"דמיינו את החלבון כרצף של אלפי אטומים הקשורים יחדיו באמצעות קפיצים," מסביר החוקר הראשי. "אם נתלה את השרשרת הזו מהתקרה באמצעות חוט וניתן לה להתנדנד, דמיינו את מספר הצורות הכה רב שיתקבל."
הצורה הטבעית של חלבוני barstar ורצף חומצות האמינו שלהם ידועים ומוכרים. מה שלא ידוע הוא כיצד הרצף מתפתל ומתקפל לצורתו המבנית הסופית. למרבה המזל של המדענים, חלבוני barstar, שלא כמו רוב החלבונים, אינם מקופלים בטמפרטורה של אפס מעלות צלזיוס, והם מתחילים להתקפל רק לאחר חימומם. הקיפול עצמו נמשך מיקרו-שניות בלבד.
המדענים החלו את הבדיקה ע"י הזרקת תמיסה קרה של החלבונים וכמות קטנה של מי-חמצן לתוך סיב אופטי זערורי וחלול. בשלב הבא, גושים זערוריים של הדגימה המצויה בסיב מחוממים באמצעות פעימות לייזר מהירות. הפעימה הראשונה מחממת את התמיסה עד השלב שבו תצורת מבנה חלבוני מסוימת מועדפת אנרגטית. הפעימה השנייה מפרקת חלק ממולקולות מי-החמצן לשני חצאים שכל אחד מהם מהווה רדיקל פעיל ביותר (הידרוקסיל). רדיקלים אלו מגיבים במהירות עם חלקי החלבון החשופים לתמיסה, ו"מסמנים" אותם באטומי חמצן. תגובות הרדיקלים חייבות להסתיים במהירות רבה; אחרת, חלק מהסימון יתרחש בחלקים הפנימיים של המבנה. בתוך מיקרושניות, חומצות אמינו המשמשות כלוכדות רדיקלים מנטרלות את כל הרדיקלים העודפים שנותרו, וזאת בכדי למנוע מהם לפרק קשרים או לשנות את צורתו של החלבון. על התהליך הזה חוזרים שוב ושוב כחמש מאות פעמים, תוך קבלת "תמונות" של המסלול שבו החלבון משנה את תצורתו במהירות. "הרדיקלים אינם מסמנים את כל האטומים," מציין החוקר הראשי. "אולם, הם מסמנים כמחצית מחומצות האמינו, תוצאה די טובה. רוב החומרים הכימיים האחרים בררניים מדי או שהם איטיים מדי לניסוי מסוג זה." "אנו אוספים כל טיפה של חלבון מסומן בעת יציאתו מהסיב," מסביר החוקר.
"בשלב הבא אנו חותכים את החלבון באופן איטי וזהיר באמצעות אנזים המפרק את שרשראות חומצות האמינו בנקודות מוגדרות וידועות מראש, לקבלת מקטעי חלבון ידועים, המכונים פפטידים. מקטעי חלבון אלו מופרדים בשלב הבא בהתאם לטיבם באמצעות כרומטוגרפיה נוזלית, וספקטרומטר-מסות "שוקל" לאחר מכן את הכמות של כל אחד מהסוגים הללו בכדי לבחון אם הם מסומנים בחמצן אם לאו. "בעזרת אותו המכשיר אנו ממשיכים ומפרקים את מקטעי החלבון שוב ושוב ובודקים אם הם מכילים את החמצן המסומן."
"מכיוון שאנו משתמשים במדיד בדיקה כימי ולא פיסיקאלי, אנו מסוגלים לבחון את התהליך ביתר פירוט," מסביר החוקר. "אנו מסוגלים לקבוע איזה חלק מהמבנה הסופי מתקפל ראשון, איזה שני וכן הלאה."

2 תגובות
קראתי עכשיו באתר "הדוס" מאמר ארוך של פרופ' דורון אורבך וזה עשה אותי עצוב.
הקרב על השפיות של האנושות ארוך קשה ונראה שאנחנו מפסידים בו.
צריך להקים מדינה אתאיסטית באיזה אי באוקינוס השקט ולעזוב את האנושות שתסדר בעצמה.
ממליץ על 2 קורסים מצויינים בנושא ביולוגיה וחקר המוח, בראשון מוסבר בצורה יפה גם נושא קיפול החלבונים:
http://www.youtube.com/view_play_list?p=ACC83028E0CBD671
http://www.youtube.com/view_play_list?p=D8C99F67C81778E8