שתי טיפות. זה כל מה שהיה צריך כדי לרפא את אייסאם דאם מחירשות מולדת, לנצח. שתי טיפות שהוזלפו לאוזנו והקנו לילד בן ה- 11 את היכולת לשמוע – לראשונה בחייו – קולות אדם
שתי טיפות. זה כל מה שהיה צריך כדי לרפא את אייסאם דאם מחירשות מולדת, לנצח. שתי טיפות שהוזלפו לאוזנו והקנו לילד בן ה- 11 את היכולת לשמוע – לראשונה בחייו – קולות אדם. על הדרך, אותן שתי טיפות מסמנות המשך ההתקדמות במחלות שנחשבו לחשוכות-מרפא עד כה, וגם הצליחו להקפיץ כמה אנשים בקהילת החירשים – ולא לטובה.
אבל נתחיל בהתחלה.
הילד שלא יכל לשמוע
אייסאם הגיח מבטן אמו לעולם של דממה מוחלטת. הפעוט גדל במרוקו כשהוא מבטא את רצונותיו לסביבה בשפת סימנים שהמציא בעצמו. בגיל עשר היגרה משפחתו לספרד, והילד זכה לראות מומחה שמיעה שהציע להם להירשם לטיפול יוצא-דופן: לניסוי קליני בהנדסה גנטית שעשויה לרפא את חירשותו.
הסיבה להצעה המפתה היא שאייסאם לוקה בחירשות גנטית מסוג מאד מסוים, המשותף רק לעוד 200,000 בני-אדם בערך בכל העולם. החירשות נגרמת כתוצאה ממוטציה בגן בודד, ששמו אוטופרלין (לא כמו אוטו שוקולדים, מכיוון שה- פ' אינה דגושה). המוטציה מביאה לכך שאחד מהחלבונים הקריטיים בתאי השערה שבאוזן הפנימית נהרס, כך שהתאים אינם מסוגלים לקלוט גלי קול מהסביבה. בשונה ממחלות חירשות גנטית אחרות, המוטציה באוטופרלין אינה גורמת למותם של תאי השערה. הם ממשיכים להתקיים, אך מבלי שיוכלו לבצע את תפקידם. כדי לרפא את המחלה, צריך רק להשלים את החסר באמצעות הטמעת הגן המתוקן בדנ"א של התאים.
צריך גם חולים שיסכימו לקבל את הטיפול, וכאן אייסאם נכנס לתמונה, ביחד עם שמונה ילדים בסין, מכיוון שהמחקר נערך במשותף עם חוקרים מהמדינה. הכל בתמיכת ענקית התרופות אלי-לילי, וחברת הביו-טכנולוגיה אקואוס (Akuous).
למה כל הילדים במחקר מגיעים ממדינות מתפתחות? התשובה מוסיפה עוד נדבך של מורכבות לטיפול.
כשהמדע הבדיוני הופך להיסטוריה
לפני עשור בערך התחילו להופיע ברחובות הערים אנשים – ילדים ומבוגרים כאחד – עם כפתור אלקטרוני עתידני-למראה שמחובר לגולגולותיהם. יש סיכוי די טוב שראיתם את האנשים האלו בעצמכם בבית-הספר, באוניברסיטה, בעבודה או בתחבורה הציבורית. כל אותם אנשים היו סובלים מחירשות מוחלטת אילולא אותו 'כפתור' שמאפשר להם לשמוע את הסביבה ולנהל חיים רגילים לגמרי.
הכפתור שעל הגולגולת הוא רק המשדר – ולעתים גם המיקרופון – שמתרגם את הקולות והרעשים מהסביבה לאותות אלקטרוניים, ומעביר אותם ל- "שתל שבלולי". מהו אותו שתל שבלולי? אלו אלקטרודות שהושתלו בתוך השבלול: אזור באוזן הפנימית שמעביר למוח מידע על קולות המגיעים מהסביבה. בחירשים רבים התאים שבשבלול אינם מסוגלים לעשות את עבודתם, ולכן האלקטרודות מחליפות אותם ומעבירות את המידע ישירות לעצבים.
השתלים השבלוליים הצילו את שמיעתם של רבים, אבל כדי שיוכלו לעבוד היטב בילדים, צריך להשתיל אותם כבר בגיל צעיר. לראיה, אפשר למצוא בגנים היום פעוטות עם השתל השבלולי, שמאפשר להם לתפקד ככל חבריהם. לרוע המזל, השתלים משנים בעצמם את מבנה ותפקוד השבלול, וכך הם עשויים דווקא לסבך את הניסויים בהנדסה גנטית שאמורים לרפא חירשות.
זו הייתה הסיבה שכל המטופלים בניסוי הנוכחי הגיעו ממדינות עניות, בהן קשה יותר למצוא מימון לשתל שבלולי עבור כל ילד. אייסאם דאם, שמשפחתו אינה משופעת בכסף בלשון המעטה, לא זכה בשתל שבלולי כזה בילדותו, ולכן התאים לקבל את הטיפול הנסיוני החדש בחינם – ואפילו קיבל כיסוי להוצאות השהייה בפילדלפיה, שם הוזלפו לתוך אוזנו אותן טיפות שפתחנו בהן את המאמר.
הטיפות עשו את עבודתן במהירות יוצאת-דופן. הן הכילו מספר עצום של וירוסים לא-מזיקים, שהכילו את הגרסה המתוקנת של אוטופרלין והזריקו אותה לתוך תאי השערה שבשבלול. התאים קיבלו את התיקון לקוד הגנטי שלהם והחלו לפעול לפיו.
תוך פחות משבוע אייסאם הצליח לשמוע צלילים לראשונה בחייו.
חודשיים לאחר מכן, יכולת השמיעה שלו הייתה כבר קרובה לרמת השמיעה של אדם רגיל.
לפני שנתרגש כולנו עד הגג – ויש ממה להתרגש – חייבים להכיר בכך שלא מדובר בסיפור אגדה מעולמות דיסני. אייסאם לא יוצא לרחובות בשירים ובריקודים. למוח יש חלון הזדמנויות צר מאד לפתח את יכולת הדיבור, והוא נסגר בסביבות גיל חמש. אייסאם כבר לא ידבר ברור לעולם, אך לפחות הוא יוכל לדעת כאשר אחרים מנסים לתקשר איתו, לשמוע מוזיקה וליהנות מנאומי פוליטיקאים. אבל אייסאם, עם כל הכבוד והשמחה על הטיפול המוצלח שעבר, השתתף בניסוי רק כדרך להדגמת יכולותיו של הטיפול החדש. הוא מעולם לא היה אמור להיות אחד מאלו שיפיקו ממנו את המירב.
למי הטיפול החדש מיועד באמת? לאלפי התינוקות שנולדים מדי שנה עם החירשות הגנטית הזו, ועתה יוכלו להיפטר ממנה לאחר טיפול בודד. וכל בר דעת מבין שהמהפכה לא תעצור כאן. בעיות גנטיות אחרות שמובילות לחירשות עשויות להיות מסובכות יותר, אבל במוקדם או במאוחר נצליח להתמודד גם איתן ולרפאן.
וההתקדמות הזו, מרגשת ככל שתהיה, מאד מפחידה חלק מהאנשים. במיוחד את החירשים.
תרבות החירשים
דמיינו כוכב-לכת ששמו איית' (Eyeth). זהו עיוות ומשחק מילים על שמו של כדור-הארץ באנגלית – Earth – שכולל בתוכו את המילה "אוזן" (ear). ובכן, איית' באנגלית כולל בתוך שמו את המילה "עין". איית' הוא כוכב-הלכת של "אנשי העיניים". כמעט כל תושבי איית' משתמשים בראייה כדרך לקלוט מסרים שפתיים: במילים אחרות, הם מתקשרים באמצעות שפת סימנים. מיעוט שבמיעוט מתוך תושבי איית' מסוגלים גם לשמוע.
תושבי איית' מקיימים ציביליזציה עם תרבות עשירה ומרתקת. יש להם מספר שפות סימנים שונות משלהם, כל אחת עם דקויותיה. הם חדי-מחשבה וחדי-עין, ושמים לב לתנועת כל שריר ושריר בפניו של בן 'שיחם'. הם אמנם אינם מסוגלים לשמוע, אבל הם מוצאים הנאה בשפע של פעילויות חברתיות ואפילו יצירות אומנות שאינן מחייבות קליטת גלי-קול מהאוויר ופענוחם ברזולוציה גבוהה. כאשר לתושבי איית' נולד ילד המסוגל לשמוע, ההורים לעתים קרובות נותרים מבולבלים: מה לעשות עם התינוק שמגיב בדרכים מוזרות ולא-צפויות לסביבה? כיצד עליהם להתמודד עם ילד שמכסה את אוזניו לפתע ללא סיבה מובנת?
אם איית' נשמע לכם כמו מקום מרתק לבקר בו, אתם לא צריכים להתאמץ יותר מדי. לכו להתערות בקהילת החירשים על פני כדור-הארץ עצמו, ותגלו את איית' על פני האדמה. תגלו גם שלמרות שחלק מהחירשים מעוניינים לשקם את שמיעתם, הרי שאחרים מתייחסים ללקות השמיעה כאל כרטיס כניסה לאותה קהילה, וכאל תכונה המאפיינת ומייחדת אותם. חלק מההורים החירשים מקיימים מסיבה כאשר הם מגלים שגם ילדם חירש, ולפיכך יוכל להיות חלק מהקהילה. אפשר להבין אותם. אף אחד לא רוצה לנטוש את כוכב-הלכת, את הציביליזציה והתרבות בהם גדל.
אין פלא שבקרב חלק מחברי קהילת החירשים, אפשרות הטיפול בחירשות בהנדסה גנטית נתפסת כ- "איום קיומי לשגשוגן של קהילות החירשים." היא מפחידה אותם, ובה באותה עת בה היא בוודאי מרגשת ומלהיבה הורים אחרים מקהילת החירשים, שאינם רוצים שילדיהם יתמודדו עם אותם קשיים שהם חוו.
הטיפול הנוכחי לא יאיים יותר מדי על קהילת החירשים, מכיוון שהוא מיועד למחלה אחת בלבד. אבל מה יקרה כאשר יתרחב ויכלול פגמים גנטיים נוספים הפוגעים בשמיעה? האם נכון לשלול מילדים את "זכותם מלידה" לקחת חלק בקהילת החירשים? האם אין כאן איום ממשי על תרבות אחרת? אין עדיין תשובות טובות לשאלות אלו, וכנראה שכל הורה יצטרך להחליט בפני עצמו כיצד לפעול.
מחירן של שתי טיפות
סוג האנשים האחר שלא לגמרי בטוח כיצד להתייחס להתפתחות המשמחת הזו, הוא אנשי השיווק העובדים בחברות התרופות. אלו רואים את המגמות ומבינים לאן העולם הולך: לטיפולים בהנדסה גנטית, המסוגלים כמעט בין-לילה לשנות את מצבו של ילד מחולה אנוש לאינדיבידואל מתפקד עם תוחלת חיים רגילה לגמרי. וזה נהדר, אבל מה יהיה תג המחיר של התרופות החדשות הללו?
המודל המקובל כיום בתעשיית הפארמה הוא זה בו הלקוחות רוכשים תרופות – בין שמדובר בכדורים, גלולות או אמפולות להזרקה – מדי שבוע-שבועיים. כל אחד מהכדורים מתומחר בדרך שתתגמל את חברת התרופות על המחקר והפיתוח הרב שהשקיעה באותה תרופה – עלות שמגיעה לעתים קרובות לעשרות-מיליוני דולרים. עלות שכזו מצדיקה את עצמה בטווח הארוך, מכיוון שהחולים ממשיכים לעתים קרובות לקחת את הכדורים לכל אורך חייהם.
מה קורה כשהם צריכים לקחת את התרופה פעם אחת בלבד – וזהו?
אנחנו מתחילים לראות את התשובה מגיעה מהשטח. ב- 2019 התרופה היקרה ביותר היתה זולגנסמה, שמתן חד-פעמי שלה תומחר ב- 2.1 מיליון דולרים. מאז הופיעו עוד כמה טיפולים חד-פעמיים בהנדסה גנטית, וזולגנסמה נותרה הרחק מאחור מבחינת המחירים. התרופות היקרות ביותר מהשנתיים האחרונות – סקייסונה לטיפול בבעיה מוחית בילדים, אלווידיס לטיפול בניוון שרירים והמג'ניקס לטיפול בהמופיליה – כבר עולות יותר משלושה מיליון דולרים לטיפול אחד.
נשמע הרבה? ובכן, זה באמת הרבה כסף, אבל צריך לזכור שהוא מגיע לחברות התרופות בזכות, כתמורה על כל מאמצי הפיתוח שלהן לאורך שנים ארוכות. מעבר לכך, חברות הביטוח הן אלו שמכסות כמעט את כל עלות התרופה, ואם הן מחליטות שהיא אינה מצדיקה את העלות – הרי שמחירה ירד בהתאם. העובדה שחברות התרופות יכולות לגבות סכומים שכאלו על התרופות, מעידה על כך שהן פועלות היטב ומצמצמות דרמטית את שכיחות האשפוזים ויתר הטיפולים הרפואיים המסובכים שנמשכים לעתים קרובות לאורך כל חיי המטופל. בסופו של דבר, חברות הביטוח הרפואי מעדיפות לשלם את הסכום הזה – ואפילו רואות זאת כעסקה רווחית.
ובכל זאת, מדובר במודל שיווקי שונה מאד מזה אליו התרגלו רוב חברות התרופות עד כה. אנשי המכירות יצטרכו להתרגל לדרכי השיווק החדשות ולמחירים החדשים. אל תדאגו להם. הם ישרדו.
המשמעות הגדולה
המשמעות האמיתית של הטיפול החדש בחירשות היא שההנדסה הגנטית ממשיכה להתקדם ולהצליח ככל שהזמן עובר. זה צריך לשמח את כולנו. ילדים שהיו גדלים לחיים של קושי וטיפולים רפואיים בלתי-פוסקים, עומדים לקבל טיפולים גנטיים כנגד בטא-תלסמיה, המופיליה, חירשות – ולהחלים כאילו מעולם לא נשאו את המחלה מלכתחילה.
זו, כמובן, תהיה רק ההתחלה.
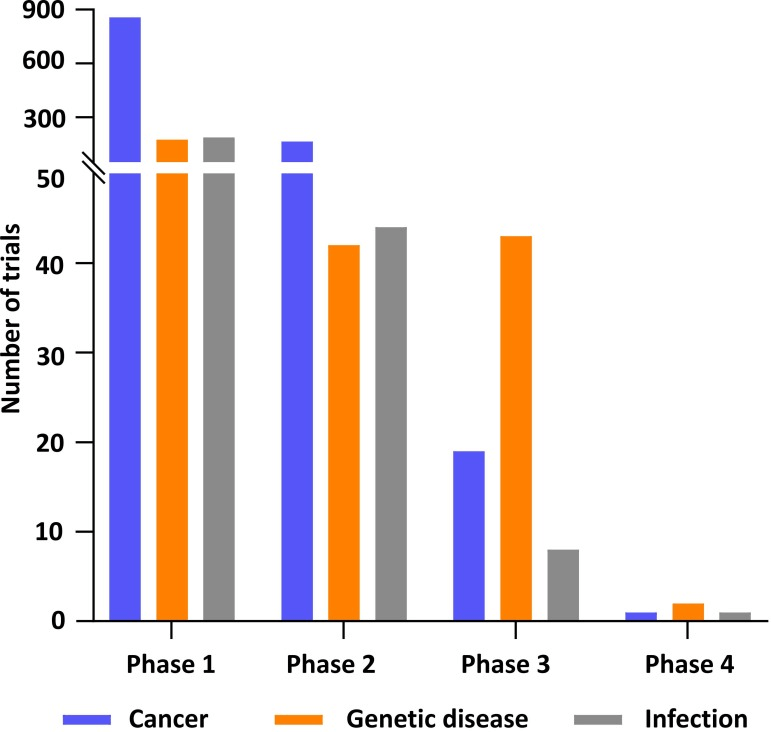
בסקירה שנערכה ב- 2022, חזו החוקרים שעד 2025 יאושרו עשרות טיפולים חדשים המבוססים על הנדסה גנטית. ניסויים קליניים בטיפולים כאלו אורכים יותר מהרגיל – בערך 3.5 שנים למחלות גנטיות – אבל אם התוצאות יהיו כפי שראינו עד כה, הרי ששווה לחכות.
הטיפולים בשלבי הניסוי המתקדמים ביותר כרגע מתמקדים במחלות גנטיות, עם יותר מארבעים טיפולים בשלבי הניסויים הקליניים. הטיפולים הללו מכסים מגוון מחלות גנטיות עם שמות לועזיים שוברי-שיניים: פמיליאל כילומיקונמיה סינדרום, עמילואיד נוירופאתי, ליפופרוטאין ליפאז דפיצ'נסי, פריימרי היפראוקסאלוריה ועוד ועוד. אני יכול לכתוב מאמר שלם על העבר וההווה של כל אחת מהמחלות האלו, אבל התקווה היא שבזכות ההנדסה הגנטית – לא יהיה בכך צורך. אנו נעלים אותן מן העולם. רופאי העתיד לא ילמדו כיצד לטפל במחלות האלו. הן ייכללו בסילבוס בפקולטות לרפואה רק כשיירים מן העבר, כפי שהם אינם לומדים כיום לטפל במחלת האבעבועות השחורות, שהאנושות הכחידה במאמץ כביר לפני כמעט חמישים שנים.
מחלות גנטיות אינן גורם הסבל היחיד בעולם. אחרי שנות הקורונה, לא צריך לפרט אודות הסכנות הטמונות במחלות מדבקות מכל הסוגים. חיידק השחפת גובה את חייהם של יותר ממיליון בני-אדם מדי שנה. טפיל המלאריה קוטל 620,000 בני-אדם בשנה, ומתחרה רק בנגיף ה- HIV שגורם למחלת האיידס, עם 630,000 קורבנות שנתיים. וכמובן, ה- man-flu יהרוג מחצית מהאנושות במוקדם או במאוחר (למרות שלא הצלחתי למצוא מקור מדעי מוסמך לטענה המסוימת הזו).
מה אם היינו יכולים לחסן את בני-האדם כנגד המחלות המדבקות הללו? זה עשוי להיות אפשרי, למרות שכנראה שלא יקרה בעשור הקרוב. אנו רואים שבשלבים המוקדמים יותר בניסויים הקליניים אפשר למצוא כיום יותר מתשעים טיפולים בהנדסה גנטית למחלות מדבקות, כאשר רובם מחסנים את הגוף כנגד אותן מחלות. ההתמקדות כרגע היא במתן חסינות לאיידס, לקוביד-19, למלאריה, לאבולה, להפטיטיס C ו- B ולהדבקה בנגיף הפפילומה האנושי.
ההצלחה בכל אלו לא תגיע מחר בבוקר, כמובן. ובכל זאת, אם אשרוד את ה- man-flu ואכתוב על הנדסה גנטית בעוד עשור, יש סיכוי טוב שאספר כבר על הילדים והמבוגרים הראשונים שקיבלו חיסון בהנדסה גנטית כנגד חיידקים, נגיפים וטפילים שקטלו בבני-האדם מאז שחר ההיסטוריה. עשור לאחר מכן – כאשר נתקרב לאמצע המאה ה- 21 – אנו עשויים כבר לראות מבצעי חיסונים רחבי-היקף שיינתנו פעם אחת בלבד, ויעלימו מן העולם מחלות מדבקות ואפילו חלק מסוגי הסרטן.
אם וכאשר נצליח בכל זאת, נוכל לחגוג את הצלחת המדע, החדשנות והמחקר האנושיים שהובילו אותנו להישגים הכבירים הללו. מסיבות יתקיימו בכל העולם, זיקוקי דינור ישוגרו לאוויר ומוזיקה שמחה תמלא את הרחובות.
אייסאם דאם, הילד שנולד חירש בצו הגורל ונרפא בזכות האדם, יוכל לשמוע את כל אלו.
עוד בנושא באתר הידען:
