מודל בינה מלאכותית שופך אור על מסלול ההתמחות של תאי שריר וחושף צומת בקרה חשוב בדרך
מדעי החיים מעולם לא היו דיגיטליים יותר. ביולוגים אוספים כמויות נתונים אדירות ונדרשים למודלים חישוביים משוכללים כדי לפענח אותם וללמוד דבר מה חדש על תהליכי החיים. ד”ר אורי אבינעם מהמחלקה למדעים ביומולקולריים במכון ויצמן למדע התמודד בשנים האחרונות עם שאלה ביולוגית לא פתורה – כיצד נוצרים סיבי שריר חדשים מתאי גזע? בחיפוש אחר תשובות הוא שיתף בבעיה את חברו – ד”ר אסף זריצקי מהמחלקה להנדסת מערכות תוכנה ומידע באוניברסיטת בן-גוריון בנגב – ויחד הם החלו לפתח מודל למידת מכונה שיוכל לפענח את התהליך הביולוגי המורכב. תגליות המודל מוצגות במאמר שהתפרסם באחרונה בכתב-העת המדעי Molecular Systems Biology ומראות כי באופן מפתיע בעת בנייתו של שריר כל תא גזע עובר תהליך התבגרות ייחודי לו.
תאי הגזע שמהם מתפתחת רקמת השריר נוצרים בעובר, אך קמצוץ מהם נשמר בשרירים בוגרים. תאים אלו רדומים רוב הזמן, אך בעת גדילה, פעילות גופנית מאומצת או פציעה הם נכנסים לפעולה. בשלב הראשון, תאי הגזע שהופעלו מתחלקים כדי לחדש את הרקמה. לאחר מכן, הם מפסיקים להתחלק ועוברים “התמיינות” – תהליך התבגרות של תאי גזע שבמסגרתו הם מתמחים בתפקיד ייחודי ורוכשים תכונות הדרושות לביצועו. במקרה של השריר, תאי הגזע המתמיינים מתארכים, מייצרים סיבי חלבון המאפשרים את פעולת הכיווץ המוכרת של השרירים – ומהגרים למקום שבו הרקמה מתחדשת. שם, מספר גדול של תאים בעלי כושר כיווץ מתאחים יחדיו ליצירת תא יחיד וארוך המכונה סיב שריר. אסופת תאים כאלו מהווה את השריר השלם. ואולם, עד היום מדענים התקשו להבין כיצד תאי גזע מתקדמים לאורך מסלול התמחות זה ומהם הגורמים שמניעים אותם לעבור ממצב למצב.
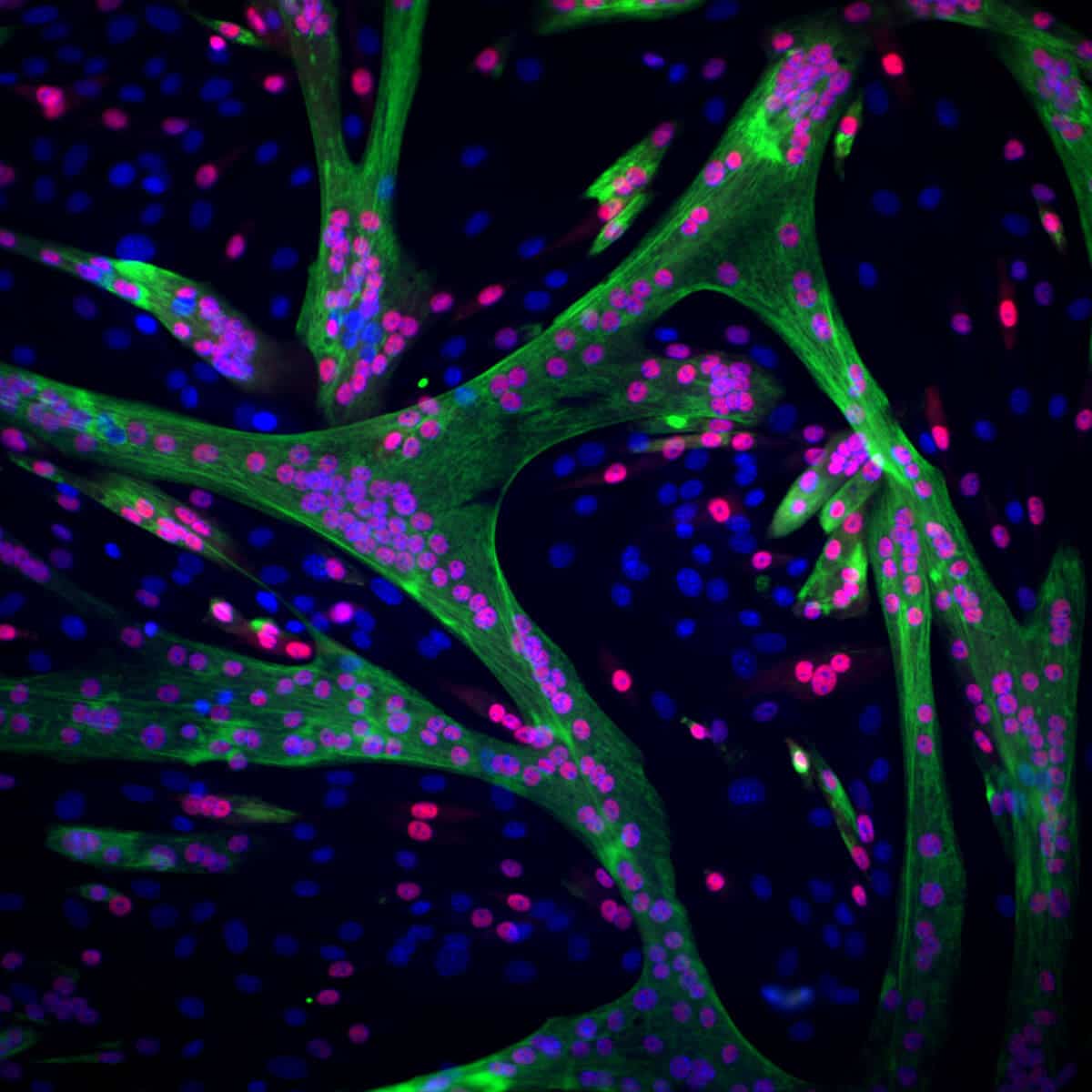
בניסיון להשיב על השאלה, ג’וליה צרפתי ועדי חזק, ממעבדתו של ד”ר אבינעם, תיעדו ב”שידור חי” כיצד נבנה סיב שריר מתאי גזע של עכבר. הן החליטו לעקוב אחר שני שינויים – תנועת התאים במרחב לאורך המסלול והבנייה של סיבים חלבוניים בתוך תאי הגזע, שהינה חיונית ליצירת שריר בוגר המסוגל להתכווץ. כדי לעקוב אחר תנועת התאים סומנו גרעיניהם בצבע פלואורסצנטי, וכדי לעקוב אחרי בניית הסיבים החלבוניים סומן חלבון בשם אקטין שמרכיב אותם. לאורך יממה של התמיינות, הפיקו החוקרות רבבות של קטעי וידאו המתעדים שלב אחר שלב, ברמת התא הבודד, כיצד מאות תאי גזע הופכים לתאי שריר בוגרים ומתאחים לסיב חדש.
לאחר שאספו את שפע המידע הביולוגי, החלו החוקרות מהמכון ותלמידת המחקר עמית שקרצ’י ממעבדתו של ד”ר זריצקי בתהליך למידה משותף שמטרתו הייתה לבנות מודל שיצליח לעקוב אחר התהליך הדינמי. “קבוצות המחקר היו צריכות ללמוד את השפה זו של זו”, מספר ד”ר אבינעם. “הצוות של אסף למד מהו תא שריר ממוין ואיך יודעים שהוא התאחה עם תאים אחרים לסיב שריר, ואילו הצוות שלי למד את עקרונות למידת המכונה וכיצד לנתח מידע שנאסף מרצף תצפיות בזמנים שונים. אחר כך, היינו צריכים להבין יחד כיצד לתרגם את התהליך הביולוגי למודל חישובי שיעקוב אחר התקדמותו”.
ישנם אתגרים רבים בבניית מודל ממוחשב שביכולתו לעקוב אחר תהליך ביולוגי דינמי. “ראשית צריך להחליט על אילו מרווחי זמן מסתכלים ומשווים ביניהם”, מתאר ד”ר זריצקי. “אחר כך מחליטים האם לייצר מודל למידה מונחית המתחשב רק בנתונים מסוימים או לאפשר למודל לתת משקל לכלל הנתונים. אנחנו החלטנו על מודל מונחה שעוקב אחר מסלול התנועה של התאים ועוצמת הצבע הפלואורסצנטי המתקבל מסיבי האקטין שבהם. המודל בחן גם נגזרות של המידע הזה, כמו שינויים בקצב התנועה של התאים וכיצד משתנה מבנה סיבי האקטין בתא לאורך זמן”.
המדענים זיהו כי עם התקדמות תהליך ההתמיינות, התנועתיות של התאים פחתה ועוצמת האות המתקבל מסיבי האקטין שבהם עלתה. מודל למידת המכונה אומן להבחין כך בין תאי גזע ותאי שריר בוגרים ויצר מדד כמותי שעוקב בזמן אמת ונותן ציון מספרי לכל תא בדגימה בהתאם למידת התקדמותו בתהליך. כשבחנו את המודל על ניסויים שלא אומן עליהם, הם זיהו כי הציון שקיבלו מרבית תאי הגזע עלה באופן הדרגתי במהלך ההתמיינות והפסיק לעלות בסיומה. “למדנו מהמודל שתהליך ההתמיינות הוא הדרגתי ומבוזר – התאים לא מתקדמים יחד בשלבים, אלא יש להם דפוסי התקדמות שונים”, אומר ד”ר אבינעם. “זו הייתה תוצאה בלתי צפויה, שיערנו שתהיה התנהגות קולקטיבית”.
“היכולת לעקוב בזמן אמת ובאופן רציף אחר השתנות תאים, עשויה לאפשר בעתיד לנטר התקדמות מחלות באופן חסר תקדים. כיום למשל עוקבים אחר גידולים סרטניים באמצעות נטילת דגימה (ביופסיה) – הליך קפוא בזמן שאינו מאפשר קבלת מידע שוטף על תהליך ביולוגי דינמי”, אומר ד”ר זריצקי. “כמו כן, בעידן שבו הבשר המתורבת עולה על השולחן, מודלים מסוג זה יכולים ללמד אותנו מדוע תאים שהגיעו מפרטים מסוימים מתרבים ומתמיינים באופן יעיל ומהיר יותר וכך לשפר את שיטות הייצור”.
עצור בטרם תתאחה
המודל חשף אמנם כי תאים השלימו את התבגרותם בזמנים שונים, אך משסיימו להתמיין חלף פרק זמן מוגדר של כשלוש שעות בממוצע עד שהתאחו לסיב שרירי. ממצא זה העלה את ההשערה שקיימת נקודת בקרה, שבמסגרתה מוודא התא כי אכן הגיע לפרקו, ורק אז מניע את תהליך האיחוי.
מחקרי עבר העלו את הסברה שהאנזים p38 מווסת את בניית השרירים: כאשר מעכבים את פעילותו, תאים אינם מתאחים לסיב שריר חדש. עם זאת, לא היה ידוע באיזו נקודה במסע ההתבגרות נתקעים תאי הגזע ומדוע. כשהריצו את המודל הממוחשב ראו החוקרים שתאים שבהם עוכב האנזים קיבלו ציון מספרי שהלך ועלה. במלים אחרות, גם בהיעדרו של האנזים הם הצליחו להשלים את תהליך ההתמיינות שלהם, אך לא המשיכו לשלב האיחוי. לפיכך, הסיקו המדענים שנקודת הבקרה מגיעה בתום תהליך ההתמיינות ולפני שלב האיחוי.
המודל הציע גם הסבר אפשרי לפעולת האנזים: הוא הראה שבתאים שבהם פעולתו עוכבה, השתנה האופן שבו מתעצבים סיבי האקטין במהלך ההתמיינות. בדיקה בפועל של רמות החלבונים המתבטאים בתאים שעוכבו איששה את תחזית המודל: המדענים זיהו כי התאים מבטאים רמות גבוהות של חלבונים המעורבים בסידור סיבי אקטין בשלד התא, שלב חשוב בהתמיינות ובהכנה לאיחוי, לצד רמות נמוכות של חלבונים המעורבים ביצירת סיבי השריר הבוגרים ובכיווץ השריר. “התאים למעשה נתקעים במצב של ‘מוכנות לאיחוי'”, מסביר ד”ר אבינעם, “לכן עם החזרת האנזים לפעולה הם יכולים לשוב ולהתאחות. זהו למעשה צומת בקרה מרכזי שבו השריר מוודא שהתאים השלימו את כל ההכנות הנדרשות לפני שיתאחו לסיב שריר חדש. מעבר לבניית שרירים, תגלית זו מעידה גם על היכולת של מודלים ממוחשבים לזהות צמתי בקרה חשובים בתהליכים ביולוגיים דינמיים”.
במחקר השתתפו גם רעות מעלם מאוניברסיטת בן-גוריון בנגב; קארינה הוק מהמחלקה למדעים ביומלקולריים במכון; וד”ר תמר זיו מהטכניון.
עוד בנושא באתר הידען:
