מידע חדש על חלבוני איתות, המכונים חלבוני G עשוי להתברר כחשוב ביותר במאבק כנגד מחלות כליקויים לבביים וניווני עצבים וסרטן
מידע חדש על חלבוני איתות, המכונים חלבוני G (הערך בוויקיפדיה), עשוי להתברר כחשוב ביותר במאבק כנגד מחלות כליקויים לבביים וניווני עצבים וסרטן. מזה עשורים רבים מדענים תוהים "כיצד חלבוני איתות מובלים ומאורגנים במתחמים מוגדרים בתא?". חוקרים בתחומי הננו-מדע מספקים עתה מידע חדש לשם פיתרון סוגיה זו.
"אנו מתחילים כעת להבין כיצד חלבוני איתות מזוהים ומועברים לאזורים מוגדרים בתא ולקבל הבנה ברורה יותר בדבר המנגנון של תהליכים תאיים חשובים כגון איתות תאי וצמיחה. ידע חשוב זה יוכל לשמש בעתיד להבנת מחלות כגון דיכאון ואלצהיימר וריפוין", מסביר הפרופסור Dimitrios Stamou, אשר הוביל את המחקר הזה.
תאים בגוף תלויים לחלוטין ביכולתם הבררנית להעביר ולתחום חלבונים לאזורים מוגדרים. השערות קודמות, שהציעו כי חלבונים נעים בתאים ע"י הכרה של ננו-רכיבים בקרומית הסובבת אותם, המכונים גם אסופת שומן, נמצאות עתה במחלוקת עזה. אולם, חוקרים מהמרכז לננו-מדע באוניברסיטת קופנהגן גילו מנגנון בלתי-מוכר המבוסס על צורת קרומית התא ואשר פורסם בכתב-העת המדעי Nature Chemical Biology.
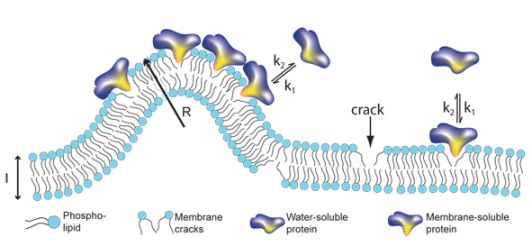
בדומה לכל החומרים האחרים, קרומיות תאים תתבקענה כתוצאה מכיפופן. אולם, לקרומית התא ישנה תכונה ייחודית: כיפופה יותר ויותר לא יוצר בקעים גדולים יותר אלא כמות גבוהה יותר של בקעים באותו הגודל. מסתבר, כי מספר חלבונים חשובים "מעדיפים" להיקשר לבקעים אלו וכך החלקים הכפופים של הקרומית הופכים למקום "מפגש" טוב עבורם לחבירה יחדיו לשם ביצוע משימות מורכבות הדורשות פעילות משותפת של חלבונים שונים רבים.
"הופתענו לגלות שמספר הבקעים בקרומית הוא זה הקובע את מספר החלבונים שייקשרו. עד עתה, חוקרים בתחום זה סברו כי הגורם המכריע היה היכולת של החלבונים ונטיתם להיקשר לקרומית, מושג המכונה זיקה (affinity). הממצאים שלנו סותרים השערה זו," מציין אחד מהחוקרים.
החלבונים נעים בתוככי התאים בתוך שלפוחיות קטנות – מעין בועיות סבון שבדומה לתאים עצמם תחומות ע"י מעטפת. החוקרים הכינו במעבדה שלפוחיות בעלות גדלים משתנים ובדקו כמה סוגים שונים של חלבונים יוכלו להיקשר לקרומיות שלהן. הם גילו כי ככל שגודל השלפוחית קטן יותר וככל שהמעטפת כפופה יותר, כך מספר הבקעים גבוה יותר וכתוצאה מכך יותר חלבונים, יחסית ליחידת שטח, יכולים להיקשר.
"ברגע שהבנו כי הגורם המכריע ביותר בתצפיות שלנו היה מבנה הקרומית חשבנו מייד שאולי מצאנו מנגנון כללי שיוכל להתאים גם לסוגים אחרים של חלבונים מלבד אלו שחקרנו. בעקבות כך, חקרנו בשלב הבא חלבוני G שהינם חלבוני איתות חשובים הקשורים לקרומית התא בדרכים שונות ע"י "עוגן" ליפידי. הממצאים שלנו אימתו כי המנגנון אכן כללי," מסביר אחד מהחוקרים.
"גילוי החשיבות המרובה לאין ערוך של מבנה הקרומית לשם תיחומם של מאות חלבוני איתות חשובים, הינו חיוני להבנתנו את גודש התהליכים הביולוגיים, שרבים מתוכם קשורים ישירות למחלות נפוצות," מדגיש החוקר הראשי.
