"אריזות סיליקון", לשחרור מקומי של תרופות אנטי-סרטניות, מתפרקות באופן שונה ברקמת הגידול, ועובדה זו משפיעה על יעילותן הקלינית. מחקר שנערך בטכניון, ב-MIT ובהארוורד שופך אור על תהליך ההתפרקות האמור וסולל דרך לשיפור הטיפול בגידולים אלה
"אריזות סיליקון", לשחרור מקומי של תרופות אנטי-סרטניות, מתפרקות באופן שונה ברקמת הגידול, ועובדה זו משפיעה על יעילותן הקלינית. מחקר שנערך בטכניון, ב-MIT ובהארוורד שופך אור על תהליך ההתפרקות האמור וסולל דרך לשיפור הטיפול בגידולים אלה.
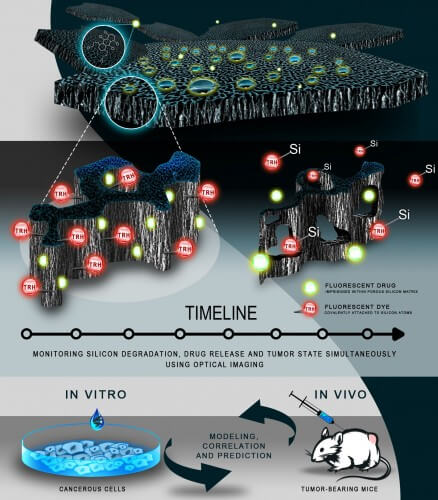
מאמר חדש בכתב העת היוקרתי Nature Communications חושף כי סיליקון ננו-נקבובי, המיועד לשחרור מבוקר של תרופות כימותרפיות, מתנהג בצורה שונה בסביבת גידול סרטני בהשוואה לרקמה בריאה. מדובר במחקר משותף הנערך בטכניון, ב-MIT ובבית הספר לרפואה בהארוורד. פרופסור אסתי סגל, העומדת בראש הקבוצה הטכניונית שהובילה את המחקר, מסבירה כי ״אנו מראים לראשונה כי ביו-חומרים בכלל, וסיליקון נקבובי בפרט, מתנהגים בצורה שונה כאשר הם מוזרקים (או מושתלים) בסביבת רקמה סרטנית. בשנים האחרונות הצלחנו להנדס סיליקון כך שישמש כ'אריזה' המובילה תרופות אנטי-סרטניות ומשחררת אותן בצורה מבוקרת, וכעת התמקדנו במנגנון התפרקותו של הסיליקון ברקמת היעד הסרטנית."
סיליקון נקבובי (Porous Silicon) הוא שם כולל למשפחה של חומרים מבוססי-סיליקון המכילים חורים ננו-מטריים. חומר זה ידוע כיום כ'אריזה' (פלטפורמה) יעילה להובלת תרופות, וזאת בשל תכונותיו הייחודיות: שטח פנים גדול (הזָמין להעמסת התרופה), תאימוּת ביולוגית (biocompatbility) והתפרקות בטוחה ולא רעילה בגוף (bio-degradability). בשנים האחרונות פיתחו פרופסור סגל והדוקטורנטית עדי צור בלטר 'אריזות' כאלה להובלת תרופות אנטי-סרטניות. באמצעות תכנון מדויק של קוטר הנקבוביות בסיליקון, ושליטה בכימיית פני-השטח שלהן, השיגה הקבוצה תכונות אופטימליות להסעת תרופות בתוך הגוף ולשחרורן באתר המטרה.
אחד הממצאים החשובים במחקר זה, שבו נבחנה הפלטפורמה האמורה ברקמות סרטן שד, קשור בתהליך הפירוק של הסיליקון. המחקר הוכיח שהגידול הסרטני משחרר חומרים הגורמים לחימצון מואץ של אותה 'אריזה' ומפרק אותה בקצב מהיר יותר בהשוואה לניסויים שנערכו במעבדה. המאמר שופך אור על תהליך פירוק הסיליקון בסביבת הגידול, ומאפשר תכנון מוקדם ומושכל של מבנה הסיליקון להשגת שחרור מבוקר של התרופה באתר המטרה.
על פרופסור אסתי סגל:
פרופסור סגל השלימה את שלושת התארים שלה בפקולטה להנדסה כימית בטכניון. בשנת 2007, לאחר פוסט-דוקטורט בפקולטה לכימיה וביוכימיה באוניברסיטת קליפורניה בסן דייגו (UCSD), היא הצטרפה לפקולטה להנדסת ביו-טכנולוגיה ומזון בטכניון. כיום היא עומדת בראש המעבדה לננו-חומרים פונקציונליים בפקולטה, ובשנה האחרונה זכתה בפרס הנרי טאוב להצטיינות במחקר אקדמי ובפרס ינאי למצוינות בחינוך אקדמי.
שמו המלא של המאמר:
Mechanism of Erosion of Nanostructured Porous Silicon Drug Carriers in Neoplastic Tissues

11 תגובות
רבות נאמר למשל על יכולתו של גידול לרמות את מערכת-החיסון.לא?
כן מאיה אני די מסכים עם דבריך.
כוונתי ביפתח עמידות –
או שיצליח להרוס את הקופסית וישבש את הריפוי או יפתח עמידות לתרופה(זה מה שאני סובר).
safkan
אינני בטוחה מה אני אמורה לעשות עם תגובה שאומרת שאין לך עניין להמשיך לדון בנושא, ובכל זאת אגיב קצת.
השינוי אותו עובר התא הסרטני ב"הסתגלותו" לכימותרפיה זהה לשינוי אותו עובר תא חיידק בהסתגלותו לאנטיביוטיקה – התא עובר מוטציות (גם תאים סרטניים וגם תאי חיידקים ידועיםלשמצה ביכולת הזו) ואחת המוטציות פוגעת בדיוק בחלבון שהכניס את התרופה לתא או בדיוק בחלבון שעיבד את התרופה בדרך שהזיקה לתא וכך התא לומד לחיות ולשגשג היטב גם בתנאים אלו. כלשאר התאים (אלו שלא רכשו את המוטציה הזו) מתים, כמובן, כי התרופה הורגת אותם, וכך נותר האחוז הקטן שרכש את המוטציה אשר כעת מהווה את כלל האוכלוסיה. בדיקות גנטיות ובדיקות ביטוי חלבונים יוכיחו כי זה מה שקרה (ואפשר אפילו לדעת איזה חלבון ספציפי עבר את המוטציה שאיפשרה את ההסתגלות הזו). והרי לנו ברירה טבעית בלייב. אם אתה לא רוצה לקרוא לזה אבולוציה אתה לא חייב, כך כל השאר קוראים לזה, אבל המנגנון במהותו זהה לזה של מיקרואורגניזם.
הרגשת בטן זה נחמד (ברצינות) והרבה פעמים זו פתיחה טובה להתחלה של מחקר מדעי מעמיק בנושא, אבל היא כמובן לא באה להחליף מחקר מדעי.
בנוגע לנושא המאמר הספציפי הזה, למרות שתכננתי לא מצאתי את הזמן עדין לקרוא את המאמר המדובר ולכן אינני יכולה בינתיים להביע דעה. להבנתי, לפי מה שקראתי כאן באתר, הקפסולה שמחזיקה את התרופה מתפרקת בקצב שונה מהצפוי באזור הגידול הסרטני ומה שהקבוצה עשתה היה למדוד את הקצב הזה ואף לתקן את הקפסולה כך שתשחרר את החומרים באופן יעיל באזור הגידול. הקפסולה אכן לא אמורה כלל להגיב עם תאי הגוף, כולל תאי הסרטן ולכן אני בספק שהם "יפתחו עמידות" כלפיה (למרות שמי יודע) ואני מניחה שמה שיגאל התכוון אליו הוא אכן עמידות לתרופה עצמה, למרות שאינני יודעת באמת למה הוא התכוון.
safkan
היום נתקלתי במקרה במאמר על טיפול בסרטן. אינני מכיר את הנושא, אני מביא דברים בשם אומרם. נא לא להרוג את השליח.
http://www.futurity.org/olive-oil-cancer-859862/
למאיה
ראשית. תגובתי הושהתה כי הייתי טרוד. לא רציתי לשלוח את תגובתי בעניינך לפני שאשלח תגובות בעניין הכור הגרעיני איקאט של אנדראה רוסי. עניינו של כור איקאט חשוב מכדי שתגובותי עליו תידחנה.
לגופו של עניין.
אני מתנצל על הטעות ועל ההטעיה מצידי. הייתי צריך לספור עד 10 לפני ששלחתי תגובה (בענין הקפסולות הזעירות להזלפה מקומית של חומרי כימותרפיה). כנראה הייתי עייף מדי וקצר רוח, לכן תגובתי היתה מוטעית.
בדרך כלל אני לא שולח מייד תגובה אם אינני בטוח בה, אני שומר אותה על הטבלט כדי לחשוב פעם נוספת. פישלתי הפעם.
על עובדות (באשר לשינוי בהתנגדות של הרקמה הסרטנית לטיפול ביוכימי ממושך) – אני סומך עליך כי עובדות אינן עניין לוויכוח. למדתי ממך משהו. "טיפול ממושך" כאן כולל "טיפול חוזר".
אני לא סומך עליך באופן עיוור בנוגע לטענה שלך שההתנגדות של הגידול הסרטני לטיפול ביוכימי נעשה בגלל שהגידול הסרטני עובר שינוי אבולוציוני. שינוי אבולוציוני נראה לי "קלף ג'וקר" ששולפים אותו בתור "הסבר מרשים" כאשר יש תהליך של השתנות פעולה שאין לו "הסבר ברור אחר".
עולים בדעתי תהליכים אחרים (לא אבולוציונים) שעשויים לחולל שינוי נירכש בהתנהגות ריקמה סרטנית (תוך כדי תהליך כימותרפי ממושך). לא רק זאת – הרגשת הבטן שלי _שרוב_ ההתנגדויות של הרקמה הסרטנית אינן באמצעות שינוי אבולוציוני. לא אכנס להסבר למה יש לי הרגשת בטן; יש לי נימוקים טובים (לדעתי) אבל אין לי רצון בהמשך הוויכוח.
הערה:
הפתרון שאותו מחפשים החוקרים אינו החלפת תרופות אלא החלפת _שיטת הזלפת תרופות_ (שינוי שיטת הזלפה על ידי שינויים בקפסולות הזעירות שמזליפות את התרופות). החומר ממנו הקפסולות עשויות אינו (כנראה) חומר תרופתי -לפיכך יש סיכוי טוב לשנות את הקפסולות (באופן שהריקמה הסרטנית לא תוכל לתקוף אותן).
אין לי עניין נוסף לדון בנושא. זה עלול לדרוש ממני זמן ממושך מדי.
מאיה שלום תגובה יפה ומעשירה אהבתי תודה
למאיה
תגובה ארוכה שלי תינתן בעוד זמן (לא מתחייב כמה זמן). לאחר הגהות נידרשות.
ספקן שלום,
אין לי כוח לפתוח את המחשב שלי ואם אני משנה את הניק על המחשב הזה הוא לא נותן לי לשלוח הודעה, אז זאת מאיה, שלום.
אני חייבת לשאול: מה גורם לך לענות בכזה ביטחון לאנשים כאשר מדובר בנושאים שברור שאין לך מושג בהם?
"סרטן אינו מיקרוארגניזם שמסוגל להתפתח באופן אבולוציוני" – אתה רציני? מה הופך לדעתך מיקרואורגניזמים לכ"כ ייחודיים שהם יכולים להתפתח באופן אבולוציוני? רמז: כלום. תא סרטני הוא אומנם תא הומני (במקרה של סרטן באדם) אבל הוא עדין תא שמתרבה, עובר מוטציות ונמצא תחת סלקציה. מסקנה – הוא נתון לתהליך אבולוציוני, כמו כל אורגניזם ביולוגי אחר.
"לכן היכולת שלו לפתח התנגדות נמוכה מאוד אם בכלל". שוב אני אשאל, אתה רציני? זה כבר לא קשור להבנה מעמיקה בתחום, כל מה שצריך זה איזה מכר או שניים חולי סרטן (ולצערינו, כאלה לא קשה למצוא) שהסרטן שלו פיתוח עמידות לכימותרפיה. מה אתה חושב שזה אומר? המנגנון, אגב, שבו התאים הסרטניים מפתחים את העמידות לתרופות זהה למנגנון שבו חיידקים מפתחים עמידות לאנטיביוטיקה. אתה יודע איך קוראים למנגנון הזה במילה אחת? אבולוציה.
אני באמת מוצאת את זה מטריד כשאנשים עונים בביטחון כזה על נושאים שהם בכלל לא מבינים בהם. הסיבה לכך היא שיש אנשים שנכנסים לאתר הזה כדי ללמוד ותשובה מלאת ביטחון נוטה לגרום לאנשים לחשוב שיש דברים בגו. אין עם זה בעיה כשאתה יודע על מה אתה מדבר, אבל כשזה לא המצב, זה בעייתי. זו הסיבה שאני, באופן אישי, נכנסת לדיונים או של נושאים שקשורים ישירות לנושאי המחקר שלי או תחומים קרובים מספיק שברור לי שאני מתמצאת בהם היטב, או של נושאים שסתם מעניינים אותי ואני לא מבינה בהם כ"כ, אבל אז אני מוודאת שכל מה שאני אומרת נגמר בסימן שאלה. כי אני לא יודעת. זה בסדר להגיד שלא יודעים. לא חייבים להיות מומחים בכל דבר. אבל לבלבל כך אנשים זה חסר אחריות.
יגאל
סרטן אינו מיקרוארגניזם שמסוגל להתפתח באופן אבולוציוני, לכן היכולת שלו לפתח התנגדות נמוכה מאוד אם בכלל. סרטן זה תא "רגיל" (של החיה בה הוא מתפתח) שהשתבש אצלו מנגנון של "השמדה עצמית" ולכן הוא מתרבה באופן פרוע , ההתרבות הפרועה היא על חשבון הרקמות הבריאות שלידו).
למעשה רוב התרופות לחיסול סרטן משתמשות בכך שהתכונות של תא סרטני שונות במקצת מתכונות תא נורמלי. התרופות מבצעות תקיפה סלקטיבית של תאים תוך ניצול השוני בתכונות שהזכרתי: התרופות בנויות באופן שישמידו בעיקר תאים סרטניים וישמידו כמה שפחות תאים בריאים. לא תמיד הסלקציה הזו עובדת בצורה מוצלחת. אז הטכניקה החדשה מנסה עוד שיטה לתקיפה סלקטיבית, אולי תצליח ואולי לא.
עד שהגידול יפתח עמידות.