הטכנולוגיה, המבוססת על פלטפורמת Nano-Ghosts, מאפשרת לצמצם את מינון התרופה פי מיליון בלי לפגוע ביעילותה
חוקרים בפקולטה להנדסת ביוטכנולוגיה ומזון בטכניון פיתחו טכנולוגיה המעכבת התפתחות מלנומה בשימוש במיליונית מהחומר הפעיל. את המחקר שהתפרסם ב- Advanced Functional Materials הובילו דיקנית הפקולטה פרופ' מרסל מחלוף והדוקטורנט ליאור לוי.
אימונותרפיה בפעולה. הפיתוח הנוכחי הוא פריצת דרך משמעותית בשדה האימונותרפיה – גישה רפואית חדשנית שהפכה לאחת המגמות המבטיחות ברפואת סרטן. גישה זו מתבססת על יכולתה של מערכת החיסון הטבעית להשמיד תאים סרטניים. מערכת זו יודעת לעשות זאת באופן ספציפי ומדויק יותר מתרופות אנטי-סרטניות מלאכותיות. עם זאת, מאחר שהגידול הסרטני הטרוגני וחמקמק, הוא יודע לפעמים לשטות במערכת החיסון – וכאן נכנס המדע לתמונה, עם כלים חדשים המסייעים למערכת החיסון להתמודד עם אתגר זה.
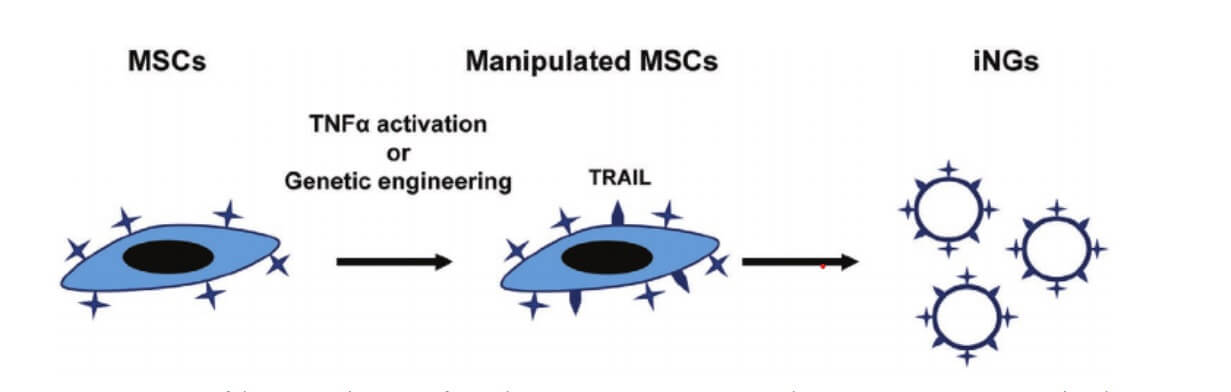
חלבוןTRAIL . בלב הפיתוח החדש עומד חלבון בשם TRAIL הקיים במערכת החיסון הטבעית ויודע לחולל אפופטוזיס (התאבדות מכוונת) של תאי סרטן. במילים אחרות, הוא פקטור-ממית-גידול (TNF). יתרון נוסף: הוא סלקטיבי, כלומר פוגע בתאי סרטן בלבד – תכונה רצויה מאוד בטיפולים אנטי-סרטניים. יישומו של TRAIL באימונותרפיה נתקל עד כה באתגרים טכניים שונים ובהם קליטתו של החלבון בגוף, תנועתו (פרמקו-קנטיקה) והעובדה שאינו שורד זמן רב. המחקר הנוכחי נותן מענה לבעיות אלה.
טכנולוגיית Nano-Ghosts. הפיתוח המוצג במאמרם של חוקרי הטכניון מבוסס על טכנולוגיה מקורית שפיתחה פרופ' מחלוף בשנות עבודתה בטכניון: פלטפורמת Nano-Ghosts. הפלטפורמה מיוצרת על ידי ריקון של תאים ביולוגיים ספציפיים (תאי גזע מזנכימליים) באופן המשאיר רק את קרום התא. לתוך קרום זה אפשר להכניס כל תרופה שהיא ולשגר אותה בהזרקה ישירות למערכת הדם. מאחר שמערכת החיסון הטבעית מתייחסת לתאים אלה כאל תאים טבעיים, היא משגרת אותם למקום הנגוע. בדרכם לשם הם אינם משחררים את התרופה ולכן אינם פוגעים ברקמות הבריאות. רק בהגיעם לרקמה הממאירה, שאותה הם יודעים לזהות, הם מתפרקים ומחדירים את התרופה לתאי הגידול.
אינטגרציה. המחקר הנוכחי משלב את שלושת הסעיפים הקודמים: הקונספט האימונותרפי, חלבון TRAIL וטכנולוגיית Nano-Ghosts שפיתחה פרופ' מחלוף. התוצאה: פלטפורמת-שיגור-תרופות שעל שכבתה החיצונית נמצא החלבון הפעיל, דבר המאפשר להפחית את מינון התרופה פי מיליון תוך שמירה על אותה השפעה רפואית.
לדברי פרופ' מחלוף, "השילוב הזה הופך את פלטפורמת Nano-Ghosts מ'מונית' המסיעה את התרופה אל היעד ל'טנק' של ממש המשתתף בלחימה. הפלטפורמה המשולבת הזאת מביאה את התרופה לגידול הסרטני, וכאמור מאפשרת להפחית משמעותית את מינון התרופה ועדיין לעשות את העבודה. הראינו גם שהשיטה שלנו אינה גורמת לפגיעה בתאים בריאים."
הטכנולוגיה הודגמה על תאים במעבדה וכן על תאי סרטן אנושיים בעכבר. החוקרים מעריכים שהאסטרטגיה החדשה, שהודגמה במחקרם במודל של סרטן מלנומה, תהיה יעילה גם בסוגי סרטן אחרים.
עוד בנושא באתר הידען:

תגובה אחת
השאלה מתי ואם, אמת חשתמשו בזה. היו בערב הרבה "פריצות דרך" שאנחנו לא רואים שמשתמשים בהם