בעוד מדענים רבים מחפשים את התשובה בתאים הסרטניים עצמם, באמצעות השוואה בין אלה שמגיבים לכימותרפיה לבין אלה שעמידים אליה, ד"ר רביד שטראוסמן ועמיתיו חשבו שהמפתח להבנת הבעיה נעוץ במקום אחר – בתיפקודם של תאי הגוף הבריאים.

"תמיד ראיתי בעצמי רופא", אומר ד"ר רביד שטראוסמן, בעל תואר כפול MD/PhD, שהצטרף באחרונה למחלקה לביולוגיה מולקולרית של התא במכון. "אך בתקופה שבה סיימתי את הלימודים הלכתי ונמשכתי למחקר. ועדיין, גם כשאני עוסק במחקר במעבדה, המחשבה שלי נתונה לחולה הזקוק לטיפול". לחולים עליהם חושב ד"ר שטראוסמן יש כיום מעט מאוד תקווה לריפוי, מכיוון שסוגי הסרטן מהם הם סובלים עמידים לכימותרפיה. מדוע גידולים מסוימים מצטמקים בתחילת הטיפול הכימי, אולם מסרבים להיעלם לחלוטין, ואילו גידולים אחרים משלימים את התהליך עד סופו, אך חוזרים בגירסה עמידה מאוחר יותר? מדוע מתברר שטיפול אשר משמיד לחלוטין תאים סרטניים במבחנה – יעיל הרבה פחות בגוף האנושי?
ד"ר שטראוסמן החל לחקור את תופעת העמידות של סוגים שונים של סרטן במהלך מחקרו הבתר-דוקטוריאלי במכון "ברוד" של הרווארד ושל המכון הטכנולוגי של מסצ'וסטס. במעבדתו של פרופ' טוד גולוב, המדען הראשי של מכון ברוד וראש התוכנית לחקר הסרטן, הוא חקר שאלה זו מזווית לא שגרתית. בעוד מדענים רבים מחפשים את התשובה בתאים הסרטניים עצמם, באמצעות השוואה בין אלה שמגיבים לכימותרפיה לבין אלה שעמידים אליה, ד"ר שטראוסמן ועמיתיו חשבו שהמפתח להבנת הבעיה נעוץ במקום אחר – בתיפקודם של תאי הגוף הבריאים.
הסיבה לכך, הוא מסביר, היא שתאים סרטניים, כמו כל תאי הגוף, הם חלק ממערכת גדולה, מתוחכמת ומקושרת, בה מופעלים מנגנונים שונים לעזרה ולתמיכה הדדית. לתאים בריאים יש יכולת להזעיק עזרה מחלקים מרוחקים של הגוף, כמו לשד העצם, כאשר הם נפגעים או מצויים תחת התקפה. המדענים חשדו, כי באופן דומה, התאים הסרטניים מזעיקים עזרה כאשר הם מצויים תחת מתקפה כימותרפית.
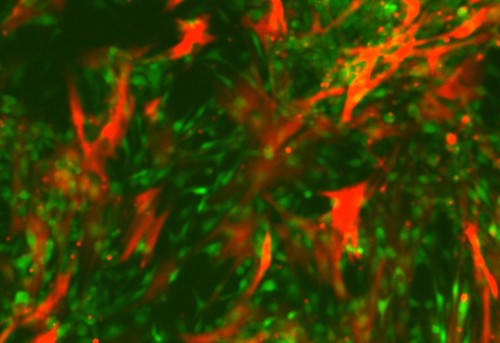
על מנת לבדוק השערה זו גידלו החוקרים סוגים שונים של תאים סרטניים, ובחנו את רגישותם לתרופות כימותרפיות. ואכן, הם גילו כי גידולים הנבדקים במבחנה ומכילים אך ורק תאים סרטניים, רגישים ביותר לסוגים שונים של כימותרפיה. אולם, כאשר הוסיפו למבחנה סוגים שונים של תאים נורמליים, המצויים באופן רגיל בסביבת הגידול, הרגישות צנחה – ובמקרים מסוימים אף נעלמה לחלוטין. לאחר שמצאו כי תופעה זו מתרחשת בסוגים רבים של סרטן, ובסוגים רבים של תרופות כימותרפיות, החליט הצוות להתמקד במלנומה – סוג הסרטן האחראי לרוב מקרי המוות מסרטן עור. הם גילו חלבון המופרש מתאים בריאים מסוימים אשר מצויים בגידול, ומגן על תאי המלנומה מפני אחת התרופות הכימותרפיות המתקדמות ביותר המשמשות כיום לטיפול במחלה זו. החלבון, שהוא גורם גידול המשפיע על תאי כבד (HGF – hepatocyte growth factor), ממלא תפקידים נוספים, בהם החלמה של פצעים.
בהמשך חיפשו המדענים עדויות לפעילותו של החלבון בדוגמאות גידול שנלקחו מחולי מלנומה. או אז הראו התוצאות, שכאשר תאים בסביבתו הקרובה של הגידול ייצרו כמויות גדולות של HGF, הגידול הראה עמידות לכימותרפיה, ואילו חולים שבהם התאים לא ייצרו HGF הפגינו תגובה טובה הרבה יותר לטיפול. מכך עולה כי HGF, כשלעצמו, מסייע להישרדות התאים הסרטניים בתגובה לכימותרפיה. בהתבסס על ממצאים אלה מתוכננים להתקיים בקרוב ניסויים קליניים שבמסגרתם יינתנו מעכבי HGF לחולי מלנומה, ביחד עם הטיפול הכימותרפי הסטנדרטי.
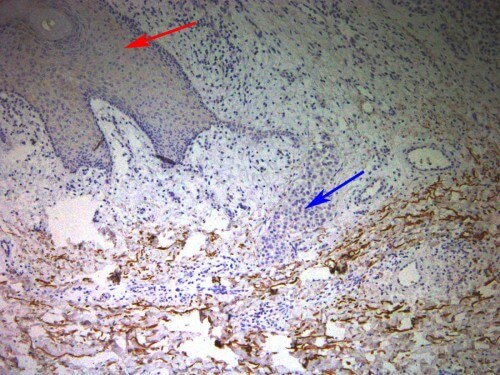
"גידול רגיל מכיל סוגים שונים של תאים – סרטניים ונורמליים כאחד", אומר ד"ר שטראוסמן. "מיגוון התאים הנורמליים המצויים בסביבתו הקרובה של הגידול עשוי לייצר עשרות חומרים שונים, אשר מסייעים לגידול לשרוד את הטיפול הכימותרפי. אנחנו מצויים בתחילתה של הדרך בניסיון להבין מה הם חומרים אלה וכיצד הם מסייעים לעמידות".
אישי
רביד שטראוסמן נולד ברמת-גן, ושירת כקצין בחיל האוויר. הוא סיים מסלול MD/PhD בבית הספר לרפואה של האוניברסיטה העברית בירושלים, ובמעבדתה של פרופ' שושנה רביד. לאחר שנה שבמהלכה עבד בבית-החולים "בילינסון" ביצע מחקר בתר-דוקטוריאלי במעבדתו של פרופ' חיים סידר באוניברסיטה העברית בירושלים. לאחר מכן המשיך למחקר בתר-דוקטוריאלי נוסף במעבדתו של פרופ' טוד גולוב במכון ברוד. "רביד, סידר וגולוב היו מנטורים במלוא מובן המלה", הוא אומר. "זו הייתה זכות גדולה לעבוד לצדם".
רביד נשוי לשרון, אנדוקרינולוגית של ילדים, ואב לארבעה ילדים בגילים שמ-11 עד שנתיים. בזמנו הפנוי הוא נוהג לשחק טניס.

2 תגובות
דרך מחשבה הגיונית ומעוררת תיקווה עבור החולים. צריך רק לשאול איך לא חשבו על זה קודם.
יהודה