אחת החידות של מערכת החיסון היא כיצד מפתחת המערכת נוגדנים לחיידקים ולנגיפים, וכיצד רכיבי הנוגדנים הללו נשמרים במעין ספריה בגֶנום. עבודת דוקטורט חדשה שופכת אור על הנושא
החיים הם מאבק מתמשך באיומים, ומערכת החיסון אמורה להקנות לנו מענה עליהם.
מערכת החיסון היא מערכת מאוד מורכבת, אומרת ד"ר מיכל ברק מהמעבדה לביולוגיה חישובית בפקולטה למדעי החיים ע"ש מינה ואבררד גודמן, שעסקה בנושא זה בעבודת הדוקטורט שלה בהנחייתה של פרופ' רמית מר. אחת התכונות של תאי מערכת החיסון האחראים על ייצור הנוגדנים היא האבולוציה המהירה שהם עוברים כל העת בתגובה לאיומים חדשים על הגוף, בכך שהם מפתחים מוטציות שיתאימו יותר לאנטיגנים, שהם סמנים המבצבצים מ פניהם של נגיפים או חיידקים, ומעוררים יצירת נוגדנים לפולשים אלה. ברק פיתחה בעבודתה הדמיה שמנסה לחקות את התהליך של יצירת הנוגדנים. "האימונוגלובולינים (הנוגדנים) שמבטאים תאי B ממלאים תפקיד מרכזי במערכת החיסונית. המטרה של המחקר היתה לבחון את האבולוציה של האימונוגלובולינים ברמת המיקרו (בתוך הפרט) וברמת המאקרו (בהתפתחות של מינים-ביולוגיים). על-ידי שימוש בטכניקות שפיתחנו לחקר אימונוגלובולינים גם למערכת עריכת הרנ"א, קיבלנו תובנות גם על תהליך זה", כותבת ברק בעבודתה.
"המעבדה עוסקת ביישום שיטות מתחום הביולוגיה החישובית לחקר מערכת החיסון", מסבירה ברק. " אנחנו מנסים, בעזרת סימולציות ומודלים מתמטיים, לחזות את ההתנהגות שלה בזמנים נורמליים ובזמנים של מחלות בכלל ומחלות אוטואימוניות בפרט – מצב שבו הגוף תוקף את עצמו."
חיסון טבעי
אפשר להשוות את מערכת הזיהוי של הנוגדנים לשני חלקי תַצרֵף המתחברים זה לזה. ככל שההתאמה גבוהה יותר כך החיבור בין שני החלקים חזק יותר. כל תא בגוף מציג על המעטפתשלו מעין סמן שמשייך אותו לגוף שבו הוא נמצא. חלקים של מערכת החיסון יודעים להתקשר לסמנים אלה וכך לזהות את התא כשייך לגוף. הנוגדן מנסה לזהות צורות חלבוניות שאינן שייכות לגוף ולנטרל את התא או את הנגיף שמציג אותם. הוא עושה זאת על-ידי היצמדות של הנוגדנים לפני התא או הנגיף, פעולה שמנטרלת את הפולש ומסמנת לחלקים אחרים של מערכת החיסון כי נמצא פולש בגוף. עם זאת, ברוב המקרים ההתאמה אינה מדויקת. לכל אדם (ולכל חולייתן אחר) יש אוסף ייחודי לו של סמני נוגדנים עם התפתחות האדם לומדת מערכת החיסון להכיר את החיידקים והנגיפים שעמם היא נפגשת וכך נוצרים הנוגדנים המספקים הגנה יותר ויותר יותר ממוקדת, לוירוס הרלוונטי. מערכת החיסון משיגה זאת באמצעות תהליך שנקרא היפר אבולוציה – אבולוציה מהירה המתרחשת במרכזי נבט הנמצאים בבלוטות הלימפה, בטחול, במעיים ובעוד רקמות.
תאי מערכת החיסון נמצאים ברקמות שונות ואף מסתובבים בגוף, ופוגעים ב כל תא או גורם אחר שאינו מציג את סימני ההיכר של הגוף. הם מפרקים את הפולש לחלקים שאותם הם מציגים על פני קרומית שלהם. אז הם נודדים לבלוטות הלימפה ומציגים את החלבון המייצג את התא או הנגיף שבלעו לתאי מערכת החיסון שנמצאים שם. אם זו הפעם הראשונה שבה נתקלת מערכת החיסון בפולש מסוים זה, אזי יתעוררו תאי ה-B עם הנוגדן המתאים ביותר ויתחילו להילחם בפולש. המערכת תמלא את החוסר בהתאמה מלאה, הגורם לקשירה חלשה יותר של הנוגדנים לפולש, בעזרת קיזוז כמות גדולה יותר של נוגדנים. בשלב זה של הדבקה ראשונית פורצת בגוף המחלה שגורם לה הנגיף או החיידק. אך בכך לא מסתיים התהליך. בתוך בלוטות הלימפה ישנם מרכזי נבט שבתוכם יתפתחו תאי B חדשים מתוך המאגר הקיים של תאי B בגוף. במקביל להתמודדות עם הפולש, ואף בפרק זמן של שבועות לאחר מכן, תאים אלה עוברים אבולוציה מהירה ומנסים, בשיטת ניסוי וטעייה, להגיע קרוב ככל האפשר להתאמה לגורם הזר. לאחר סיומה המוצלח של המלחמה בנגיף או בחיידק, יישארו עותקים של תא B זה במערכת אפילו עשרות שנים ואף לכל החיים וישמשו כתאי זיכרון, וכאשר הפולש יגיע שוב אפשר יהיה להילחם בו בקלות, לרוב מבלי שהאדם ירגיש בכך בכלל.
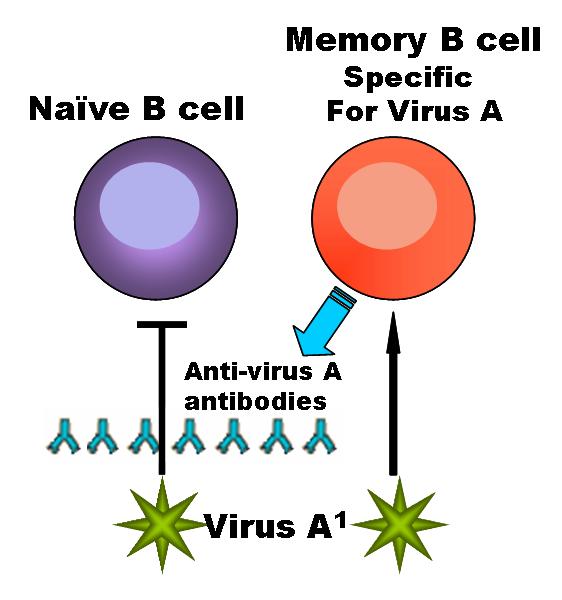
מערכת החיסון, המתאימה עצמה לאיומים, משתמשת במולקולות שמזהות את האנטיגנים כדי לסייע לה להגיב תגובה חיסונית. מבנה הנוגדן מאפשר לו למלא את תפקידו. מולקולות הנוגדן מכילות שני אזורים נפרדים מבחינה תפקודית: האזור המשתנה, המשמש לצורך זיהוי האנטיגנים, והאזור הקבוע לצורך התפקוד של הנוגדן.
מבנה האזור הקבוע (C) קובע אם הנוגדן יישאר מחובר אל קרומית תא B או יופרש ממנו, וכן אחראי אזור זה לקישור עם חלקים אחרים של מערכת החיסון. המבנה של האזור המשתנה (V) מותאם לקשירת אנטיגנים.
עבודתה של ברק נועדה לדמות מרכיבים של תהליך קשירת האנטיגנים. החלק הראשון היה הדמיה של התפתחות תאי ה-B במרכזי הנבט ותהליך ההיפר אבולוציה שהם עוברים כדי להתאים את עצמם יותר ויותר לאנטיגן. הדמיה זו נערכה עם ד"ר גיתית לביא-שחף.
"הדמיה זו שיפרה בהרבה את הבנתנו לגבי התהליך של היפר-אבולוציה במרכזי הנבט", אומרת ברק. "אנחנו מניחים שישנו מרכז נבט שאליו מגיע האנטיגן. כמותו יורדת עם הזמן ככל שיותר תאי B נחשפים אליו ונקשרים למולקולות האנטיגן. פיתחנו משוואות דיפרנציאליות המתארות את השינוי בכמות האנטיגן לאורך הזמן וגם את שיבוט תאי B המתאימים למאבק באנטיגן זה. במהלך התהליך של ההיפר-אבולוציה תאי B מתחלקים בקצב גבוה, ומוטציות נוצרות באזור שאחראי לקידוד החלק המשתנה של הנוגדן בקצב הגדול במספר סדרי גודל מקצב המוטציות הרגיל בדנ"א. התהליך מתחיל כשכמה תאי-B עם נוגדנים שונים מתחרים על ההתקשרות לאנטיגן. ככל שעולה ההתאמה בין הנוגדן לאנטיגן, כך גם מתחזקת עוצמת הקשר ביניהם ויעילותו של הנוגדן. כאשר התאים מתחלקים ומשתנים, נוצרים נוגדנים שונים בתאים החדשים. גם נוגדנים אלו מתחרים על הקישור לנוגדן. במקביל פועל תהליך של ברירה שבו תאים עם קולטנים שעלולים לסכן את הגוף ותאים עם קולטנים שמידת הקשירה שלהם לנוגדן קטנה מורחקים מהתחרות ואף מומתים על מנת שלא יפגעו בגוף עצמו.
אפשר לתאר את התפתחות תאי B בעת תהליך ההיפר אבולוציה בצורת עץ, שמתחיל בתא הראשון שהוא תא B שאינו מתאים אופטימלית לנגיף המסוים, ונמשך באמצעות שינוי הגן לנוגדן בדנ"א של תא ה-B, שנועד להתאימו לאנטיגן בסדרת של מוטציות באזור האחראי לקשירה עם האנטיגן.
מסבירה ברק: "הבעיה של ייצור העץ היא בעיה מסוג בעית NP שלמה (NP COMPLETE) כלומר בעיה קשה מאוד למחשבים, שאי אפשר לפתור אותה בזמן סביר. לפיכך, בחלק הבא של המחקר, כתבנו אלגוריתם שמנסה למצוא את העץ הסביר ביותר מבלי להיכנס לחישובים בלתי אפשריים להרצה בידי מחשב. לאור הניסויים שערכנו נראה שהאלגוריתם מתאר את התוצאות בקירוב די טוב. האלגוריתם משתמש בסדרה של הנחות שמובילות אותו לפסול כבר בשלב ראשוני את העצים הלא סבירים ביולוגית, כשהעיקרית שבהן היא שגודל העץ הוא מינימלי – זאת אומרת שמספר מינימלי של מוטציות יכול לייצר את כל הרצפים של הנוגדנים שנמצאו בדגימה."
"השימוש בעצים נעשה על מנת להשוות בין הדרך שבה נוצרו הרצפים השונים בהדמיה לעומת רצפים שנדגמים אצל אנשים", מוסיפה ברק. "בעצים שנוצרים בהדמיה, כל המוטציות ידועות וכך גם המבנה המדויק של העץ. לעומת זאת ברצפים של נוגדנים שנלקחים מאנשים חסרים שלבים של ההיפר-אבולוציה וקיימים רק התאים ששרדו אותה, ושנמצאו בדגימה. האלגוריתם שיצרנו מאפשר לנו לייצר את העץ השלם מתוך המידע החלקי של הדגימה. תוך שימוש בהשוואה בין העצים של המודל לעצים שנוצרו מדגימת דם אמיתית של אנשים (חולים ובריאים) מצאנו דרך לבדוק איזה שלב בתהליך ההיפר-אבולוציה הוא פגום במחלות שונות (למשל מוטציות שלא מפסיקות גם לאחר שהאנטיגן סולק או מנגנון ברירת נוגדנים שלא עובד כראוי)."
חלק אחר של המחקר עוסק בהתפתחות הארגון של הקוד ליצירת נוגדנים בדנ"א במהלך האבולוציה. בגנום קיימים אזורים המוקצים לספריות המכילות עותקים שונים במעט זה מזה. של החלקים הבונים את הנוגדן. הנוגדן עצמו נבנה כמו תצרף. לוקחים חלק מפה וחלק משם ומחברים אותם ביחד, אבל לא תמיד בדיוק באותה צורה. מטרתו של תהליך ביולוגי זה היא לייצר שונוּת בניגוד לכל תא אחר בגוף, שם המטרה היא לייצר תא זהה שיחליף תא שסיים את חייו, למשל תא שריר. שונות זו מועצמת לאחר מכן בתהליך ההיפר-אבולוציה שמתרחש רק לאחר חשיפה בפועל לאנטיגן.
תאי מערכת החיסון, תאי B ותאי T (שבהם לא עסק מחקר זה) מסתובבים בגוף. אף שכל תאי B מקורם באותו גנום, הם מבטאים נוגדנים שונים לחלוטין וכל אחד מהם יהיה מסוגל להתקשר לאנטיגן אחר. תאי B המתחברים בקלות רבה מדי לתאים של הגוף עצמו יומתו, כל שאר התאים ישרדו ויכסו את מרחב המבנים האפשריים השונים של אנטיגנים זרים.
"הסידור בגנום של ספריות הגנים לנוגדנים נמצא בצורות שונות אצל בעלי חיים שונים. אצל מקצתם – בייחוד אצל בעלי חיים קדומים יותר − הספריות מכילות גנים שלמים של נוגדנים ללא צורך בחיבורם של חלקים שונים. אצל אחרים החלקים השונים של הנוגדן מפוזרים בספריות שונות. יצרנו הדמיה שתראה כיצד התפתחו ספריות האנטיגנים ביצורים עכשוויים מנוגדן ראשוני יחיד. הספריות נוצרו על ידי מוטציות שמכפילות את קידוד הנוגדן בגנום ומוחקות גנים או יוצרות מוטציות בעותקים של הגנים לנוגדנים. תהליכים אלו מסוגלים לייצר רמת שונוּת גבוהה בנוגדנים המקוּדדים בגנום."
"השאיפה בעתיד היא שעץ האבולוציה של הנוגדנים, שיילקח מדגימת דם או רקמה של החולה, יוכל להיות כלי דיאגנוסטי, אבל לכך עוד נדרש זמן. היום אפשר לרצף גנום בכ-4,000 דולר. ברגע שאפשר יהיה לעשות דברים כאלה בקלות רבה יותר ובמחיר זול יותר, אפשר יהיה לבצע בדיקת דם ולדעת מיד אם האדם כרגע חולה ואם כן, איך מערכת החיסון שלו מגיבה לתרופות, וכך להתאים לו תרופה יותר נכונה. הביולוגיה מתכנסת לכיוון של פיתוח תרופות מותאמות אישית למחלה שממש מתרחשת בגוף. האלגוריתם שיצרנו למציאת עץ ההיפר-אבולוציה של נוגדנים התגלה כשימושי גם בתחום ביולוגי שונה לחלוטין – זה של עריכת רנ"א. עריכת רנ"א, שבה מוחלף הבסיס אדנוזין באינוזין (Adenosine-to-Inosine RNA editing) מתרחשת בצורה אינטנסיבית במוח האנושי. העריכה משנה את התוכן המקורי של הגנום המשועתק, ויש המשערים כי היא קשורה לתהליכי חשיבה.
למרות ההבדלים בתהליכים הביולוגים, המידע המנותח בשני המקרים – עריכת רנ"א והתפתחות נוגדנים – חולק קווי דמיון מסוימים: רצף הדנ"א המקורי ידוע, אורך הרצפים הנבדקים זהה, לא כל המוטציות במקרה של גנים של נוגדנים או כל אירועי עריכת הרנ"א נמצאות כרצפים שונים במידע הנדגם, ובשני המקרים ייצוג של המידע כעץ יכול להביא לתובנות על התנאים הביולוגיים של המערכת ממנה התקבל המידע.
במחקר משותף עם ד"ר ארז לבנון מאוניברסיטת הרווארד השתמשנו בעצי עריכה ומצאנו כי עריכת רנ"א היא מקור לשונות גדולה מאוד.
אודות החוקרת
ברק עברה באוניברסיטת בר-אילן מסלול די ייחודי. את התואר הראשון היא עשתה בכלל בפיסיקה ומחשבים, בתואר שני היא התמחתה בפיסיקה חישובית, ואילו הדוקטורט שעשתה אצל רמית מר עוסק בביולוגיה חישובית. "ביולוגיה חישובית וביולוגיה תיאורטית בכלל הם תחומים חדשים יחסית. כשריצוף ה-DNA פתח בפנינו כמויות מידע ענקיות שלביולוגיה הקלאסית לא היו כלים להתמודד עימו, ועוצמת המחשבים הלכה וגדלה, עברו הביולוגים להשתמש בכלים שפותחו בפיסיקה כגון מודלים של משוואות דיפרנציאליות ומודלים חישוביים, שעד לעת האחרונה שימשו רק בחלק קטן של המחקר הביולוגי, כמו למשל במודלים אקולוגיים. הדמיות בכלים חישוביים, שהשתמשו בהם בפיסיקה, החלו להוכיח את עצמם יעילים גם בביולוגיה.
עם זאת, ברק מעריכה כי תהליך מעבר הפיסיקאים ואנשי המחשבים לביולוגיה עומד להסתיים כי קם דור חדש של סטודנטים שלומדים ביואינפורמטיקה וביולוגיה חישובית, שהם יהיו הדור הבא של החוקרים שמגיעים מביולוגיה.
הכתבה התפרסמה בגלילאו ובכתב העת חידושים של אוניברסיטת בר-אילן

3 תגובות
נודר
נודר
האם אפשר, בצורה מלאכותית לגרום לתא B להקשר לרקמה מסוימת בגוף, כדי למנוע מחלות אוטואמיוניות ?