ממצאיהם עשויים לאפשר חיסון של יותר אנשים המצויים בסכנת הידבקות
בחודש יולי 2019 הכריז ארגון הבריאות העולמי על מצב חירום בין-לאומי בעקבות התפרצות מחלת האבולה בקונגו. עד לפני זמן לא רב, צוותים רפואיים הפועלים באפריקה ניצבו חסרי אונים אל מול התפרצויות קטלניות אלה, אך מאז 2016 פותחו חיסונים שעשויים לשנות את התמונה. יותר מ-100,000 איש כבר חוסנו נגד המחלה האלימה, אך החיסונים עדיין מוגדרים ניסיוניים, הכמות הזמינה מועטה, ויעילותם לטווח הארוך אינה ידועה. מדעני מכון ויצמן למדע איחדו באחרונה כוחות עם צוות מחקר בגרמניה, כדי לחשוף מה בדיוק קורה למערכת החיסונית לאחר מתן החיסון. הממצאים שהתפרסמו בכתב-העת המדעי Nature Medicine, עשויים לסייע בגיבוש אסטרטגיות טובות יותר להתמודדות עם המחלה ולמניעתה.
"קשה מאוד לייצר חיסונים נגד אבולה, המופקים בשיטות גנטיות רקומביננטיות באמצעות הצמדת חלבון אבולה לנגיף בלתי-מזיק", אומר ד"ר רון דיסקין מהמחלקה לביולוגיה מבנית במכון. "לפיכך, אין די בכמות החיסונים המיוצרת כיום כדי לחסן את כלל האוכלוסייה, והחיסון ניתן רק לאנשים הנמצאים במגע הדוק ביותר עם חולי אבולה. אם נבין טוב יותר את התגובה החיסונית, נוכל לא רק לשפר את החיסון עצמו – אלא אף להבין אם המינון הניתן כיום הוא אופטימלי, ואם החיסון יעיל נגד זנים שונים של הנגיף".
קשה מאוד לייצר חיסונים נגד אבולה, ולכן אין די בכמות החיסונים המיוצרת כיום כדי לחסן את כלל האוכלוסייה"
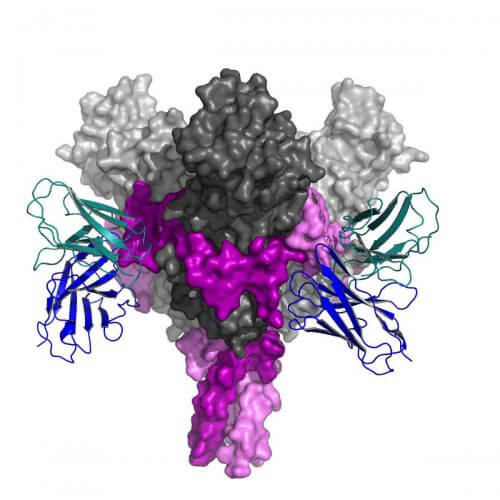
ד"ר פלוריאן קליין מאוניברסיטת קלן וקבוצת המחקר שלו ניסו לאתר סימנים לתגובה החיסונית בדגימות דם של שישה נבדקים שקיבלו את החיסון שנה ויותר קודם לכן. הם התמקדו בתאי B אשר מייצרים נוגדנים המהווים את "הזיכרון החיסוני" שלנו, ואיתרו מספר רב של נוגדנים הנקשרים לחלבונים של נגיפי אבולה. ד"ר דיסקין וצוות המחקר שלו – הכולל את ד"ר נדב אלעד מהמחלקה לתשתיות למחקר כימי וד"ר הדס כהן-דבשי מקבוצת המחקר של ד"ר דיסקין – החליטו להתמקד בשניים מבין נוגדנים אלה, שנחשדו כבעלי מעורבות עמוקה בתגובה החיסונית ארוכת הטווח שמונעת הדבקה. מטרתם הייתה להבין כיצד והיכן נקשרים נוגדנים אלה לחלבון הנמצא על-גבי הקרום החיצוני של הנגיף (חלבון שעליו מתבסס החיסון), ואיך בדיוק היקשרות זו מנטרלת את הנגיף בצורה כה יעילה. לשם כך, נעזרו החוקרים במערכת חדשה: מיקרוסקופ אלקטרונים עוצמתי ומתקדם, שהותקן באחרונה ביחידת המיקרוסקופיה האלקטרונית של מכון ויצמן למדע, המאפשר לזהות את המבנה התלת-ממדי – עד לרמת האטומים הבודדים – של נוגדן הקשור לאתר המטרה שלו. "עד לאחרונה, מחקר שכזה בביולוגיה מבנית היה כרוך בתהליך מסובך של יצירת גבישים וביצוע קריסטלוגרפיה בקרני רנטגן – תהליך הנמשך בדרך כלל כמה חודשים ויותר", אומר ד"ר דיסקין. "כעת אנו יכולים לדלג על יצירת הגבישים ולפענח מבנה של חלבון בתוך שבועות ספורים".
הנוגדנים שחקרנו נקשרים ביעילות גבוהה יותר לחלבון הנגיפי מנוגדנים אחרים הנבחנים כיום כטיפול אפשרי באבולה"
אף שרבים מהנוגדנים שהופקו על ידי תאי B נקשרו לחלבונים של הנגיף – חלקם כנראה ביעילות גבוהה יותר מאחרים – החוקרים הראו כי שני הנוגדנים שבהם התמקדו אכן יעילים במיוחד בעצירת הנגיף. ד"ר דיסקין ועמיתיו חשפו את המבנה של נוגדנים אלה ומיפו את הנקודות המדויקות שבהן נקשרו לחלבון הנגיפי. "למעשה", אומר דיסקין, "הנוגדנים שחקרנו נקשרים ביעילות גבוהה יותר לחלבון הנגיפי מנוגדנים אחרים הנבחנים כיום כטיפול אפשרי באבולה".
ממצא חשוב נוסף שעלה במחקר הוא כי בדמם של נבדקים שקיבלו מינון נמוך יותר של החיסון נמצאה כמות נוגדנים יעילים הדומה לזו שבדמם של נבדקים שקיבלו מינון גבוה יותר. עובדה זו עשויה להוביל לבחינה מחודשת של הפרוטוקולים לטיפול, ואולי לאפשר בעתיד הגנה לאנשים רבים יותר על-ידי הזרקה של מנות חיסון קטנות יותר. לחוקרים אין בשלב זה די מידע כדי לקבוע אם החיסונים אכן יעילים נגד זנים שונים של אבולה, הנפוצים באזורים שונים של אפריקה, אך הם מקווים כי מחקר נוסף יספק את המידע הזה, ואף יאפשר לשפר את החיסון כך שיוכל להילחם בתפוצת המחלה בכל רחבי היבשת.
למאמר המדעי
