P2 הוא רק בן 18 והוא קיבל עירוי דם חודשי מאז היה בן 3, עקב מחלת הבטא תלסמיה. אך במשך 21 החודשים האחרונים, הוא לא היה זקוק להם. צוות בין לאומי של מדענים הצליח לתקן באופן חלקי את הפגם הגנטי, ולאפשר לו עצמאות. זהו ניצחון גדול לריפוי הגנטי, הפעולה של עריכת גנים פגומים בתוך התאים החיים במטרה לטפל במחלות.
מחקר חדש שפורסם במגזין Nature ב-16 בספטמבר 2010, הביא את סיפור הריפוי הגנטי של החולה P2 ממחלת בטא-תלסמיה. בטא תלסמיה היא מחלה גנטית רצסיבית, כלומר צריך לרשת שני עותקים פגומים של המחלה, אחד מכל הורה, בכדי שהיא תבוא לידי ביטוי. במחלה זו תאי הדם האדומים נוצרים עם המוגלובין פגום. ההמוגלובין הוא חלבון הנמצא בתוך תאי הדם האדומים והוא המאפשר להם לשאת חמצן מהריאות אל רחבי הגוף. ההמוגלובין מורכב משתי תת יחידות, אלפא גלובין ובטא גלובין, המיוצרות על ידי גנים שונים. במחלת בטא תלסמיה ייצור הבטא גלובין הוא שנפגע. החולים בבטא תלסמיה סובלים מאנמיה חריפה ומסכנת חיים מאחר ואינם מייצרים די כדוריות דם אדומות תקינות. הדרך היחידה להחזיקם בחיים היא ריבוי עירויי דם, זאת כיוון שתאי הדם האדומים חיים שלושה חודשים בלבד. התרופה הנוכחית היחידה היא השתלת תאי גזע של מוח העצם מקרוב משפחה. אפשרות זו לא תמיד זמינה, וגם כשהיא זמינה היא מסוכנת ואינה מבטיחה הצלחה.
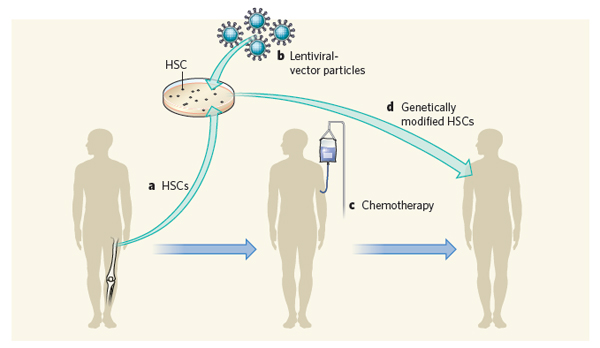
מרינה קוואזאנו-קאבאלו ( Cavazzana-Calvo) ועמנואל פאיין (Payen) בחרו בגישה אחרת. הם ניסו לתקן באופן ישיר את הגנים הבעייתיים מאחורי המחלה. הם עבדו עם צוות בין לאומי גדול, לקחו קצת תאי גזע ממוח העצם (שם נוצרים תאי הדם) מP2 והדביקו אותם בנגיף שהכיל עותק תקין של הגן לבטא גלובין.
הנגיף בו השתמשו הוא מסוג לנטיוירוס (lentivirus) המסוגל להכניס את הגנום שלו לתוך הגנום של התאים אותם הוא מדביק. גם נגיף האיידס שייך למשפחה הזאת, אך הנגיפים המשתמשים בריפוי הגני עברו טיפול המונע מהם להתרבות בכוחות עצמם ומטרתם היחידה היא לשמש כלי הובלה להכנסת הגנים הרצויים לתוך התאים. בתור מקדם בטיחות נוסף, הנגיף מתוכנת לשתק את עצמו לאחר שהעביר את המידע לגנום.
לפני שקיבל את תאי הגזע לייצור דם החדשים, P2 עבר סיבוב של כימותרפיה כדי לנקות את הגוף שלו מתאי הדם הפגומים הקיימים. זה תהליך לא פשוט אך הוא מכין את הגוף לקבלת התאים המתוקנים, שהוכנסו לגופו לפני שלוש שנים ב-7 ביוני 2007. לאחר שנה P2 קיבל את עירוי הדם האחרון שלו. הוא לא היה זקוק לעירוי נוסף במשך השנתיים הבאות. הוא עדיין סובל מאנמיה קלה אך איכות החיים שלו טובה.
הצלחה חדשה זו באה לאחר הרבה עבודה קשה. השיטה נוסתה בהצלחה בעכברים בשנת 2000 ועברה שדרוגים במהלך השנים הבאות. מקרה זה הוא הראשון בו ההשתלה חזרה של התאים המתוקנים עברה בהצלחה. התאים המתוקנים מהווים רק תשעית מסך תאי הדם האדומים של P2 , ומולקולות הבטא גלובין המתוקנות הן רק שליש מתוך אלה. אף שאינם הרוב, הם מספיקים כדי להבטיח שיש לו מספיק עותקים תקינים של המוגלובין כדי לאפשר לו עצמאות.
הצלחת הריפוי הגנטי מגיעה עם הערת אזהרה. אין דרך לדעת היכן יוחדר העותק התקין של הגן בתוך הגנום. נקודה זו עשוי להוביל לפגיעה בתפקוד של גן אחר, למרות שאז קיים העותק השני של אותו גן שימשיך לתפקד כראוי. התרחיש ממנו חוששים במיוחד הוא המקרה בו החדרת העותק משבשת שלב בבקרת תהליך החלוקה התאית ומובילה לגידול סרטני, כפי שכבר קרה במקרי ריפוי גנטי בעבר.

3 תגובות
לא מצאתי את שמות החוקרים, לפי דעתי משהו לא הגיוני.
אז ההצעה שלי היא זו כדי לפתור את בעית הגנים המתמקמים לא טוב.
1. לשכפל תא בודד לאחר שעבר השתלת גן, לשמור חלק מהשיכפולים ולהשתמש באחרים לריצוף גנטי ( אני מבין שהם נהרסים בתהליך )
2. לאחר שיזוהה הריצוף הגנטי התקין להשתמש בתאים ששמרנו לביצוע תהליך הריפוי.
3. אם אין גינום תקין לחזור להשתלת הגנים בעזרת הוירוס עד שיהי גינום תקין.
אני מבין שצואר הבקבוק פה הוא אי המצאותו של מרצף גנים מהיר וזול והתהליך היום יכול להיות יקר וארוך
ואז יגיע מישהו ויגיד שמתעללים בבעלי חיים.
צריך להבין שניסוי בחיות הוא שלב הכרחי בהמצאת תרופה שיכולה להציל בנים וגם חיות