מערכת לשחרור תרופה נוגדת-סרטן, המבוססת על חומר חדשני המכונה ננו-ספוג (nanosponge), יעילה יותר פי שלושה עד חמישה בצמצום ההתפתחות של גידול סרטני מאשר הזרקה ישירה
"מערכות יעילות להעברה ממוקדת של תרופות היוו יעד נכסף מזה זמן רב, אולם פיתוחן עוכב בשל הכימיה המורכבת הכרוכה בהן," אמרה החוקרת Eva Harth, פרופסור לכימיה באוניברסיטת Vanderbilt, אשר פיתחה את מערכת ההעברה החדשנית. "הצלחנו לבצע התקדמות רצינית בהתגברות על מהמורות אלו."
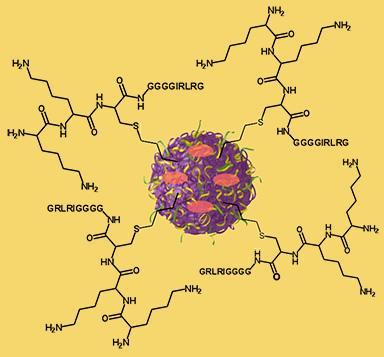
בכדי להבין את המערכת החדשה, תארו לעצמכם הכנה של ספוגיות זעירות, בגודל של נגיף, מילוין בתרופה הרצויה וקישור מחברים כימיים ייחודיים אליה המגיבים באופן מועדף עם קבוצות כימיות המצויות על-פני השטח של תאים סרטניים בלבד, ואז הזרקתן למטופל. הספוגיות הזעירות זורמות במחזור הדם עד אשר הן נתקלות בפני-השטח של תא סרטני ובשלב הזה הן "עוגנות" עליו (או חודרות אליו פנימה) ומתחילות לשחרר את המטען הפעיל שלהן באופן מבוקר ומדוד.
למערכות העברה ממוקדת מסוג זה יש מספר יתרונות: מאחר והתרופה משוחררת לתוך התאים הסרטניים ולא מפוזרת במערכות הגוף השונות, יעילותה, יחסית למינון, אמורה להיות גבוהה יותר. כמו-כן, היא אמורה להניב פחות תופעות לוואי מזיקות מאחר וכמויות קטנות יותר של התרופה מגיעות, אם בכלל, לרקמות בריאות.
"אנו מכנים את החומר ננו-ספוג, אולם זה דומה יותר, בעצם, לרשת או פיגום תלת-מימדי," מסבירה החוקרת. השלד של החומר הינו שרשראות ארוכות של הפולימר פוליאסטר. הפולימר מעורבב בתמיסה עם פרודות קטנות המכונות חיבורי-צילוב (cross-linkers) המתפקדות כמו ווי-חיבור זעירים בכדי לחבר חלקים שונים של הפולימר יחדיו. התוצאה הסופית הינה קבלת חלקיקים כדוריים המלאים בחללים, שבתוכם ניתן לאחסן את פרודות התרופה. הפוליאסטר פריק ביולוגית כך שהוא מתפרק בהדרגתיות בתוככי הגוף. תוך כדי התפרקותו זו הוא משחרר את התרופה אותה הוא נושא בשיעורים ידועים מראש.
"שחרור מדוד הינו אחד מהיתרונות החשובים ביותר של מערכת זו בהשוואה לננו-מערכות העברה אחרות הנמצאות בפיתוח כיום," מציינת החוקרת. כאשר הן מגיעות ליעדן, הרבה מהמערכות האחרות פורקות את מרבית מכמות התרופה שלהן באופן מהיר ובלתי-מבוקר. התנהגות זו מכונה "תוצא ההתפרצות" והיא מקשה על קביעת מינוני התרופה המדויקים.
יתרון חשוב נוסף הינו בכך שחלקיקי ננו-הספוגית מסיסים במים. עיטוף התרופה נוגדת הסרטן בננו-ספוגית מאפשר להשתמש בתרופות הידרופוביות ("דוחות מים") שאינן מסיסות במים. כיום, חייבים לערבב את התרופות הללו עם כימיקל נוסף, הקרוי adjuvant (מסייע) העלול להפחית את יעילות התרופה ולגרום לתופעות-לוואי מזיקות.
בנוסף, ניתן לשלוט בגודלם של חלקיקי ננו-הספוגית – באמצעות שינוי היחס בין פרודות הפולימר לפרודות החיבור ניתן להגדיל או להפחית את גודלם של החלקיקים. עובדה זו חשובה מאחר ומחקר הראה כי מערכות להעברת תרופות פועלות באופן מיטבי כאשר גודלן קטן ממאה ננומטרים – בערך כעומקן של השקעים על-גבי השטח של תקליטור. החלקיקים ששימשו במחקר הנוכחי היו בגודל של חמישים ננומטרים. "התלות שבין גודל החלקיק ויעילות הפעילות שלו הינה המוקד של מחקר נמרץ," מציינת החוקרת.
היתרון החשוב הנוסף של המערכת החדשנית טמון בכימיה הפשוטה הנדרשת להכנתה. החוקרים פיתחו שיטות סינתזה פשוטות ובעלות ניצולת גבוהה להכנת ננו-החלקיקים הללו ולקישור ווי-החיבור המורכבים מפפטידים. "הרבה ממערכות העברת התרופות האחרות מחייבות שימוש בכימיה מורכבת שמקשה על העברת הייצור לקנה-מידה תעשייתי ומסחרי," אומרת החוקרת.
