חוקרים עשו שימוש בננו-סיבים בצפיפות גבוהה המחקים את המיקרו-סביבה של המוח על מנת ללכוד תאים סרטניים במסגרת מחקר הסולל את הדרך לפיתוח פתרונות טיפוליים חדשניים עבור סרטן מוח אלים
[תרגום מאת ד"ר משה נחמני]
גידולים במוח קשים להכלה ולרוב הם עמידים לשיטות טיפול רגילות. חיזוי ההתנהגות של תאים סרטניים מחייב הבנה טובה יותר של מנגנון ההתפשטות שלהם. כעת, חוקרים מאוניברסיטת פוקואי ביפן עשו שימוש בננו-סיבים בצפיפות גבוהה המחקים את המיקרו-סביבה של המוח על מנת ללכוד תאים סרטניים במסגרת מחקר הסולל את הדרך לפיתוח פתרונות טיפוליים חדשניים עבר סרטן מוח אלים.
הגוף שלנו מרפא את הפציעות שלו על ידי החלפת תאים פגועים בתאים חדשים ובריאים. התאים החדשים לרוב נודדים לאתר הפגיעה, בתהליך הידוע בשם 'נדידת תאים'. אולם, נדידת תאים לא תקינה יכולה לעודד גם את ההעברה וההתפשטות של תאים סרטניים בתוך הגוף. גְּלִיּוֹבְּלַסְטוֹמָה רַב-צוּרָתִית (Glioblastoma multiforme, GBM) היא דוגמה אחת כזו של גידול מוח אלים מאוד המתפשט דרך נדידה של תאים סרטניים. התכיפות שבה תאים סרטניים שכאלו מתפשטים וגדלים הופכת את שיטות ההסרה הרגילות של סרטן זה לבלתי יעילות.
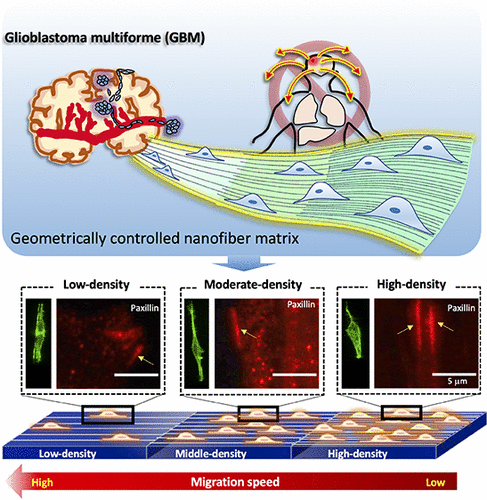
בנוסף, אפשרויות טיפול אחרות כגון רדיו-תרפיה וכימותרפיה פוגעות בתאים בריאים וגורמות לתופעות לוואי שליליות. על מנת לפתח שיטות ריפוי משופרות, נדרשת לנו הבנה מדויקת של מנגנון הפלישה של תאים סרטניים מסוג זה. שיטת טיפול חלופית אפשרית מערבת לכידה של התאים הסרטניים הנודדים. מסתבר כי נדידת תאים מוכתבת על ידי המבנה והכיווניות של המַשְׁתִּית החוּץ-תָּאִית (extracellular matrix, ECM) – מבנים סיביים מסביב לתאים. על ידי הנדוס מבנים דומים בעלי כיווניות נדרשת, ניתן, לפיכך, לשלוט בתהליך הנדידה. כעת, במחקר שפורסם במאמר בכתב-העת המדעיApplied Bio Materials, חוקרים מאוניברסיטת פוקואי ביפן פיתחו פלטפורמה המבוססת על ננו-סיבים המחקים את המַשְׁתִּית החוּץ-תָּאִית על מנת לבחון את ההשפעה שלהם על תאי הסרטן. "סנתזנו משטח של ננו-סיבים שבו צפיפות הסיב משתנה מקצה לקצה תוך שימוש בשיטה של 'טוויה אלקטרוני' (Electrospinning) ובדקנו בעזרתה תאים של סרטן המוח", אמר החוקר הראשי.
החוקרים גילו הבדלים ברורים בתנועת התאים בננו-סיבים בעלי צפיפות שונה. הם מצאו כי הסיבים הדחוסים יותר עודדו את היצירה של צברים מסוג 'הידבקויות מוקדיות' בתאים הגורמים לנדידת תאים איטית יותר. על סמך מתאם שלילי זה שבין קצב תנועת התאים לבין צפיפות הסיבים, החוקרים הצליחו לשלוט ולהכווין את נדידת התאים על ידי תכנון משטח ננו-סיבים בעל צפיפויות משתנות באופן מדורג. על ידי סידור המשטחים בתצורה של צפיפות גבוהה לנמוכה, הם הצליחו להגביל את התנועה של התאים מאחר ורובם פשוט נלכדו בתוך האזורים הצפופים. מצד שני, המשטחים בתצורה של צפיפות נמוכה לגבוהה היו בעלי השפעה הפוכה ודווקא עודדו את הנדידה. בנוסף, הם שמו לב כי הפערים שבין האזורים המעכבים את נדידת התאים גורמים להם להילכד בתוך האזורים הצפופים. נדידה חד-כיוונית כזו נצפתה לראשונה אי פעם והחוקרים כינו אותה 'מלכודת תאים' בהקבלה למלכודות דגים וחרקים הגורמים לטרף שלהם לנוע לאורך כיוון אחד לפני לכידתו.
"המחקר מדגים את ההיתכנות של לכידת תאים נודדים בעזרת ננו-סיבים שנטוו אלקטרונית, סיבים המחקים את מיקרו הסביבה של המוח", אמר החוקר הראשי. לאור ממצאים ראויים לציון אלו, צוות החוקרים נרגש באשר לפוטנציאל העתידי של ננו-הסיבים שלו. "המערכת שלנו זמינה עבור העיצוב של חומרי פיגומים, שהם הבסיס לרפואה מתחדשת (regenerative), בשילוב עם שיטות עיבוד שונות של סיבים ושיטות לטיפול בפני שטח של חומרים. שילוב כזה יוכל להוביל לפיתוח של יישומים מעשיים בתחום של רפואה מתחדשת", אמר החוקר הראשי. "בנוסף, השיטה יכולה לשמש כשיטת עיבוד עבור חומרים נשאים של תרביות לשם ייצור יעיל של תרופות ביולוגיות, לרבות חלבונים, נוגדנים וחיסונים".
עוד בנושא באתר הידען:
