פותח 'נייר דבק' לתאי סרטן, המסוגל לשבת בכלי הדם, למשוך וללכוד תאי סרטן בדם ולקטול אותם לפני שיספיקו ליצור גידולים חדשים בגוף
במחקר שנערך באוניברסיטת רוצ'סטר ועתיד להתפרסם במגזין לביו-טכנולוגיה וביו-הנדסה, הוכח כי ניתן להשתמש בשני חלבונים הנמצאים באופן טבעי בגוף, כדי למשוך ולקטול עד שלושים אחוזים מתאי הסרטן שבזרם הדם – בלי לפגוע בתאים בריאים. החוקר, מיכאל קינג מאוניברסיטת קורנל, פיתח צינור זעיר מצופה בחלבונים. את הצינור ניתן באופן עקרוני להשתיל באחד מכלי-הדם של החולה כדי שיסנן ויהרוס את תאי הסרטן הזורמים באופן חופשי בדם.
למרות שסרטן נוטה להתפתח ברקמות ספציפיות, קיימים סוגי סרטן המסוגלים להתפשט דרך הדם וליצור גרורות סרטניות חדשות ברקמות בריאות. זהו אחד מסוגי הסרטן הקטלניים ביותר והקשים ביותר לטיפול, מכיוון שכמעט ובלתי-אפשרי לתפוס את כל תאי הסרטן שהספיקו להתפשט בגוף. המצאתו של קינג עשויה לספק פתרון לבעיה שטובי הרופאים עמדו נבוכים בפניה בעשרות השנים האחרונות.
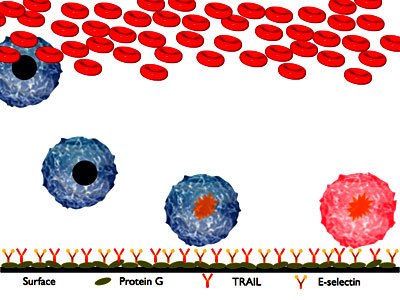
קינג השתמש במולקולות הנקראות סלקטינים על מנת לתפוס את תאי הסרטן. חלבונים אלו מופיעים בדרך-כלל על דפנות כלי-הדם בזמן דלקת וקושרים אליהם תאי דם לבנים המשייטים בזרם הדם. קשירה זאת מאפשרת לתאי הדם הלבנים לזהות את איזורי הדלקת בגוף, ולהגר מתוך כלי הדם אל המקום הפגוע, שם ילחמו בזיהום. קינג הראה כי הוא מסוגל לצפות את הצינור בסלקטינים שיצליחו למשוך ולהדביק אליהם גם תאי סרטן.
ברגע שתאי הסרטן נצמדו לסלקטינים שבצינור, קינג חשף את הסלקטינים לחלבון הנקרא TRAIL (Tumor Necrosis Factor Related Apoptosis-Inducing Ligand). חלבון זה נקשר לשני 'קולטני מוות' על ממברנת התא הסרטני ומעביר דרכם מסר חד-משמעי לתוך התא: למות, ומהר. למרות שתאי הסרטן איבדו כבר את רוב מנגנוני הבקרה הפנימיים שלהם, הם יכולים עדיין לקבל חלק מההוראות המגיעות מהקולטנים, וכתוצאה מהפעלת קולטני המוות מתחילה בתא תגובת שרשרת הגורמת להרס עצמי. לאחר הפעלת הקולטנים משחרר ה- TRAIL את התאים בחזרה לזרם הדם, שם הם מתים – ואז ההתקן חפשי ללכוד ולקטול תאים חדשים.
לפי המחקר העדכני, ההתקן מסוגל לתפוס ולקטול בערך שלושים אחוזים מתאי הסרטן הזורמים דרכו, ובעל פוטנציאל ללכוד הרבה יותר בזרימת הדם בגוף, המתרחשת במעגל סגור. קינג טוען כי בשילוב עם טיפולים שגרתיים לסרטן, ההתקן יוכל לסלק כמות משמעותית של תאי סרטן מהדם, "וייתן לגוף סיכוי לסלק את כל שאר תאי הסרטן."
יעילות ההתקן נבדקה על תאי בלוטת הערמונית סרטניים ותאים סרטניים של המעי הגס, אך אותו רעיון צפוי לעבוד גם על תאי סרטן אחרים, על-ידי שימוש בחלבונים שונים למשיכת התאים וקטילתם. נראה כי ההתקן עצמו אמור להיות קל להשתלה – ואפילו להחלפה – בתוך כלי דם, בשל גודלו המזערי.
"זה מעולם לא נוסה בעבר. זוהי דרך חדשה להסתכל על הטיפול בסרטן," הוא מוסיף. "כמובן שיש עוד הרבה עבודה לעשות לפני שזה באמת עוזר לאנשים – אבל ככה הכל מתחיל." ובכל זאת, עד כמה רחוק מאיתנו החיסון מסרטן גרורתי? נראה כי יש עוד מספר שנים לפני שההתקן יגיע לשוק. קינג מודה כי העברת המחקר ליישום קליני תדרוש זמן ועדיין רחוקה מאיתנו. בכל זאת, הוא אופטימי לגבי העתיד. "אם אתה יכול להפחית או למנוע את התפתחות הגרורות, ניתן יהיה לטפל בערך בכל סרטן."
בכתיבת המאמר השתתפו קולדיפ ראנה, סטודנט לתואר דוקטור בקורנל וג'יין לייאסוולד, דוקטור לרפואה באוניברסיטת רו'צסטר.

5 תגובות
זה באמת כיוון מעורר חשיבה למלחמה בסרטן, שמעולם לא נתקלתי בצורת התבוננות כזו על הבעיה אך האם זה מספיק ?
איזה פתרונות יצירתיים ומעוררי השראה. כל הכבוד
היא תהיה יותר יעילה – וניתן להעביר דרכה את דם החולה ולהחזירו חזרה מסונן.
נניח טיפול כזה כל כמה זמן- נניח כל 3 שבועות נותנים מנת כימוטרפיה – אז לפני כן לסנן את דם החולה במסנן כזה חיצוני- ואז לתת גם כימוטרפיה.
איזה יצירתיות.
לגבי השאלה שבתגובה שמעלי. סביר ששחרור התאים הסרטניים מתרחש לאורך זמן.
אם הסרטן נישא כך בדם ולא מתביית מייד, אז מדוע לא מקיזים מייד את כל הדם של החולה?