חוקרים מאוניברסיטת תל-אביב גילו תהליך שבו וירוס "טוב" מצליח להרוס בצורה סלקטיבית את הדנ"א של החיידק "הרע", וכך לעצור את ההתרבות של החיידק. הגילוי עשוי לסייע בפיתוח טיפולים נגד חיידקים עמידים לאנטיביוטיקה, הגורמים למחלות זיהומיות
המלחמה נגד החיידקים העמידים לאנטיביוטיקה: מחקר חדש של אוניברסיטת תל אביב חשף לראשונה מנגנון שבאמצעותו נגיפים "טובים" מצליחים לתקוף את המערכות של החיידקים "הרעים", מחסלים אותם ומפסיקים את התרבותם. החוקרים הראו שהנגיף "הטוב" (בקטריופאג׳). מצליח לפגוע במנגנון שכפול הדנ"א החיידקי מבלי לפגוע במנגנון השכפול של עצמו. האבחנה בין עצמי לזר היא משמעותית ביותר בטבע. לטענת החוקרים, התגלית חושפת נדבך מרתק נוסף ביחסי הגומלין בין נגיפים וחיידקים ועשויה לשמש גם להבנת מנגנוני התחמקות מנגיפים וגם לשימוש בנגיפים נגד חיידקים.
אתגר עמידות החיידקים לאנטיביוטיקה
המחקר שהתפרסם לאחרונה בכתב עת היוקרתי של האקדמיה הלאומית למדעים של ארה"ב – PNAS, נערך בהובלת פרופ' אודי קימרון, ד"ר דור סלומון, ד"ר טרידיב מהאטה ושחר מולשנסקי-מור מהפקולטה לרפואה ע"ש סאקלר. כמו כן, במחקר השתתפו פרופ' טל פופקו, ראש בית הספר למחקר ביו-רפואי ולחקר הסרטן ע"ש שמוניס ומהמרכז החדש למדעי המידע וד"ר אורן אברם מהפקולטה למדעי החיים ע"ש ג'ורג' וייז, ד"ר עידו יוסף, ד"ר מורן גורן ד"ר מירי מנור-כהן וד"ר ביסוונאט ג'אנה, מהפקולטה לרפואה ע"ש סאקלר.
פרופ' קימרון מסביר כי עמידות של חיידקים לאנטיביוטיקה היא אחת הבעיות המאתגרות שאיתה מתמודדים המדענים בימינו. אחד הפתרונות לבעיה טמון בהעמקת הידע אודות הסיכול הממוקד של החיידקים על-ידי "הנגיפים הטובים", לדבריו, זיהוי מנגנוני ההשתלטות שלהם על חיידקים עשויים לייצר כלים חדשים לטיפול בחיידקים מחוללי מחלות.
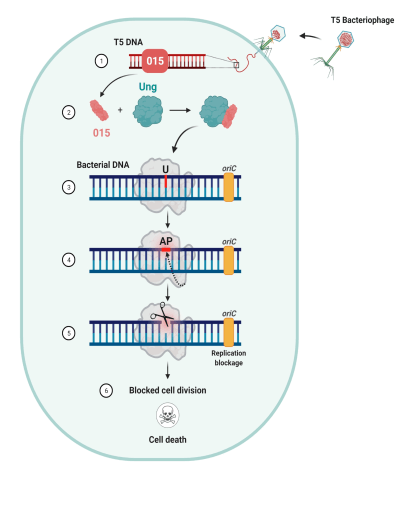
במסגרת המחקר, החוקרים חשפו כאמור לראשונה, את המנגנון של השתלטות הבקטריופאג' על החיידק. על פי החוקרים, חלבון של הנגיף מנצל חלבון לתיקון הדנ"א של החיידק, וכך ב"עורמה" חותך את הדנ"א של החיידק במהלך תיקונו. מכיוון שהדנ"א של הבקטריופאג' לא נזקק לחלבון התיקון הזה, הוא עצמו מוגן מפני החיתוך.
הבקטריופאג' "הטוב" מצליח באמצעי זה גם להבדיל בין הדנ"א של עצמו לזה של החיידק, גם להרוס את החומר התורשתי של החיידק, וגם לעצור את הגדילה והחלוקה שלו.
פרופ' קימרון מוסיף: "הבקטריופאג' מנצל את העובדה שהדנ"א החיידקי זקוק לתיקון מסוים בעוד שהוא עצמו אינו זקוק לתיקון כזה. בכך הוא מחסל את החיידק ללא פגיעה בעצמו. האבחנה בין עצמי לזר חשובה מאין כמוה בטבע, וביישומים ביולוגים שונים. כך לדוגמה, כל מנגנוני האנטיביוטיקה, מבחינים ומנטרלים חיידקים בלבד, תוך פגיעה מינימלית בתאי האדם. כך גם מערכת החיסון שלנו מכוונת לפגיעה מירבית בגורמים חיצוניים, תוך פגיעה עצמית מינימלית".
החוקרים גילו את התהליך על-ידי חיפוש ואיתור סוגים של חיידקים אשר אינם נפגעים ממנגנון הפעולה הנגיפי הזה, כלומר שהחיידק אותו הם תוקפים פיתח "חסינות" או "עמידות" נגד המנגנון הנגיפי. "גילינו שהווריאנטים החיידקיים הללו פשוט הפסיקו לתקן את הדנ"א שלהם בצורה הרגישה לפגיעה, וכך חמקו ממנגנון ההרס. הממצאים שופכים אור נוסף על הדרכים בהם נגיפים חיידקיים תוקפים חיידקים, ועשויים לשמש כלי נוסף במלחמה האינסופית נגד חיידקים עמידים לאנטיביוטיקה" – מסכם פרופ' קימרון.
עוד בנושא באתר הידען:

תגובה אחת
Check his thought on biology
https://geniuses.club/genius/ernst-heinrich-philipp-august-haeckel