מדענים ממכון ויצמן גילו מעין "קרון רכבת" החיוני לחישת הממדים של התאים – חלבון הקרוי "אימפורטין-בטא-1". חלבון זה מעביר את אות החישה בחזרה לגרעין התא.
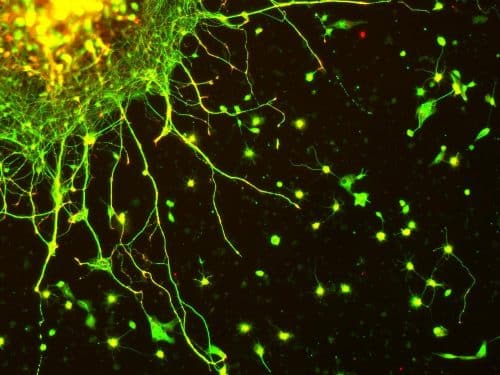
לפני מספר שנים גילו פרופ' מיכאל פיינזילבר וחברי קבוצתו במחלקה למדעים ביומולקולריים של מכון ויצמן למדע, מנגנון חישה שבאמצעותו חשים תאי עצב את ממדיהם. מדובר ב"פסי רכבת" זעירים עליהם "נוסעים" האותות; הם נישאים על גבי מנועים מולקולריים, כמו קרונות רכבת הנגררים על-ידי קטר, ממרכז התא אל קצותיו ובחזרה, ותדירות האותות מאפשרת לתא לקבל מושג על ממדיו. למשל, אם חוזרים ה"קרונות" מהר מקצה התא אל מרכזו, משמעות הדבר היא כי התא קטן. לעומת זאת, כאשר חוזרים האותות לאחר זמן רב יותר, וכתוצאה מכך "נוסעים" ה"קרונות" הלוך וחזור לעיתים רחוקות יותר, מלמד הדבר כי התא גדול יותר.
כעת, במחקר חדש אשר התפרסם באחרונה בכתב-העת המדעי Cell Reports, חשפו החוקרת הבתר-דוקטוריאלית ד"ר רותם בן-טוב פרי, מדענית הסגל ד"ר אידה רישל, ותלמידת המחקר אלה דורון מנדל – יחד עם חברים נוספים בקבוצתו של פרופ' פיינזילבר ועם חוקרים ממוסדות אחרים בארץ ובחו"ל – כיצד פועל מנגנון חישה זה ברמה המולקולרית. תחילה זיהו המדענים "קרון" החיוני לחישת הממדים – חלבון הקרוי "אימפורטין-בטא-1": מולקולת אר-אן-אי שליח, המקודדת הוראות גנטיות ליצירה של החלבון אימפורטין-בטא-1, נוסעת על "פסי הרכבת" המולקולריים ממרכז התא אל קצהו; כאשר מגיעה מולקולה זו אל קצה ה"פסים", מתחילה בנייתו של אימפורטין-בטא-1, וחלבון זה מעביר את אות החישה בחזרה לגרעין התא.

כדי לגלות כיצד "נוסע" האר-אן-אי שליח של אימפורטין-בטא-1 על ה"פסים" המולקולריים, נעזרו המדענים בחומר מחקר מקורי: מבית מטבחיים בצפון הארץ הם אספו גידי נשה של פרות, אשר מושלכים בדרך כלל לפח כיוון שאכילתם אסורה על-פי חוקי הכשרות. גיד הנשה המקראי למעשה איננו גיד אלא עצב, המכיל את השלוחות העצביות הארוכות ביותר בגוף. בתוך שלוחות אלה זיהו המדענים חלבון הקרוי "נוקלאולין". חלבון זה נקשר לאר-אן-אי שליח של אימפורטין-בטא-1, ויחד הם יוצאים לדרך – כמו רכבת בעלת שני קרונות, מגרעין התא אל קצהו.
כאשר שיבשו המדענים את פעילות החלבון נוקלאולין באמצעות תרופה ניסיונית נגד סרטן הנקשרת לחלבון זה, נשארו שני ה"קרונות" – גם הנוקלאולין וגם אר-אן-אי שליח של אימפורטין-בטא-1 – במרכז התא, או "נסעו" מרחק קצר בלבד. היות שהמרחק היה קצר כל כך, הייתה תדירות התנועה על "פסי הרכבת" המולקולריים גבוהה מאוד, ודבר זה היטעה את תא העצב, וגרם לכך שהוא חש כי שלוחתו קצרה הרבה יותר מאשר הייתה במציאות. בתגובה לכך החל תא העצב לגדול בקצב מהיר – לעיתים פי חמישה יותר מהר מהרגיל – ולהצמיח שלוחה ארוכה מאוד. התרופה הנסיונית הקושרת את הנוקלאולין איפשרה למדענים להטעות לא רק את תאי העצב, אלא גם תאי רקמת גוף אחרים, דבר שהוביל את תאים אלה לגדול לממדים חריגים.
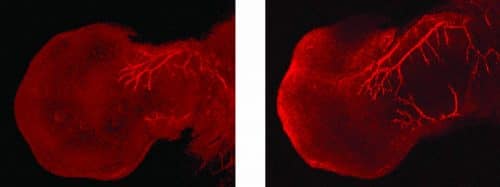
לממצאים אלה עשויות להיות השלכות על חקר מחלת הסרטן, וחקר הצמיחה מחדש ("רגנרציה") של הרקמה העצבית. החלבון נוקלאולין מתבטא בכמויות גדולות בתאי סרטן, והתרופה הניסיונית שבה השתמשו המדענים במחקר, אשר נקשרת לנוקלאולין, הורגת את תאי הגידול, אך המנגנון המדויק שלה אינו ידוע. המחקר החדש, אשר מצביע על כך שנוקלאולין מעורב במנגנון החישה המבקר את צמיחת התאים, עשוי לפתוח כיוון חדש בפיתוח תרופות נגד סרטן. יתר על כן, הבנה לעומק של מנגנון החישה של גודל התאים, אשר מבקר את קצב צמיחת תאי העצב, עשויה בעתיד לסייע בפיתוח אמצעים לזירוז התחדשות הסיבים העצביים לאחר פציעה.
במחקר השתתפו גם ד"ר מרקו טרנזיו, סטפני אלבר, ד"ר סנדיפ קולי, אלבינה לין, ד"ר מאיר רוזנבאום, ד"ר דמיטרי יודין, ופרופ' אברהם ירון מהמחלקה למדעים ביומולקולריים של המכון; ד"ר ורה שינדר מהמחלקה לתשתיות למחקר כימי של המכון; ד"ר וסים ג'ראיסי מ"תנובה"; וכן מדענים מהמעבדות של פרופ׳ ג׳ף טוויס מאוניברסיטת דרום קרוליינה, פרופ׳ אל בורלינגאם מאוניברסיטת קליפורניה, ופרופ׳ קליפורד וולף מבית ספר לרפואה של הרווארד.
מספרי מדע
מנועים מולקולריים נעים בתוך תאים ב"צעדים" של כ-8 ננומטר כל אחד, במהירות ממוצעת של 125 "צעדים" – או 1 מיקרומטר – לשנייה. אם אדם היה צועד באותו הקצב, מהירותו הייתה מגיעה ל-450 קמ״ש.

2 תגובות
אולי מדובר בIPP 204106 ?
מאמרים:
http://adisinsight.springer.com/drugs/800027743
https://clinicaltrials.gov/ct2/show/NCT01711398
האם התרופה הניסיונית נגד סרטן המוזכרת בכתבה ניתנת לבני אדם כבר? אפשר פרטים?