כתב העת SCIENCE בחר, בנוסף לפריצת הדרך של השנה, מספר אירועים ראויים לציון בכמה תחומים מדעיים. אחד התחומים הללו הוא תחום הגנטיקה.

סטייה גנטית קשורה בלמעלה מ- 60,000 מחלות אנושיות, כמעט 35,000 מהן נגרמות על ידי שגיאות קטנות ב-DNA– שינוי של בסיס אחד בנקודה מסויימת בגנום. השנה הודיעו חוקרים על שיפור משמעותי של טכניקה המתהווה, הנקראת עריכת בסיסים, לתיקון מוטציות נקודתיות כאלה לא רק ב- DNA, אלא גם ב-RNA.
חלוץ התחום, דייוד ליו, כימאי באוניברסיטת הרווארד, השתמש במערכת לעריכת בסיסים CRISPR, שהוכח לראשונה ככלי מעבדה רב עוצמה בשנת 2012. CRISPR מצטיין בחיתוך הדנ"א במיקומים ספציפיים, איתור שגיאות וכיבוי הגנים, אבל יש לו הצלחה חלקית בלבד בתיקון טעויות הנגרמות ממוטציה נקודתית, שאחד מארבעת בסיסי ה-DNA כלומר A, C, T ו- G — הוחלף באחר. הקבוצה של ליו שינתה את האפשרויות הקיימות ב-CRISPR כדי ליצור עורך בסיסים זה שלא יחתוך את ה-DNA במיקום היעד אלא יחליף בסיס כימי אחד במשנהו. בשנה שעברה הצליחו החוקרים להחליף C ב-T והשנה החליפו G שגוי במוטציה השכיחה ביותר. יש לציין כי צוות נפרד בראשות ג'אנג פאנג ממכון ברוד הסמוך בקיימברידג', מסצ'וסטס, הדגימו עריכת בסיס שבה הם החליפו G ו-A ב-RNA.
השנה הדגימו החוקרים את הכוח של יכולת עריכת הבסיסים על-ידי תיקון מוטציה גורמת מחלות בעוברי אדם. הם מעולם לא התכוונו לגדל את העוברים, התיקון לא היה תמיד מוצלח, אבל ההישג הוכיח כי בעריכת הבסיס יש פוטנציאל עצום. לדעתם CRISPR הוא מתנה הממשיכה להניב פריצות דרך.
תרופה לסרטן המותאמת ל-DNA של הסרטן ולא לאיבר ממנו גדלה
בחודש מאי, נתנה רשות המזון והתרופות האמריקנית (FDA) אור ירוק למוצר pembrolizumab המיוצר על ידי חברת מרק, תחת שם המותג Keytruda. התרופה, אשר כבר אושרה לטיפול במלנומה וקומץ של סוגי סרטן אחרים, ניתנת כעת בכל מקרה של גידול מוצק מתקדם בילדים או במבוגרים, בתנאי אחד: התאים הסרטניים חייבים לשאת פגם בעל השם מוזר mismatch repair deficiency (תקלה במנגנון תיקון די.אן.אי מסוג MMR) משמעות הדבר היא כי אם התאים הסרטניים מצויים בלבלב, במעי הגס, בבלוטת התריס או בכל אחד מתריסר רקמות אחרות – עליהם לשאת את המוטציה ב-DNA שהתרופה מתקנת.
אישור ה-FDA מרמז על שינוי גדול עבור התחום משום שהוא מראה כי יש הרבה מן המשותף בגידולים שמקורם באיברים שונים. אבל להפוך את הידע הזה לטיפול לא היה קל. פריצת דרך הגיעה בשנת 2015, כאשר רופאים מאוניברסיטת ג'ון הופקינס בבולטימור, מרילנד, בראשות לואיס דיאז ממרכז הסרטן בממוריאל סלואן קטרינג בניו יורק, חקרו pembrolizumab בחולי סרטן המעי הגס. הם הבחינו במשהו בולט: אצל שמונה מתוך 13 אנשים הסובלים מ-,mismatch repair deficiency התכווצו הגידולים, ואצל ארבעה נוספים הם שמרו על גודלם אך הפסיקו לגדול בעת מתן התרופה, התרופה היוותה "מחסום חיסוני מעכב" שמאפשר למערכת החיסונית להילחם בסרטן. 25 חולי סרטן המעי הגס אחרים ללא הפגם לא הגיבו לטיפול. התיאוריה של הרופאים היא כי תאים המכילים את המחסום אמנם צוברים מאות מוטציות אך מערכת החיסון מזהה את התאים הללו כזרים בקלות והורגת אותם.
מחקר שפורסם בחודש יוני על ידי דיאז לי, מאוניברסיטת ג'ונס הופקינס, ומחקרים נוספים הרחיבו יחד את הניסוי לכדי 86 חולים הסובלים מ- 12 סוגי סרטן שונים, אשר לכולם היהmismatch repair deficiency. 53% הגיבו לתרופה. בהתבססו בין היתר על מחקר זה, נתן ה-FDA אישור לתרופה שאונקולוגים מקווים שתהיה התרופה הראשונה מני רבות באסטרטגיה החדשה נגד סרטן.
ניצחון לטיפול גנטי
הצלחה בניסוי קליני קטן דרמטי מסתמנת בתחום של טיפול גנטי השנה. חוקרים דיווחו כי הצילו את חייהם של תינוקות שנולדו עם מחלת ניוון שרירים העוברת בתורשה, באמצעות הוספת גן שיוסיף נוירונים בעמוד השדרה שלהם. אם התינוקות אינם מטופלים, הם עלולים למות עד גיל שנתיים.
הניסוי גם מציין אבן דרך משמעותית יותר, משום שהחוקרים העבירו את הגן החדש דרך הקרום המגן על המוח ועל עמוד השדרה באמצעות פתוגנים ורעלים. ניסוי זה יכול לפתוח את הדלת לריפוי גנטי של מחלות ניווניות אחרות.
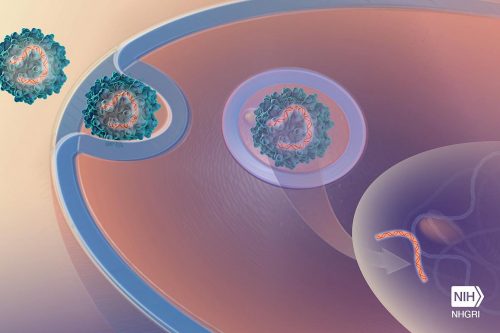
המפתח היה וירוס בלתי מזיק, שנקרא AAV, בו נעשה שימוש נרחב בריפוי גנטי בעכברי מעבדה. בשנת 2009, גילו קבוצות מחקר בצרפת ובבית החולים לילדים בקולומבוס, אוהיו, כי זן של הוירוס שנקרא AAV9 שהוזרק דרך הווריד לעכברים היילודים יכול להתפשט דרך המוח וחוט השדרה.
כעת, חוקרים הראו כי ריפוי גנטי באמצעות AAV9 תוך ורידי יכול לעצור ניוון שרירים של עמוד השדרה מסוג 1 (SMA1), הגורם הגנטי הנפוץ ביותר של מוות אצל תינוקות. אצל ילודים עם SMA1 חסר החלבון הדרוש לתנועת נוירונים בעמוד השידרה; השרירים מדלדלים בסופו של דבר והילודים אינם יכולים לנשום. בחודש נובמבר, חברי קבוצת המחקר וחברת AveXis דיווחו כי כל אחד מ-12 התינוקות שקיבלו מינון גבוה של AAV9 הנושא את הגן של החלבון החסר – יכול לדבר, לאכול ולשבת בעצמו, לפחות לזמן קצר. אחת הילדות אפילו הצליחה ללכת מהר ולהיות ילדה פעילה. התרופה החדשה השיגה תוצאות דומות, אבל חייבים להזריק אותה לתוך עמוד השדרה כל כמה חודשים.
החוקרים עכשיו משתמשים ב-AAV9 שנושא גנים אחרים לטיפול בילדים עם הפרעות קשות במוח שעברו בתורשה. בעבר, החוקרים היו צריכים לקדוח חורים בגולגולת כדי לספק טיפול גנטי לילדים האלה, והטיפול גם לא היה יעיל.
השנה בוצעו שני טיפולים בסרטן בהם המערכת החיסונית של החולה הונדסה גנטית מחוץ לגופו וזו הושתלה בו חזרה. טיפולים אלו הם הטיפולים הגנטיים הראשונים שהגיעו לשוק האמריקני. ב-19 בדצמבר, אישר מינהל המזון והתרופות (FDA) את הטיפול הגנטי הראשון עבור הפרעה תורשתית נדירה הגורמת לעיוורון.
עוד בנושא באתר הידען:

תגובה אחת
כתבה ברורה ויפה.