צוות כימאים מאוניברסיטת הרווארד פיתח שיטה מיקרוסקופית חדשנית עבור הצפייה, בצבע, של פרודות הנעדרות פלואורסצנטיות בטמפרטורת החדר
צוות כימאים מאוניברסיטת הרווארד בראשות החוקר X. Sunney Xie פיתח שיטה מיקרוסקופית חדשנית עבור הצפייה, בצבע, של פרודות הנעדרות פלואורסצנטיות. השיטה, המתבצעת בטמפרטורת החדר, מאפשרת לחוקרים לזהות פרודות שלא ניתן היה לראותן קודם באורגניזמים חיים, ומספקת יכולת לפיתוח מגוון יישומים בדימות ביורפואי ובמחקר מדעי.
נגיהת אור (פלואורסצנטיות) הינה תופעה שבה אלקטרון בפרודה קולט אנרגיה נוספת מקרינת אור חיצונית ועובר לרמת אנרגיה גבוהה יותר, רמה מעוררת. אנרגית האור קיימת ביחידה הקרויה פוטון. לאחר שהות קצרה במצב המעורר, האלקטרון חוזר לרמת האנרגיה המקורית שלו, רמת הבסיס, תוך כדי פליטה של פוטון. האנרגיה של הפוטון שנפלט הינה באורכי-גל של אור הנראה לעין אנושית, אך אור זה מתקיים למשך זמן קצרצר ביותר של מיליארדית השנייה.
רבות מהפרודות הביולוגיות הצבעוניות החשובות, כגון המוגלובין – חלבון המנייד חמצן והמצוי בתאי הדם האדומים – קולטות אור אך אינן פולטות קרינה פלואורסצנטית. בניגוד לכך, האלקטרונים בפרודות אלו פולטים את האנרגיה העודפת שלהם ע"י המרתה לחום. "מאחר ופרודות אלו אינן פולטות קרינה, הן למעשה בלתי-נראות למיקרוסקופים אופטיים עכשוויים," מסביר החוקר הראשי. בכדי לזהות פרודות מסוג זה במערכות ביולוגיות, צוות המחקר פיתח סוג חדיש של מיקרוסקופיה המבוססת על פליטת פוטון מאולצת.
פליטה מאולצת של פוטון תוארה לראשונה ע"י אלברט אינשטיין כבר בשנת 1917, ובעיקרון היא תהליך שבו מערכת קוונטית עוברת ממצב בעל אנרגיה גבוהה, למצב בעל אנרגיה נמוכה יותר על ידי פליטה של אור כתוצאה מאינטראקציה עם השדה החשמלי שבסביבה. הפוטון הנפלט זהה לחלוטין לפוטונים שגרמו לפליטה מבחינת קיטוב, כיוון, תדירות ומופע. ניתן לראות את הפליטה המאולצת כמנגנון הגברה של אור: נכנס פוטון אחד ויוצאים שניים. הכפלה זו היא הבסיס לעקרון הפעולה של הלייזר, וכן של מגברים אופטיים.
שיטת המיקרוסקופיה החדשה מחוללת ורושמת אות פליטה מאולץ באמצעות השימוש בשני מסלולי אותות, קלט ופלט, המתואמים ביניהם במרווחי זמן מדויקים מאוד. במסלול אות הקלט, מאפנן ממתג את עוצמת האלומה המעוררת לכבוי/דלוק בתדירות של חמישה מגהרץ. אפנון זה מחולל אות פליטה מאולץ באותה התדירות. לכל אחד מאותות אלו יש משך פעימה קצר ביותר של כמאתיים פמטו-שניות. האות שנפלט מפרודות בלתי-קורנות אלו במקור מספק תמונה ברגישות גבוהה של פרודות שהיו בעבר בלתי-נראות.
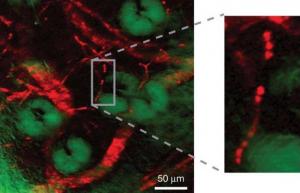
אחד ממספר היישומים האפשריים של המצאה זו הינו המיפוי בצבע של תנועת תרופות בלתי-קורנות לתאי המטרה שלהם. שימוש נוסף אפשרי הינו הדימות של מבנים זעירים ביותר כגון כלי-דם, בכללם תאי דם אדומים ונימים פרטניים.
המבנה והתנועה של חלבוני ההמוגלובין בכלי-הדם השונים הינם בעלי תפקיד משמעותי בתהליכים ביורפואיים רבים. שתי דוגמאות לתהליכים כאלו הינן המעבר של גידולים ממצבם הרדום למצבם הממאיר ואספקת חמצן למוח.
שיטות דימות רפואי קיימות כגון סורקי MRI ו- CT או שחסרות את כושר-ההפרדה המרחבי הדרוש לצפייה בכלי-דם פרטניים או שנדרשים להן חומרי-ניגודיות חיצוניים. תגים פלואורסצנטיים כדוגמת "חלבון קרינה ירוקה" (green fluorescent protein, GFP) נפוצים ביותר לשם הצפייה בפעילותן של ביו-פרודות והזיהוי של פרודות מטרה בתאים. שיטת התיוג בחלבון זה מספקת תמונות ברורות ביותר. למרות זאת, מבנהו הנפחי של החלבון עלול להפריע לפעילות ולמסלולים ביולוגיים עדינים, בעיקר כאשר הוא גדול יותר מביו-הפרודה הנבחנת. צוות המחקר הצליח למפות את המסלול של פרודות תרופה בלתי-קורנות ואת המבנה המפורט של כלי-הדם ללא השימוש בתגים פלואורסצנטיים. שיטתם החדישה מסוגלת גם למפות את החלבונים הבלתי-קורנים בתאים חיים של החיידק אשריכיה קולי.
"בעוד שמחקרים קודמים השתמשו בניסויים דומים בכדי לקבל תמונות בעלות כושר הפרדה מרחבי של פרודות קורנות, המחקר שלנו, לראשונה אי-פעם, השתמש במיקרוסקופית פליטה מאולצת בכדי לדמות פרודות בלתי-קורנות," מסביר אחד מהחוקרים בצוות.
למרות שעדיין יש צורך להתגבר על הסיכוי לנזק פוטוני, על המורכבות ועל העלות הגבוהה של המערכת בכדי שהיא תהיה ישימה יותר, "אין כל ספק שהמחקר שלנו מספק אמצעי ייחודי לדימות מגוון רחב של פרודות, שכיום אינן מתאימות לצפייה אפילו במיקרוסקופיים האופטיים המתקדמים ביותר," מציין החוקר. "זוהי רק ההתחלה," מוסיף החוקר הראשי. "עוד צפויים לצמוח יישומים מענייניים רבים מכלי חדשני זה."
ממצאי המחקר פורסמו בכתב-העת המדעי Nature.

תגובה אחת
מהתמונה נראה שמדובר ברזולוציה שמסתובבת סביב מיקרונים בודדים וזה בהחלט עליה מרשימה ביחס ל MRI שנותן רזולוציה של בערך 40 מיקרון. עדין מדובר במבנים גדולים מאוד בטח שלא תוך תאיים (למעט תאים גדולים מאוד). טכנולוגיה מעניינת מאוד שאני רואה לה יישומים רבים בהקשר של מיקרוביולוגיה סביבתית, תחום בו אני עצמי מתעסק. מעניין כמה יקר מכשיר כזה (אני מנחש שהוא אמור לנוע סביב חמישה מליון יורו) וכמה מהר ישתכנעו חוקרים שיש כאן פוטנציאל שיחזיר את ההשקעה. בסופו של דבר זו המצאה נהדרת אבל כנראה שלא תפרוץ יותר מדי גבולות בביולוגיה שזקוקה לרזולוציות קטנות ממיקרון.