תוכנית המחקר של יבמ בתחום הפולימרים לננו-רפואה מתנהלת זה ארבע שנים, על בסיס מסורת של עשורים ארוכים של פיתוח חומרים בתחום המיקרו-אלקטרוניקה.
מדענים ביבמ ובמכון האמריקאי לביו-הנדסה ולננו-טכנולוגיה פיתחו ג'ל אנטי-בקטריאלי על בסיס מים המסוגל לחדור משטחי חיידקים ורקמות נגועות ולחסל לחלוטין חיידקים עמידים לתרופות, באמצעות מגע בלבד עם החיידקים האלה. תוצאות המחקר מתפרסמים החודש בעיתון המדעי Angewandte Chemie
הג'ל הסינתטי, הנוצר בתהליך ספונטאני בחימום נוזל-ממיס אל הטמפרטורה של הגוף האנושי, הוא הטיפול הראשון מסוגו אי-פעם המתכלה בתהליך ביולוגי ותואם למבנה ולתהליכים הביולוגיים של הגוף, באמצעות חומר בלתי-רעיל. כל אלה, הופכים אותו לכלי אידיאלי למלחמה בסיכונים בריאותיים חמורים המאיימים על עובדי בתי חולים, מבקרים ומטופלים.
חיטוי משטחים ביתיים מתבצע באמצעות חומרים דוגמת אלכוהול ואקונומיקה. אלא שמעבר מהמשטחים האלה לטיפול בחיידקים עמידים לתרופות הגורמים לזיהומים בעור או למחלות מדבקות הוא אתגר מורכב יותר: אנטיביוטיקה קונבנציונאלית הופכת פחות ופחות אפקטיבית בשל התפתחות חיידקים עמידים, בעוד החומרים המשמשים לניקיון ביתי אינם מתאימים לשימוש על פני הגוף.
המדענים ביבמ פיתחו ג'ל אנטי-בקטריאלי הניתן למריחה ולשימוש נוח – ומורכב מ- 90% מים, בשילוב עם חומרים פולימריים במבנה ייחודי. אם יגיע הפיתוח הזה לשלב השימוש הרפואי המסחרי, הוא יתאים במיוחד למשחות ולטיפולים בהזרקה לריפוי פצעים, ציפוי שתלים ונקזים (קטטר), זיהומי עור ואף זיהומים חודרניים יותר. משטחי זיהום חיידקי מסוגלים להתרבות על גבי כל רקמה או משטח. קבוצות תאים נגועים כאלה נמצאות ב- 80% ממקרי הזיהום, ואופייניות למגוון רחב של אזורים בגוף, במיוחד בשימוש בציוד רפואי. הזיהומים האלה מהווים חלק משמעותי מהזיהומים בבתי חולים, המהווים אחת מחמש הסיבות השכיחות ביותר למוות בארה"ב, ואחראים להוצאה של 11 מיליארד דולר מתקציבי הבריאות האמריקאים.
למרות ההתקדמות בטכנולוגיות הסטריליזציה והחיטוי, זיהומים הקשורים בשימוש בציוד רפואי ממשיכים להתקיים ולהכות במטופלים. זאת, גם בשל התפתחות חיידקים עמידים לתרופות. על פי נתוני המרכז האמריקאי לבקרת מחלות, עלות הטיפול בחולים בחיידקים עמידים לתרופות מוערכת ב- 20 מיליארד דולר בשנה, ובשמונה מיליון ימי אשפוז נוספים.
באמצעות תפירה מדוייקת של פולימרים, הצליחו החוקרים ביבמ לתכנן מולקולות-ענק, הכוללות כמות גדולה של אטומים, המשלבות מסיסות במים, מטען חשמלי חיובי ומאפיינים של כושר התכלות ביולוגי. כאשר מערבבים את המולקולות האלה במים ומחממים את התמיסה לטמפרטורה של הגוף האנושי, עוברים הפולימרים תהליך הרכבה עצמית, והופכים לג'ל סינתטי קל למריחה ולשימוש. היכולת הנדירה הזאת נובעת מאינטראקציות פנימיות בין הפולימרים באמצעות מה שמכונה "רוכסן מולקולארי": כמו השיניים ברוכסן בגד המשתלבות זו בזו – יודעים הפולימרים ליצור קשר ההופך את התמיסה מבוססת המים לג'ל סמיך. כיוון שהג'ל הזה שומר על המאפיינים של הפולימרים המסיסים, הם יכולים להישאר במקומם בתנאים פיזיולוגיים שונים, ולהמשיך בפעילותם האנטי-בקטריאלית.
הגישה של החוקרים ביבמ שונה מהותית מהשיטות הקיימות למלחמה בחיידקים עמידים לתרופות.
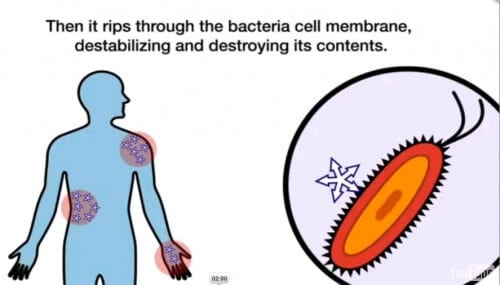
הטכנולוגיה החדשה מופיעה בעידן שבו אנטיביוטיקות ותרופות קודמות מתקשות להתמודד עם חיידקים עמידים – ומציעה שיטה חדשה למלחמה בחיידקים האלה: בעוד האנטיביוטיקה מתמקדת במכאניזם הפנימי של החיידק, מחסל הג'ל את החיידק באמצעות פגיעה בממברנה, הקרום החיצוני החיוני לקיומו. כאשר מורחים את הג'ל החדש על גבי משטח נגוע, מושך המטען החשמלי החיובי שלו את כל הממברנות של חיידקים המאופיינות במטען שלילי, ושואב אותן באופן דומה לזה שבו שואב חור שחור עצמים בעלי מסה.
תוכנית המחקר של יבמ בתחום הפולימרים לננו-רפואה מתנהלת זה ארבע שנים, על בסיס מסורת של עשורים ארוכים של פיתוח חומרים בתחום המיקרו-אלקטרוניקה.

4 תגובות
מה הקשר לחור שחור? ומה עושה שאיבת הממברנה? היא משאירה את החיידק ללא ממברנה? היא מושכת את כל החיידק לתמיסה? לא ברור
לא הבנתי איך זה עדיף על כלור בריכוז 1000 ppm שמשתמשים בו היום.
בתוך הדף המקושר מתחתית הכתבה
אפשאר קישור לסרטון?