צוות חוקרים משותף מאוניברסיטאות מישיגן וקליפורניה פיתחו שיטה חדשה למציאת תרופות הפועלות על מולקולות רנ"א
צוות חוקרים משותף מאוניברסיטאות מישיגן וקליפורניה פיתחו שיטה חדשה למציאת תרופות הפועלות על מולקולות רנ"א.
מסתבר כי מי שנחשבה עד לא מזמן כמולקולה המעבירה באופן סביל מידע גנטי בלבד, מולקולת הרנ"א, מבצעת מספר תפקידים חיוניים אחרים בתא, והתפקוד הפגום שלה עשוי להוביל להתפרצות מחלות. המולקולה הזו חיונית גם לרטרו-וירוסים כגון נגיף האיידס, שאינו מכיל בתוכו דנ"א, ואשר במקום זאת מסתמך על מולקולת הרנ"א הן לשם העברת מידע גנטי והן לשם הפגנת יכולותיו לפלוש אל ולהשתלט על התא המארח. ככל שמתגלים יותר ויותר קשרים להתפרצות מחלות, החיפוש אחר תרופות הפועלות על רנ"א הולך ומתרחב.
אולם, החיפוש אחר תרופות שכאלו אינו פשוט. רוב הכלים לגילוי תרופות כיום מתוכננים למצוא מולקולות קטנות הנקשרות למטרות חלבון, אולם רנ"א אינו חלבון והוא שונה מחלבונים במאפיינים חשובים רבים. "כך שהתפתח צורך הולך וגדל לטכנולוגיות מתקדמות שבאמצעותן ניתן לאתר תרכובות הנקשרות לרנ"א," אמר Hashim M. Al-Hashimi, פרופסור לכימיה ולביופיסיקה באוניברסיטת מישיגן.
החוקרים התאימו שיטה מחשובית קיימת לסריקת ספריות של מולקולות קטנות על מנת לקבוע את היכולות שלהן להיקשר למולקולת רנ"א. בשיטה זו, קובעים בתחילה את צורתה של מולקולת היעד באמצעות קריסטלוגרפיית קרני-רנטגן או באמצעות ספקטרוסקופיית תמ"ג (NMR); בשלב הבא, החוקרים מריצים הדמיות מחשב בכדי לקבוע כיצד מולקולות קטנות – תרופות אפשריות, לדוגמא – נכנסות ונקשרות אל מבנה המטרה. רנ"א מהווה אתגר רציני עבור שיטה זו מאחר והוא אינו מורכב מתצורה אחת בלבד – זוהי מולקולה גמישה המסוגלת לאמץ לעצמה צורות שונות בהתאם למולקולה שנקשרה אליה.
בעבר סברו המדענים כי יחסי הגומלין בין מולקולות התרופות לבין הרנ"א הם האחראיים לשינויי המבנה, וכי לא ניתן לחזות מראש מה תהיה הצורה שהרנ"א יאמץ לעצמו בעקבות קשירה למולקולה קטנה נתונה. אולם, במחקרם הקודם, צוות המדענים אתגר את הרעיון הזה באמצעות ההדגמה כי רנ"א, בפני עצמו, מסוגל לעבור בין הצורות השונות שלו גם כאשר הוא קשור לתרופות שונות. החוקרים גילו כי כל מולקולת תרופה פשוט "ממתינה" שהרנ"א יגיע לצורה המועדפת עבורה, ואז נקשרת אליו.
במחקר חדש זה, החוקרים הצליחו להקפיא "מבנים" פרטניים מ"ננו-סרטונים" המציגים את הרנ"א בתצורות שונות, והריצו על כל מבנה כזה ניפוי מדומה. על מנת לבחון את יעילות שיטתם "בעולם האמתי", החוקרים ניסו תחילה את השיטה מול תרכובות שמנגנון קשירתן למולקולת רנ"א מסוימת מנגיף האיידס, הקרויה TAR, כבר ידוע.
"הראנו כי באמצעות ניפוי מדומה של תמונות מרובות של מולקולת ה- TAR, הצלחנו לחזות, ברמת דיוק גבוהה, כיצד תרכובות שונות אלו נקשרות ל- TAR," מציין החוקר הראשי. "אולם, אם היינו מבצעים זאת בשיטה הרגילה של בחינת מבנה יחיד של TAR באמצעות קריסטלוגרפיה או תמ"ג, לא היינו מצליחים לחזות במדויק את צורת הקישור של התרופות הללו."
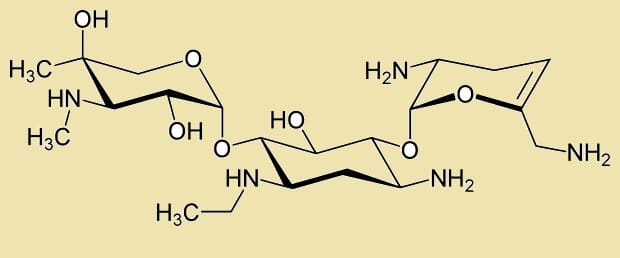
בשלב הבא, אחרי שהוכיחו כי השיטה שלהם יעילה, החוקרים ניסו לגלות בעזרתה תרופות חדשות הפועלות על מולקולת ה- TAR תוך סריקת כחמישים אלף תרכובות קיימות. "מתוך ספריית תרכובות די קטנה זו, הגענו לשש מולקולות קטנות חדשות הנקשרות ל- TAR וחוסמות את הפעילות שלו עם מולקולות אחרות החיוניות לפעילות הנגיף," מסביר החוקר. יתרה מכך, החוקרים גילו כי אחת משש התרכובות הללו (Netilmicin) הפגינה העדפה חזקה למולקולת ה- TAR.
"תרכובת חדשה זו, Netilmicin, נקשרת באופן בררני ל- TAR, ולא למולקולות רנ"א דומות אחרות," מציין אחד מהחוקרים. "היינו מרוצים מאוד מתוצאות אלו מאחר ואחד מהאתגרים הגדולים ביותר בגילוי תרופות הפועלות על רנ"א הוא היכולת לאתר תרכובות הנקשרות למטרת רנ"א ספציפית מבלי להיקשר למולקולות רנ"א אחרות. בררנות גבוהה זו של תרכובת ה- netilmicin מספקת הוכחה ליעילותה של שיטה חדשנית זו," מצין החוקר.
ניסויים נוספים הראו כי עבור שש מולקולות התרופה הפוטנציאליות, השיטה לא רק שחזתה בהצלחה כי הן ייקשרו למולקולת ה- TAR, אלא הצביעה – ברמת דיוק אטומית – על הנקודות שבהן תיקשר התרופה למולקולת הרנ"א.
החוקרים העבירו את שש התרכובות המועמדות לשמש כתרופות לביה"ס לרפואה באוניברסיטת מישיגן על מנת לבדוק את פעילותן הרפואית בתאי T אנושיים הנגועים באיידס. מטרת ניסוי זה הייתה לבדוק אם התרופות יוכלו למנוע מהנגיף לשכפל עותקים שלו – שלב הכרחי בהתפתחות המחלה. "המולקולה netilmicin אכן הצליחה למנוע את שכפולו של הנגיף," מציין החוקר הראשי. "ממצא זה מדגים כי באמצעות מכשיר תמ"ג ומספר מחשבים ניתן לגלות תרופות הפועלות על רנ"א ואשר הינן בעלות פעילות רפואית בתאים אנושיים."

5 תגובות
ל-ר.נ.א (20 ביולי 2011 בשעה 11:21)
עשית סלט.
גם ר.נ.א וגם ד.נ.א הם חומצות גרעין (קרא עוד כאן: http://he.wikipedia.org/wiki/%D7%97%D7%95%D7%9E%D7%A6%D7%AA_%D7%92%D7%A8%D7%A2%D7%99%D7%9F) שמורכבות ממשפחה של מולקולות כימיות קטנות שנקראות בסיסים או נוקלאוטידים (למשל אדנין, גואנין, קרא עוד כאן: http://he.wikipedia.org/wiki/%D7%A0%D7%95%D7%A7%D7%9C%D7%90%D7%95%D7%98%D7%99%D7%93).
חלבונים לעומת זאת מורכבים ממשפחה אחרת של מולקולות כימיות קטנות שנקראות חומצות אמינו (כמו למשל ליזין, טירוזין ואלאנין, קרא עוד כאן: http://he.wikipedia.org/wiki/%D7%97%D7%95%D7%9E%D7%A6%D7%AA_%D7%90%D7%9E%D7%99%D7%A0%D7%95)
ד.נ.א אינו חלבון אלא מולקולה כימית שנושאת את המידע על זהות אנבי הבניין מהן מורכבים החלבונים. התהליך הזה כולל שעתוק (העתקת המידע שמצוי על ה-ד.נ.א) ותרגום (בו מתבצע צימוד בין קטע קצר של המולקולה המועתקת ובין חומצות אמינו שהן אבני הבניין של החלבונים).
לאיציק :
אם RNA עשוי מחומצות הגרעין מהן בנוי ה DNA הרי שגם הוא אמור להיות חלבון – כפי שה DNA הינו חלבון בהגדרתו .
??
כל מולקולה מוגדרת מבחינה מבנית, הבעיה עם מאקרומולקולות (כמו חלבונים ורנ"א) היא שהמבנה שלהם מורכב מאד, וקשה לחיזוי. העובדה שמולקולות אלה מורכבות מאבני בניין מוגדרות מקלה במידה מסוימת על האפשרות לחשב את במבנה המרחבי שלהן.
במקרה של RNA זה קצת יותר מסובך מחלבונים, והרבה יותר מדנ"א, כיוון שזו מולקולה "גמישה" יחסית, המסוגלת ללבוש צורות שונות ללא שינוי במבנה המולקולרי.
עד כמה שאני מבין חלבון עשוי מחומצות אמינו בעוד ש RNA עשוי מחומצות גרעין שמהם עשוי ה DNA
אם אינו סוג חלבון – כיצד מוגדר RNA מבחינה מבנית ?