תרופות רבות המשמשות היום מכילות כחומר פעיל חלבונים קצרים המתפרקים ומורחקים במהירות מהגוף. מדענים מאוניברסיטת מינכן בגרמניה משלבים חלבונים אלו עם חומר מולקולארי דמוי בלון המתנפח בגוף ובכך מאריך את זמן פעילותם הכולל
דר. משה נחמני
תרופות רבות המשמשות היום מכילות כחומר פעיל חלבונים קצרים המתפרקים ומורחקים במהירות מהגוף. מדענים מאוניברסיטת מינכן בגרמניה משלבים חלבונים אלו עם חומר מולקולארי דמוי בלון המתנפח בגוף ובכך מאריך את זמן פעילותם הכולל (הגברת זמן מחצית החיים שלהם בגוף).
אנשים החולים בצהבת בי מטופלים לרוב בהורמון אינטרפרון (interferon). אולם, קיימת מגבלה – אינטרפרון הינו חלבון קטן, המורחק ממחזור הדם דרך הכליות תוך פרק זמן קצר. עבור המטופלים, משמעות הדבר הינה הזרקת מינון גבוה מדי יום ביומו בכדי לשמור על פעילותו של החומר הרפואי.
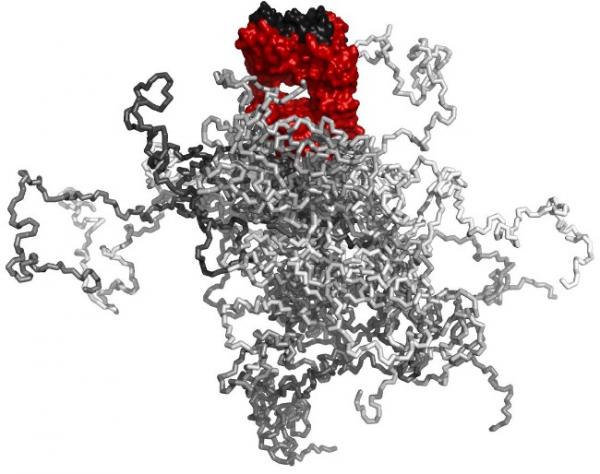
אולם, אינטרפרון נותר בגוף פרק זמן ארוך יותר כאשר הוא מחובר כימית לפרודת פוליאתילן גליקול (PEG, polyethylene glycol). חומר זה הינו שרשרת ארוכה ומפותלת של פולימר המתנפח כאשר הוא סופח מים. בעקבות כך, החומר המשולב הופך נפחי מכדי להיכנס לנקבוביות הזעירות שבכליות – כלומר, האינטרפרון נותר במחזור הדם פרק זמן ארוך יותר, והמטופל צריך לקבל זריקה זו רק פעם בשבוע או בשבועיים.
באמצעות הנדסה גנטית, פרופסורArne Skerra ועמיתיו למחקר מהמחלקה לכימיה ביולוגית באוניברסיטת מינכן, פיתחו עתה שרשרת של חומצת אמינו המתפתלת וסופחת מים, בדומה לפוליאתילן גליקול. אולם, בניגוד לתרכובות פוליאתילן גליקול רבות, אין חשש כי ביו-הפולימר החדש הזה יצטבר בגוף ויסכנו. למעשה, בחלוף הזמן, החומר מפורק או מורחק ביולוגית מהגוף וזאת מאחר ושרשרת חומצות האמינו, הפוליפפטיד, מורכבת משלוש חומצות אמינו טבעיות: פרולין, אלאנין וסרין, או בקיצור PAS.
החומר החלבוני אינטרפרון, המורכב בעצמו מחומצות אמינו טבעיות, יכול בקלות לעבור לצורה החדשה. בניסיונות ראשונים עם בע"ח המדענים קבעו כי האינטרפרון בצורתו החדשה הינו בעל זמן מחצית חיים בגוף שהינו ארוך יותר בפקטור של שישים מהצורה המקורית, מה שיאפשר הרחבה משמעותית של מרווחי המינון במהלך תקופת הטיפול.
יתרון נוסף טמון בפשטות ההפקה הביוטכנולוגית של הצורה החדשה: מקטעי הד.נ.א., הראשון המקודד את רצף חומצות האמינו PAS והשני המקודד את האינטרפרון עצמו, יכולים לחבור יחדיו באופן פשוט, ולאחר מכן, כדוגמא, להיות מופעלים בחיידק. בשלב הבא, החיידק עצמו מייצר את האינטרפרון המחובר ל- PAS בחתיכה אחת, תוך קיצור משמעותי של שלבי הייצור הנדרשים בהשוואה לצימוד הכימי עם PEG. לדברי החוקרים, שיטה זו תוכל להפחית באופן משמעותי את עלויות הייצור.
בעיקרון, כל חלבון קצר המשמש היום ברפואה, או הנמצא בשלבי פיתוח – כדוגמת גורמי צמיחה (growth factors) או קטעי נוגדן פעילים – יכול לעבור את הצימוד הביולוגי הזה בקלות.
החוקרים בטוחים כי לשיטתם החדשה עתיד להיות שוק מסחרי גדול וכי היא תוכל להוביל לפיתוחו של דור חדש לחלוטין של תרופות מצליחות, שחלקן נמצא כבר עכשיו בשלב מתקדם של פיתוח קדם-קליני.

תגובה אחת
תודה רבה על המאמר.