השימוש בנוגדנים חד שבטיים למטרת ביות אנטיגנים המתבטאים בגידול הסרטני הוא כלי יעיל לאבחון וטיפול בסרטן, מחלות אוטו-אימוניות ומחלות דלקתיות
הכותבת: ד"ר אושרת פרנקל ,מנהלת המחקר בחברת אימיון פארמה המפתחת טכנולוגיה של טיפול מבויית לסרטן
השימוש בנוגדנים חד שבטיים למטרת ביות אנטיגנים המתבטאים בגידול הסרטני הוא כלי יעיל לאבחון וטיפול בסרטן, מחלות אוטו-אימוניות ומחלות דלקתיות. כיום כבר ידוע כי יעילות הטיפול בסרטן מוגברת ע"י קומבינציה של נוגדן ותרופה כימותרפוייטית. אך השימוש בתרופות כימותרפוייטיות כרוך בתופעות לוואי שעשויות להגביל את הטיפול וזאת לאור חוסר הספיציפיות של תרופות אלו.
דרך אחת לשיפור היעילות של נוגדנים היא צימוד שלהם למולקולות טוקסין, הפוגעת בשלד התא (microtubule disrupting agents). באוגוסט2011 אישר מנהל התרופות והמזון האמריקאי (FDA) תרופה בשםAdcetris שפותחה ע"י חברת Seattle Geneticsלטיפול בסוגים מסויימים של ליפומה ולמעשה מבוססת על טכנולוגיה זו המכונה צימוד נוגדן-תרופה Antibody Drug Conjugates (ADC) . הטכנולוגיה פורסמה בעיתונות המדעית והפופלארית האמריקאית ובכלל זה ב New York Timesוה- Wall Street Journal כמהפכה בטיפול בחולים ובשוק הפארמצבטי. אולם, השימוש בתרופות כימותרפוייטיות שאינן טוקסינים הפועלות במנגנון פעולה שונה כרגע אינו אפשרי בטכנולוגית ה-ADC. היכולת לצמד מספר קטן בלבד של מולוקולות תרופה לנוגדן וכן חוסר היוכלת להשתמש בקומבינציה של מספר תרופות מהווה מגבלה ליישומים התרפוייטיים של הטכנולוגיה.
בנקודה זו נכנסת לתמונה פלטפורמת ה Nanomabs , פרי פיתוח מחקרי ישראלי. זוהי פלטפורמה להעברה מבוייתת של תרופה לטיפול בסרטן או קומבינציה של תרופות המשמשת בעיקר בטיפול בסרטנים מוצקים, אגרסיביים וקשים לטיפול. העברה מבוקרת של מולקולות התרופה ספיציפית לאיזור הגידול ואף לתוך התא הסרטני נעשית ע"י כליאה של התרופה או הקומבינציה התרופתית בתוך ננוחלקיק פולימרי. החלקיק הזה מבויית כמעין טיל מונחה לתא המטרה הסרטני ע"י אינטראקציה ספיציפית של נוגדן העוטף את החלקיק עם אניטגן המבוטא ביתר בתא הסרטני. לכן מתאפשרת הגברה של היעילות התרופתית בשל הגעה ספיציפית לתוך תא הגידול וכן הפחתה בפרופיל תופעות הלוואי הבעייתי של התרופות כימותרפוייטיות בגלל ירידה בחשיפה של רקמות בריאות למולקלות התרופה הכלואות בתוך החלקיק לפני כניסתן לתא הסרטני. פלטפורמה זו פותחה ע"י צוות בראשותו של פרופסור שמעון בניטה מהמכון למדעי התרופה בבית הספר לרוקחות באוניבסיטה העברית. שותף למחקר בנושא הנוגדנים היה עם ד"ר ז'אן קדוש, סמנכ"ל מחקר וחדשנות בחברת אימיון פארמה.
אם כן מהו בעצם חלקיק הnanomab?
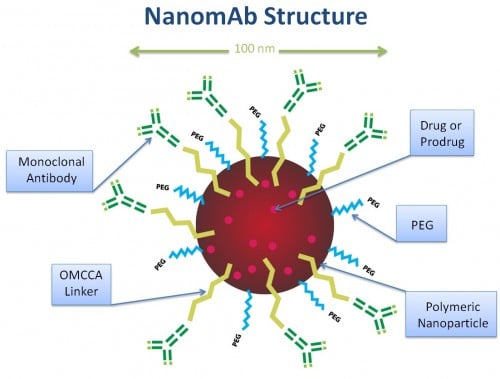
בבסיס הטכנולוגיה חמישה מודולים בסיסיים:
- חלקיק פולימרי שגודלו כ 100 ננומטרים. החלקיק כולא את מטען התרופה המועבר ישירות לתא הסרטני. הפולימרים מהם החלקיק עשוי מתפרקים בתוך התא.
- שכבה מגנה על פני השטח של החלקיק ע"י שייר פולימרי המכונה . PEGשכבה זו הופכת את החלקיק לחמקן מפני תאי מערכת החיסון האחראים לסילוק חומרים זרים לגוף.
- מולקולת המקשרת את הנוגדן לחלקיק הפולימרי.
- תרופה או תרופות נוגדות סרטן. התרופות נכלאות בתוך החלקיק הפולימרי ולמעשה אינן יוצאות ממנו עד לפירוקו של החלקיק בתוך התא. מספר תרופות נוגדות סרטן הפועלות במנגנוני פעולה שונים עברו כליאה בהצלחה בתוך הננוחלקיק. האפשרות למתן של קומבינצית תרופות מרחיב את אפשריות הטיפול.
- נוגדן חד שבטי. עיקר תפקידו של הנוגדן הוא בשימושו למטרות ביות החלקיק לתא הסרטני.
אם כן נשאלת השאלה מהו מנגנון הפעולה ?
המטרה בשימוש ב NanomAbs היא למעשה הגברת הספיציפיות של התרופה לשם שיפור היעילות והבטיחות של הכימותרפיה. השימוש במולקולת לינקר יחודית לשם צימוד של מספר מבוקר של נוגדנים לחלקיק פולימרי חמקני המכיל את התרופה נמצא כיעיל. טכנולוגית ה NanomAbs הראתה שיפור ביעילות העברת תרופה כימותרפוייטית לתוך תא סרטני שלרוב אינו נגיש ברמה מספקת תוך הפחתה באלימינציה של התרופה ע"י איברים כגון הכבד, טחול, כליות. ואכן בהשוואה באפקטיביות של ה NanomAbsהמכילים תרופה כימותרפוייטית טקסול לעומת התרופה הקונבנציונאלית נראה אכן שיפור באפקט נוגד הסרטן גם במודלים של תרביות תאים וגם במודלים של של סרטן הריאה והערמונית בעכבר.
לאחר מתן סיסטמי בזריקה ה NanomAbsמצטברים ברקמה הסרטנית מכיוון שדפנות כלי הדם ברקמת הגידול מחוררות ומאפשרות מעבר של חלקיקים בגודל של כ-100 ננומטרים. הצטברות החלקיקים ברקמה ע"י מעבר כמעין מסננת דרך דפנות כלי הדם מאפשרת אינטראקציה ספיציפית של הנוגדן עם אנטיגן שנמצא על פני התא הסרטני. ניתן לדמות את האינטראקציה בין הנוגדן שעל פני החלקיק לבין האנטיגן שעל פני התא כאינטראקציה של מפתח עם מנעול. הקישור מאפשר כניסה של החלקיק לתוך התא בתהליך שניתן לדמותו לכעין פעולת בליעה של התא (אנדוציטוזה). החלקיק שנבלע עובר עיכול בתוך התא, שלמעשה משחרר את מולקולות התרופה הכלואות בחלקיק באופן מבוקר והן אלו הגורמות לתמותה של התא הסרטני.
היישומים במתן בזריקה של הטכנולוגיה עברו מיסחור באמצעות חברת יישום לחברתPharmaceuticals Immune שנמצאת כרגע בהכנות לקראת ניסויים קליניים. מאחר ונעשתה כבר עבודת מחקר ופיתוח ליצירת פורמולציה אבקתית מיובשת בהקפאה שהראתה יציבות למשך שנתיים, הדרך למסחור יחסית מהיר של התרופה כבר סלולה. החזון של אימיון הוא שבסופו של תהליך פיתוח ואישור קליני, טכנולוגיה זו תפתח אפשריות טיפול חדשות לחולי סרטן תוך שיפור היעילות והבטיחות של הטיפול. בשבוע האחרון הודיעה חברת אימיון על מיזוג עם חברת תרופות אמריקאית הנסחרת בבורסת התרופות מעבר לדלפק (OTC).
פירסומים נוספים
A quantitative evaluation of the molecular binding affinity between a monoclonal antibody conjugated to a nanoparticle and an antigen by surface plasmon resonance.
Debotton N, Zer H, Parnes M, Harush-Frenkel O, Kadouche J, Benita S.
Eur J Pharm Biopharm. 2010 Feb;74(2):148-56. Epub 2009 Oct 14.
http://www.ncbi.nlm.nih.gov/pubmed/19835957
Overcoming the formulation obstacles towards targeted chemotherapy: in vitro and in vivo evaluation of cytotoxic drug loaded immunonanoparticles.
Debotton N, Parnes M, Kadouche J, Benita S.
J Control Release. 2008 May 8;127(3):219-30. Epub 2008 Feb 8.
http://www.ncbi.nlm.nih.gov/pubmed/18343522
The design and evaluation of a novel targeted drug delivery system using cationic emulsion-antibody conjugates.
Goldstein D, Nassar T, Lambert G, Kadouche J, Benita S.
J Control Release. 2005 Nov 28;108(2-3):418-32. Epub 2005 Oct 13.
http://www.ncbi.nlm.nih.gov/pubmed/16226821
The ligand nanoparticle conjugation approach for targeted cancer therapy.
Karra N, Benita S.
Curr Drug Metab. 2012 Jan; 13 (1): 22-41 21892918
http://lib.bioinfo.pl/auid:18550854

5 תגובות
אני שי
ממליץ לחפש בגוגל: ננו צוללות.
ישנם כמה מאמרים מאד מעניינים, חלקם מאתר זה.
זה כנראה ביות (HOMEING) ולא בייות … הודעה לעיתונות מקצועית שתורגמה בעזרת גוגל… שאלוהים יעזור להם 🙂
נהניתי לקרוא אבל זה בעיקר בגלל שאני עוסק בתחום ואוצר המילים מוכר. אם את רוצה לפנות לקהל קוראים רחב יותר הייתי ממליץ לתת את הטקסט לביקורת לתיכוניסט סקרן וחובב מדע.
איזה שימוש מדהים בננו טכנולוגיה 🙂
ממש מקסים לפתוח את הבוקר לידיעה כזאת, על התקדמות ביעילות בטיפול בסרטן.