תאי גזע מושרים (induced pluripotent stem cells, iPS) מיוצרים במעבדה מתאי גוף נורמליים ע"י שימוש בפקטורים ידועים, הגורמים לתאים בוגרים לחזור אחורה בהתפתחות, למצב של תאי גזע עובריים (תהליך המכונה reprogramming). ניתן לבצע תהליך זה על תאים שמקורם בחולה, ולנצל זאת למחקר של מחלתו. במקרה זה הפיקו החוקרים תאי גזע מושרים מחולי ALS, מחלה נוירולוגית ניוונית קשה וחשוכת מרפא. הם השתמשו בתאים אלה לחקר התפתחות המחלה, ואף מצאו שחומר מסוים, חומצה אנאקרדית, עשוי להוביל לתיקונם של מאפייני מחלה שונים בתאים אלה. השימוש בתאי גזע עובריים מושרים שמקורם בחולים עשוי לקדם משמעותית את המחקר הרפואי של מחלות רבות.
אז מה זה בדיוק תאי גזע מושרים (תאי iPS)? כל התאים בגופנו מקורם בתאי גזע עובריים (embryonic stem cells, ESCs). ניתן להפיק תאי גזע עובריים מעוברים בני מספר ימים (בסביבות שבוע לאחר ההפריה). עם פרוטוקולים מתאימים, ניתן בעיקרון למיין תאים אלה במעבדה לכל סוג של תא: תא שריר, תא עצב, תא כבד, תאי דם שונים, וכן הלאה.
ברמת העיקרון, לאחר שתא גזע עוברי התמיין למצבו הסופי (תא עצב נניח), אין לו כבר דרך חזרה – לא לתאי מוצא של אותו תא עצב, ובוודאי שלא לתא גזע עוברי. היוצאים מהכלל של עיקרון זה הם תאי המוצא לתאי המין (תאי זרע וביצית). אולם, עיקרון זה לא מנע מחוקרים לנסות ולבצע תהליך שכזה, כלומר הפיכת תא בוגר ממוין לתא גזע עוברי, תהליך המכונה תיכנות מחדש (reprogramming). ואכן, ב-2006 הושגה פריצת הדרך: חוקרים יפנים לקחו פיברובלסטים מעכברים (תאים בוגרים בשלב התמיינותי מתקדם, הנמצאים ברקמות חיבור), ובאמצעות ביטוים של ארבעה גנים מוגדרים הצליחו לעשות להם תיכנות מחדש לקבלת תאי גזע (עובריים) מושרים.
תאים אלה דומים בתכונותיהם לתאי הגזע העובריים הטבעיים:
1. ניתן למיינם בעיקרון לכל סוגי התאים בגופנו. תאי גזע מושרים מוינו במעבדות שונות לסוגי תאים רבים: למשל לתאי דם שונים, לתאי עצב, ואפילו לתאי שריר לב המייצרים פעימות. תאי גזע מושרים שימשו גם ליצירת עכברים שלמים שמקורם בתאים אלה.
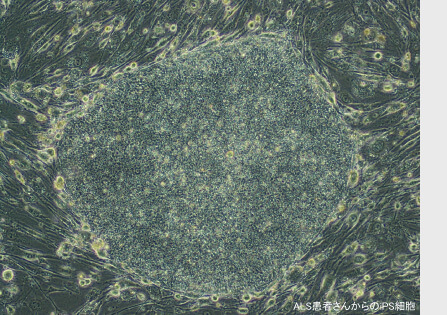
2. אל-מוות (immortality): תאי גזע עובריים, טבעיים או מושרים, יכולים להמשיך ולגדול בתרבית לנצח. זאת בניגוד לתאים בוגרים ממוינים, אשר מספר החלוקות שהם יכולים לבצע בתרבית מוגבל, ולכן גם השימוש בהם למחקר מוגבל יותר. קצב החלוקה של תאים אלה מהיר ביותר, ובניגוד לרוב התאים אשר גדלים בצלחת בשכבה אחת (גדילה דו-ממדית), תאי גזע עובריים (טבעיים או מושרים) יוצרים בצלחת מושבות תלת מימדיות של תאים קטנים וצפופים.
3. ביטוי של גנים שונים המאפיינים תאי גזע עובריים.
4. סמנים אפיגנטיים שונים (מודיפקציות בדנ"א או בחלבונים שעליהם הדנ"א ארוז בתאים), המאפיינים תאי גזע עובריים.
לתאי הגזע המושרים שימושים פוטנציאליים ויתרונות רבים. הם עשויים להחליף את השימוש בתאי גזע עובריים טבעיים גם ברפואה וגם במחקר, ולפתור בכך בעיות רפואיות, מחקריות, אתיות ובירוקרטיות רבות. לדוגמה, ברפואה, ניתן להשתמש בתאי גזע מושרים שמקורם בחולה עצמו על-מנת להתגבר על הצורך בהתאמת רקמות. הדגמה מעשית לכך בעכברים הושגה כבר ב-2007, כשנה אחת בלבד לאחר פרסום השיטה להפקת תאי גזע מושרים.
החוקרים (שכללו את החוקר הישראלי יעקוב חנא, כיום במכון ויצמן) הצליחו לרפא עכברי מודל החולים במחלה הגנטית אנמיה חרמשית, ע"י שימוש בתאי גזע מושרים. הם לקחו תאים ממוינים (פיברובלסטים) מהעכברים הבוגרים, עשו להם תהליך של תיכנות מחדש לתאי גזע מושרים, ובנוסף השתמשו בשיטות של הנדסה גנטית לתיקון הגן הפגום. את התאים המתוקנים הם מיינו לכיוון של יצירת תאי גזע של מערכת הדם (hematopoietic stem cells, HSCs, הנמצאים במח העצם). תאים אלה הושתלו בעכברים החולים, ויצרו מערכת דם חדשה ותקינה, ללא המוטציה שהביאה למחלה. התקווה היא שבצורה דומה ניתן יהיה בעתיד לרפא גם בני-אדם החולים במחלות דם גנטיות, לוקימיה, מחלות נוירולוגיות שונות, ועוד. בכדי להגיע לכך שתאי גזע מושרים ישמשו גם לריפוי בני אדם יש צורך לפתור עדיין לא מעט סוגיות, ובראשן בעיית בטיחות השימוש בהם, בעיקר בהקשר של מניעת היווצרות סרטן שמקורו בתאים אלה.
בנוסף לשימושים הרפואיים, תאי גזע מושרים עשויים להוות כלי מרכזי גם במחקר המדעי. חזון זה הולך ומתממש. בהקשר זה ישנם שני היבטים מרכזיים. הראשון הוא שימוש בתאי גזע מושרים במחקר כתחליף לתאי גזע עובריים טבעיים. כעקרון, שימוש בתאי גזע עובריים טבעיים ו"אמיתיים" (ESCs) עדיף למחקר על-פני תאי גזע מושרים (תאי iPS). אולם, השגת תאי גזע עובריים מאדם כרוך בבעיות אתיות ובירוקרטיות שונות, בעיקר משום שמפיקים אותם מעוברים כאמור, למשל כאשר יש עודף של ביציות מופרות במהלך הפריית מבחנה.
ההיבט השני הוא שימוש בתאי גזע מושרים למחקר של מחלות שונות, כפי שעשו החוקרים במקרה זה, בראשותו של הרואיסה אינו (Haruhisa Inoue) מאוניברסיטת קיוטו שביפן. הם לקחו תאים בוגרים ממוינים משלושה חולי ALS, בעלי מוטציה בגן TDP-43, ועשו להם תיכנות מחדש ליצירת תאי גזע מושרים. עד כה התגלו בסה"כ כ-14 גנים אשר מוטציות בהם עשויות לגרום ל-ALS, מחלה ניוונית קשה, הפוגעת בתאי עצב מוטוריים (שאחראים לתנועת שרירים), ומביאה לשיתוק הולך ומחמיר, ובד"כ גם למוות בתוך מספר שנים. את תאי הגזע המושרים, המכילים את המוטציה הרלוונטית מהחולים, מיינו אח"כ החוקרים לכיוון של יצירת תאי עצב מוטוריים, התאים שנפגעים כאמור ב-ALS. הם הבחינו שתאים אלה אכן מבטאים מגוון של תופעות המאפיינות תאי עצב של חולי ALS, כגון שלוחות עצביות קצרות יותר, צברים (אגרגטים) של חלבונים בתאים, ועוד.
המחקר בתאים אלה הניב מספר תוצאות מעניינות – למשל, זיהוי של חלבון מסוים (SNRPB2) אשר נקשר לחלבון ה-TDP-43 המוטנטי במהלך יצירת האגרגטים הנ"ל, או זיהוי של גנים רבים אשר ביטוים משתנה במהלך התפתחות המחלה. בנוסף, הם השתמשו בתאי הגזע המושרים לסריקה (screening) של מספר חומרים, בתקווה שאחד מהם יציל את התאים מאותן תופעות האופייניות לתאי ALS. ואכן, שימוש באחד החומרים בסריקה, ששמו חומצה אנאקרדית (anacardic acid), הציל את התאים נושאי הגן הפגום מהתופעות הנ"ל. המשך מחקר במודלים עכבריים יראה האם טיפול זה עשוי להיות יעיל גם בחיה השלמה (in vivo), ולא רק בתאים בתרבית (in-vitro).
תהליך דומה נעשה גם עבור מחלות אחרות, כגון מחלת האלצהיימר, פרקינסון, הנטינגטון, ווילסון, ועוד. הרעיון הכללי בכל המקרים האלה דומה: שימוש בתאים כלשהם מהחולה (בד"כ פיברובלסטים מהעור) להפקת תאי גזע מושרים המכילים את המוטציה הרלוונטית, ולאחר מכן לגרום להתמיינות של התאים ליצירת סוג התאים שנפגע במחלה. תאים אלה, כלומר התאים הממויינים שמכילים את המוטציה, יכולים להוות בסיס חשוב למחקר של המחלה הרלוונטית ולמציאת תרופות פוטנציאליות.
כתבה על המחקר באתר sciencedaily
תקציר המאמר- שימוש בתאי גזע מושרים מחולי ALS למציאת תרופה פוטנציאלית
תקציר המאמר מ-2006 שבו תיארו לראשונה יצירת תאי גזע מושרים
תקציר המאמר מ-2007 של ריפוי אנמיה חרמשית בעכברים בעזרת תאי גזע מושרים

תגובה אחת
האם זה יכול להועיל לנשאי rp?