הדפסת איברים חליפיים בדרך שתאפשר השתלתם בגוף של אדם ושישתלבו בפעולתו

בגיל עשר עמדו בפני לוק שתי אפשרויות שילדים אינן נאלצים לבחור ביניהן בדרך-כלל: השתלת כליה, או חיים קצרים עם ביקורים תכופים בבית-החולים כדי לטפל בכליותיו הכושלות. הוריו בחרו באפשרות השלישית: ניתוח יוצא-דופן ונסיוני. פרופ' אנתוני אטלה מאוניברסיטת ווייק פורסט אסף תאים משלפוחית השתן של לוק וגידל אותם במעבדה בסבלנות ובאהבה. ביחד עם צוות המחקר שלו הוא יצר עבורם פיגום: כדור מפולימר סינתטי בצורת שלפוחית חדשה. החוקרים ציפו את השלפוחית הסינתטית בתאי שריר מבחוץ ובתאים המחפים את שלפוחית השתן הטבעית מבפנים. הם צפו לאורך שבועות באיבר הטבעי-מלאכותי בזמן ששהה בביו-ריאקטור במעבדה, וידעו שהתאים מתרבים ונופחים בו חיים אמיתיים. לבסוף הם השתילו אותו בגופו של לוק הצעיר[1].
הילד זכה מחדש בחייו.
כיום, לוק עדיין נהנה מבריאות טובה. הטיפול המהפכני בזמנו – יצירת איבר חלופי שלם – הצליח במלואו[2].
מה אם היינו יכולים לעשות זאת לאיברים נוספים בגוף?
את התשובה – לפחות, תשובה אפשרית אחת – סיפק לי פרופסור נחשב לרפואה לפני עשור. אותו פרופסור התנבא בפניי כי לא רחוק היום בו נוכל להחליף את איברי הגוף, איבר-אחר-איבר.
"הלב התקלקל?" אמר, "נחליף אותו. הכליות התקלקלו? גם אותן. אתה לא מרוצה ממצב העור שלך? גם בו אפשר יהיה לטפל."
התוצאה של מצב זה תהיה, לדעתו, עצירת ההזדקנות מכל בחינה מעשית. אפשר להתווכח על הפרטים הקטנים בחזון, אבל ברור שכאשר נוכל להחליף כל רקמה בגוף, רבות מהמחלות המטרידות אותנו כיום ייראו בעינינו בעתיד כזוטות הניתנות לטיפול. זוטות לא-נעימות, אולי, אבל כפי שאנו הולכים כיום לרופא השיניים ומוכנים לסבול למען הבריאות, כך נהיה מוכנים באותו עתיד ללכת גם ל- 'מהנדס הרקמות' בבית-החולים כדי להאריך את משך חיינו הבריאים בעוד עשור-או-שניים.
ובכן, חזון הוא עניין טוב ויפה, אבל לא משלמים איתו במכולת. נשאלת השאלה, לפיכך, עד כמה אנו יכולים למצוא כיום חלופות לרקמות ולאיברים, מהם האתגרים הגדולים בתחום – ומתי באמת נגיע לארץ המובטחת של בריאות אין-קץ.
נתחיל בחלופות הפחות-מרשימות במבט ראשון: האיברים החלופיים הדוממים.
ריקרד נורמק היה קרוב לגיל העמידה כשאיבד את זרועו בתאונת עבודה. הוא קיבל פרותזה – זרוע תותבת – מסורתית. אותה זרוע, שהייתה כרטיס הכניסה שלו לעולם האיברים החלופיים, התחברה לאזור הגדם בעזרת שרוול שהיה אמור להיות מותאם לו אישית.
זו, לפחות, ההבטחה. המציאות פחות נעימה: קשה למצוא דרך נוחה לחבר את האיברים התותבים לגוף, ונורמק לא הצליח להתרגל לפרותזה החדשה[3]. הוא לא הפעיל אותה היטב. היא הייתה, בפשטות, איבר מת.
מבחינה זו, סיפורו של נורמק דומה לחוויותיהם של רבים הנאלצים להחליף את זרועותיהם הביולוגיות-המקוריות באיבר פלסטי-מתכתי. רוב פרותזות הזרוע כיום פשוטות באופיין. הפשוטות ביותר מזכירות קרס מוארך המסוגל להיסגר באמצעות הנעת המרפק או הכתף באופן שגורמת לרצועות שבפרותזה להימתח. המשוכללות יותר מסוגלות לקבל אותות חשמליים המגיעים בדרך-כלל מהעצבים באזור החזה, ומתרגמות את האותות העצביים הללו להנעת המפרקים ו- 'השרירים' המלאכותיים. אלו גם אלו סובלות מאותן בעיות: קשה להלביש אותן על הגוף, קשה לשלוט בהן וקשה להעביר משוב בחזרה לעצבים, כך שהמשתמש בהן יזכה שוב בתחושה בידו ובאצבעותיו.
לאחר התלבטות, החליט נורמק לקבל סוג חדש של פרותזה: כזה שהופך לחלק מהגוף לכל דבר ועניין. הפרותזה הרובוטית חוברה לגופו בתהליך של אוסאו-אינטגרציה: שתל מתכתי – בדרך-כלל מטיטניום – הוחדר לתוך העצם, ותאי העצם עודדו לנדוד לתוך המתכת המחוררת ולמלא אותה ברקמת עצם בריאה. במילים אחרות, העצם והמתכת – החי והדומם – השתלבו ביחד בטבעיות[4].
הפרותזה שקיבל נורמק לא השתלבה רק עם העצם, אלא גם עם העצבים והשרירים. אלקטרודות חכמות הותאמו לעצבים המתאימים, ואלגוריתמים מתוחכמים תרגמו את המסרים להוראות שיעברו לזרוע הרובוטית, לכף היד ולאצבעות. המידע זרם בשני הכיוונים: כאשר האצבעות הרובוטיות נגעו בתפוח, למשל, הועבר מיד אות חשמלי בחזרה לחיישנים הממוקמים מסביב לעצבים. העצבים שלחו את המידע בחזרה למוח, וכך יכול היה נורמק ליהנות גם מחוש מגע של ממש[5].
"אני בדרך-כלל אומר שעם פרותזת-שרוול מסורתית, אתה עונד את הפרותזה – זה מכשיר רפואי. אבל עם אוסאואינטגרציה, המכשיר הרפואי הופך לחלק ממך. אתה לא מרגיש שאתה עונד את הפרותזה. במקום זאת, היא חלק ממך." אמר.
סיפורו של ריקרד נורמק מלמד אותנו מספר לקחים. ראשית, הוא מבהיר שאיננו יכולים להתייחס אוטומטית לאיברים חלופיים כאילו הם ביולוגיים בלבד. בדומה ליריעת הפולימר הסינתטי עליה השתיל אנתוני אטלה את תאי שלפוחית השתן של לוק, כך גם זרועו של נורמק הפכה לשילוב של הביולוגי לצד חומרים שאינם קיימים באופן טבעי בגוף. אנו נרתעים באופן אוטומטי משילובים כאלו – שנראים בעיני רבים כמפלצתיים ולא-טבעיים – אבל אי-אפשר להתכחש לתועלת העצומה שהם מביאים לבעליהם.
הלקח החשוב השני הוא שפרותזות אינן חייבות להמשיך להיראות כאילו הן האיבר המקורי. סרטונים שמראים את הפרותזה של נורמק חושפים את נקודת החיבור שלה עם הזרוע – מראה מעורר חלחלה. אבל שוב, גם כאן, דווקא הנכונות להתעלם מצורתו המקורית של האיבר, יכולה לעזור למקבל הפרותזה.
אנחנו רואים כאן את ההמשך של תנועה שנפתחה בסוף שנות השבעים, כאשר ואן פיליפס – סטודנט צעיר – עבר תאונה שהסתיימה בכריתת רגל מתחת לברך. הפרותזות שהותאמו לו היו כל-כך לא-מספקות, שהוא עבר להנדסה ביו-רפואית ופיתח פרותזות שהיו יותר שימושיות מייצוגיות. זו הייתה התקופה בה הנדסת החומרים זינקה קדימה, וחומרים חזקים וקלים מתעשיית התעופה החלו למצוא דרכם גם לפרותזות. פיליפס פיתח את ה- Flex-Foot, שצאצאיה הרוחניים מאפשרים לרצים באולימפיאדת הנכים להגיע למהירויות המתחרות באלו של אצנים ללא-מוגבלות[6]. הפרותזות האלו אינן נראות כמו רגליים, אבל הן מקנות למשתמש בהן כוחות-על מתונים.
כיום נראה שאנשים מתביישים פחות באיברים החלופיים שלהם. אפשר למצוא באינטרנט תמונות של זרועות ורגליים פרותטיות משובצות ביהלומים, בצבע ורוד בוהק, עם טפרי-וולברין, ועוד שפע של המצאות בסגנון סייבר-פאנק. מעצבים רק מתחילים לחקור את מרחבי היופי והצורה האפשריים של האיברים החלופיים, ויהיה מרתק לראות לאן הם יקחו אותנו.
ללקח השני הזה יש משמעות חשובה גם עבור איברים פנימיים: אנחנו לא חייבים לשחזר אותם בדיוק בדרך בה הם התקיימו במקור.
קחו, למשל, את הלבלב. האיבר המורכב הזה מסוגל לחוש את רמות הגלוקוז – הסוכר – בדם, ולהפריש אינסולין שיביא להורדת רמת הסוכר בדם. מהנדסים ביו-רפואיים עמלו בפרך שנים ארוכות כדי ליצור לבלב מלאכותי שיוכל לבצע את כל המטלות הללו. למעשה, הם עדיין מנסים. אבל אפשר גם אחרת: לבלב מלאכותי מודולרי, כלומר כזה המפורק לחלקים שונים. חיישן גלוקוז מחובר כל-העת לעור, ובוחן את רמות הסוכר בדם. המידע מועבר לבינה מלאכותית שמחליטה האם יש צורך בהזרקת אינסולין וקובעת את המינונים הנדרשים. אחרון חביב, משאבה מפמפמת את האינסולין לתוך הגוף דרך מחט זעירה.
כל אחד מהחלקים האלו ממוקם במקום אחר על הגוף. זהו אינו "לבלב" כפי שאנו מכירים אותו, אבל כשהם פועלים ביחד – הם ממלאים את מקומו של הלבלב הביולוגי. המטרה הסופית היא החשובה, לא הדרך להשגתה.
הלקח הזה פותח עבורנו צוהר גם לדמיונות מוזרים ומרהיבים של עתיד האיברים החלופיים. אולי, במקום לב אחד-ויחיד, נוכל למקם מספר משאבות מלאכותיות בכמה מקומות בגוף, שביחד ימלאו את אותו תפקיד של הלב ויזרימו את הדם ברחבי הגוף? אולי הפתרון לכבד חלופי אינו כבד ביולוגי אחד, אלא סדרה של מסננים המנטרלים רעלים ומפרקים מזהמים?
אולי. אולי לא. רק חשוב להבין שבתחום הנדסת הרקמות והאיברים, איננו חייבים להיות מוגבלים 'למוצר הקיים'.
הלקח השלישי מסיפורו של נורמק הוא שהטכנולוגיות של היום הגיעו לרמה בה הן יכולות להתממשק עם המוח ועם העצבים. יש לכך משמעויות גדולות לעתיד, בהן ניגע בחלק האחרון של המאמר. בינתיים, נחזור לקרקע המציאות ונבחן סוג אחר של חלופות לאיברים: חלופות ביולוגיות.
נדבר לרגע במספרים. בארצות הברית בלבד, מחכים כיום 106,075 בני-אדם להשתלת איברים. חלק מתוכם לעולם לא יקבלו את האיברים להם הם זקוקים, מכיוון שתורמים חיים מספקים רק 6,000 איברים בשנה, בממוצע. מדי יום מתים 17 אנשים בממוצע בעודם ממתינים להשתלת איברים. מדי תשע דקות, מתווסף אדם חדש לרשימת ההמתנה. בקיצור, הסטטיסטיקה אינה לטובת הממתינים לקבלת איבר-מן-החי.
קיימות שלוש שיטות מרכזיות כיום ליצירת איברים חלופיים: דה-סלולריזציה, יצירת אורגנואידים, והדפסה בתלת-ממד. לכל אחת מהן יש את היתרונות והחסרונות שלה, אבל דבר אחד משותף לכולן: יש להן עוד הרבה מקום לשיפור.
נתחיל בדה-סלולריזציה.
אנו נוהגים לחשוב שהגוף מורכב מתאים – וזה נכון, אבל חלקית. למעשה, התאים מפרישים מסביב לעצמם רקמה המכונה "מטריקס חוץ-תאי", ובתוכה הם יושבים. המטריקס תומך בהם, מייצב אותם ואפילו 'מתקשר' איתם ומעביר להם הוראות כימיות שתאים אחרים מפרישים לתוכו. בלי המטריקס החוץ-תאי, התאים בגופנו לא היו מסוגלים לפעול או לשרוד.
שיטות של דה-סלולריזציה – סילוק תאים – מסתמכות על המטריקס החוץ-תאי כבסיס לרקמה. בשלב הראשון נשטפת הרקמה ומנוקה מכל תאיה. מה שנשאר מאחור הוא המטריקס הנקי: מבנה שנראה כמו האיבר המקורי, אבל נטול צבע וחיים. הסיבה שהמבנה הריק הזה יקר-ערך כל-כך היא שהוא מכיל את כל החלבונים וגורמי הגדילה – כל ההוראות הכימיות – שתאים חדשים יוכלו להסתמך עליהם כדי לאכלס מחדש את הרקמה. לא רק זאת, אלא שהוא גם מעוצב בדיוק בצורה הנכונה: לב, כבד, עצם או כל איבר אחר.
שיטת הדה-סלולריזציה נמצאת כיום בשימוש במקרים מסוימים, כמו ברה-קונסטרוקציה של שד. מטריקסים שנוקו מתאיהם מושתלים בשדיים, ומושכים בהצלחה רבה את התאים המרכיבים את כלי-הדם בגוף, כך שאלו מחלחלים לתוך המטריקס וממלאים אותו בכלי-דם. לאחר מכן מוזרקים לתוך המטריקסים גם תאים המתחלקים ומתפתחים לתאי שומן[7].
לצערי, לא מוכר לי מקרה של החלפת איבר שלם ומורכב באדם, במטריקס שעבר דה-סלולריזציה. באחד המחקרים המתקדמים ביותר בחזירים, קיבלו אלו לב של חזיר אחר שנוקה מתאיו. הם הצליחו לשרוד שלושה ימים, לפני שהלבבות נקצרו לבחינה מדוקדקת תחת עדשת המיקרוסקופ. ברור שעבור בני-אדם אנו מעוניינים בהצלחה ארוכת-טווח יותר[8].
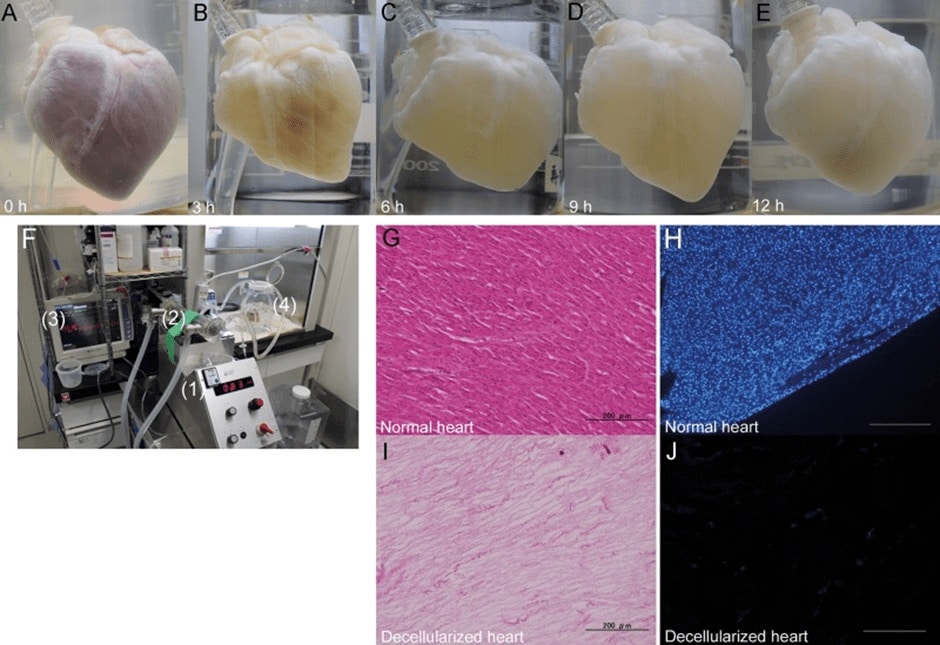
בעיה אחרת עם דה-סלולריזציה היא שהשיטה עדיין מחייבת הסתמכות על איברים המגיעים מבני-אדם. אפשר באופן תיאורטי להשתמש במטריקסים ממקור חייתי, אבל ברור שאלו לא יהיו מוצלחים כמטריקסים אנושיים.
אורגנואידים
באמצע 2021 הופיעה ידיעה מוזרה בעיתונות הבינלאומית: "מיני-מוחות במעבדה הצמיחו זוגות עיניים משלהם". זו אחת מאותן ידיעות שהייתם מצפים לראות בסיפורי מדע-בדיוני, אבל היא עכשווית בהחלט. אותם 'מיני-מוחות' הינם האורגנואידים.
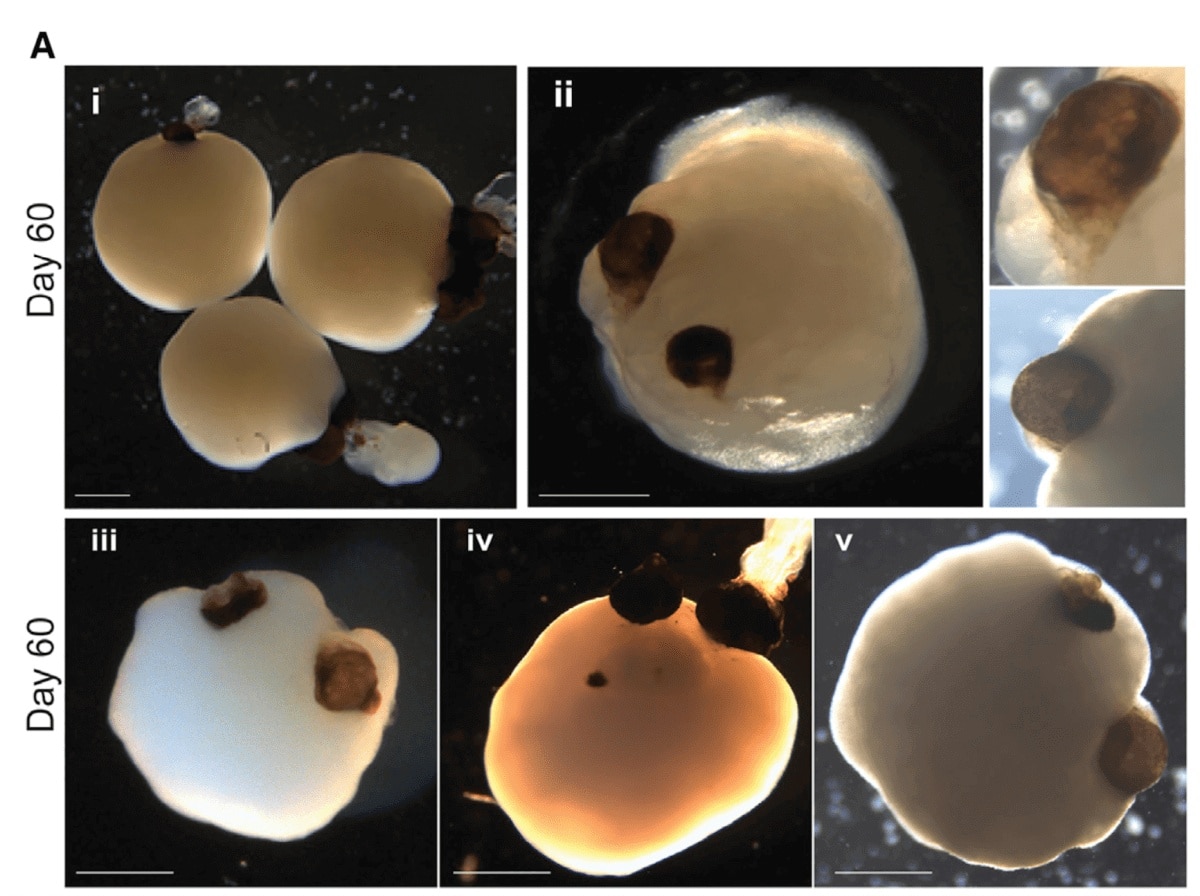
כדי להסביר מאין מגיעים אורגנואידים, אנחנו צריכים קודם להכיר את תאי הגזע: סוג של תאים קדומים המסוגלים להתמיין לסוגים שונים ורבים של תאי-גוף. העובר האנושי, בשלבי ההתפתחות המוקדמים ביותר שלו, מורכב מתאי גזע שכאלו. התאים הללו מקבלים הנחיות שונות בגוף העובר, ובהתאם לכך מתמיינים לרקמות שונות: רקמת מוח, רקמת כבד, רקמת עצם וכל היתר.
מה יקרה אם ניקח תאי גזע, נשים אותם בצלחת הפטרי ונעביר להם הוראות ליצור רקמה מסוימת? הם ייצרו "אורגנואיד" – מיני-רקמה שמחקה את הרקמות והאיברים שבגוף האנושי.
באותה ידיעה על מיני-מוחות שהצמיחו עיניים חדשות, האורגנואידים קיבלו הנחיות מהחוקרים להתמיין וליצור תאי-עצבים ומבנים מוחיים. באופן טבעי, הגדילה המשיכה ליצירת העצבים המובילים לעיניים, וה- Optic cups – מבנים בסיסיים שאמורים להצמיח את הרשתית – הופיעו תוך שלושים ימים והתבגרו עד ליום החמישים. זהו גם משך הזמן המשוערך להתפתחות דומה בעובר האנושי. האורגנואידים גם המשיכו ופיתחו עדשות ואת רקמת הקרנית[10].
האם המשמעות היא שבקרוב נוכל להשתיל עיניים ביולוגיות, שיפותחו על-גבי אורגנואיד?
לרוע המזל, לא מסתמן שזה המצב. האורגנואיד הוא חיקוי בלבד של האיבר המקורי. הוא אמנם זהה במבנה הפנימי שלו למבנה של האיבר האמיתי, אבל הוא אינו מתאים להשתלה או לחיבור עם גוף אנושי. תמיד קיים גם החשש שתאי הגזע יצאו משליטה בגוף המושתל, וייצרו גידול סרטני קטלני. מסיבות אלו, האורגנואידים אינם משמשים עדיין להחלפת איברים בתוך הגוף. השימוש המעניין ביותר בהם הוא דווקא להחלפת איברים מחוץ לגוף: חוקרים בוחנים עליהם מגוון של חומרים תרפוטיים, מתוך הנחה שאם החומרים הללו מזיקים לאורגנואידים, הרי שהם יסבו נזק גם לאיבר האמיתי בתוך הגוף.
המשמעות היא שבהחלט יש שימוש באורגנואידים. כאיברים חלופיים מחוץ לגוף, הם עוזרים להאיץ את קצב התקדמות מדע הרפואה. אבל בתחום הקליני, למרבה הצער, עדיין אין התקדמות ממש.
הדפסת רקמות
וכך אנו מגיעים סוף-סוף לשיטה המבטיחה והמעניינת ביותר – או לפחות זו שזוכה לכותרות הגדולות והתכופות ביותר בעיתונים. זוהי, כמובן, הדפסת רקמות בתלת-ממד.
תהליך ההדפסה בתלת ממד מתחיל לרוב בקצירת תאיו של החולה עצמו. הרופאים מבצעים ביופסיה קטנה באמצעות מחט, או ניתוח פולשני מזערי. כל זה כדי להשיג חתיכה קטנה של רקמה, ממנה אפשר להסיר את התאים ולגדל אותם מחוץ לגוף. התאים מבלים את הימים והשבועות הבאים בביו-ריאקטורים, בהם הם נהנים מסביבה דומה לזו שבגוף, כולל טמפרטורה, רמת חמצון, מזון – ואפילו מחזוריות יום-לילה ופעילות גופנית, בחלק מהמחקרים.
קיימות מספר שיטות הדפסה שונות, אבל אחת מהנפוצות ביותר היא זו בה התאים מודפסים ישירות ביחד עם המטריקס ממנו תיבנה הרקמה. כאשר ישנם מספיק תאים בביו-ריאקטורים, הם מעורבבים עם חומר ההדפסה – שהוא בעצם גרסה ראשונית של המטריקס החוץ-תאי. אותו מטריקס מועשר מראש בגורמי גדילה – כלומר, הוראות כימיות – שעוזרות לתאים להבין מה עליהם לעשות באותו אזור. המטריקס-להדפסה מורכב לרוב מחומרים כמו ג'לטין וקולגן, שאינם פוגעים בגוף או בתאים.
התאים והביו-דיו מועברים למדפסת תלת-ממד, שמזריקה אותם באזורים הנכונים. אם רוצים ליצור רקמה מורכבת – למשל, לב – אזי יהיו מספר ראשי הדפסה שכל אחד מהם ידפיס תאים שונים עם מטריקס שונה-במקצת עבור כל סוג תא. כפי שמדפסת רגילה מסוגלת להדפיס במספר צבעים באמצעות מספר ראשי הדפסה או כמה מחסניות-צבע שונות, כך גם מדפסת התלת-ממד מדפיסה סוגים שונים של רקמות, כל אחת במקומה הנכון באיבר.
כל תהליך ההדפסה אינו אמור לקחת יותר ממספר שעות, והמבנה הסופי אמור להיות דומה מאד לזה של האיבר הנחשק. באופן תיאורטי אפשר אפילו להתאים אותו בגודל ובצורה, בהסתמך על מידע שמגיע מצילומי רנטגן וסריקות של האיבר המקורי של המטופל.
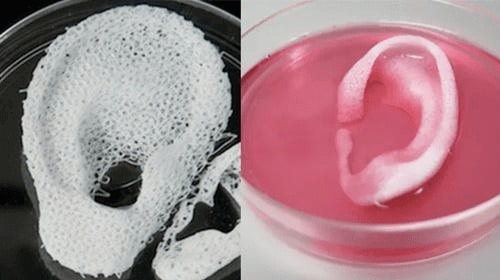
נותרה רק בעיה אחת: כל האיבר המרשים שהודפס, מתחיל להיהרס עוד בזמן ההדפסה. הסיבה היא שתאים זקוקים לחמצן ולחומרי מזון, ואלו אינם יכולים לחלחל בקלות דרך רקמה צפופה. לכן יש צורך בכלי-דם שמרווים את הרקמה בחמצן. המדפסות המתקדמות ביותר אמורות להדפיס גם את כלי הדם, אבל אלו עדיין אינם מתפקדים בקלות או היטב, ויש צורך לחבר אותם לכלי-דם קיימים ולהזרים דרכם חמצן באופן אקטיבי. המשמעות היא שברגע שהרקמה המודפסת מגיעה לעובי מסוים, התאים שבעומקה מפסיקים לקבל חמצן – ומתחילים למות.
מה עושים? נושכים שפתיים ומשתילים. מנסים להעביר לתאים בעומק-הרקמה חמצן ככל האפשר כדי לשמר אותם בחיים, ומשתילים את הרקמה בהקדם האפשרי כדי לתת לגוף לעשות את מה שהוא יודע. התקווה היא שלאחר ההשתלה, כלי-הדם הקיימים מסביב לאזור יישלחו שלוחות לתוך הרקמה החדשה ויזרימו חמצן ודם חדש לתוכה. דגש על "תקווה", מכיוון שזהו אתגר שטרם נפתר.
כך או כך, לאחר ההשתלה מתחיל המטריקס המלאכותי להתפרק ולהתפורר, בדיוק כפי שאנו רוצים שיקרה. הוא עשה את שלו, סיפק לתאים נקודת אחיזה ואת ההנחיות הראשוניות להן הם היו זקוקים כדי להישאר בחיים – ועכשיו הוא מתחלף לאיטו במטריקס חדש שהתאים מפרישים בעצמם.
זה, בקיצור נמרץ, הוא תהליך הדפסת הרקמות בתלת-ממד. מדובר בפרוצדורה עתידנית-כמעט, שכבר הוכיחה את עצמה במחקרים רבים – אך עדיין לא נכנסה לפרקטיקה הרפואית. היא פשוט עדיין לא מתקדמת מספיק. המבנים שהיא יוצרת אינם יציבים מספיק, התאים שבעמקי הרקמה סובלים ממחסור בחמצן ומזון, ואם נודה באמת – היא גם יקרה מאד. באופן אידיאלי נעשה שימוש בתאים המגיעים מגוף החולה עצמו, וכל התהליך הנדרש כדי להפיק אותם, לגדל אותם ולזרוע אותם באמצעות המדפסת, לוקח זמן רב וטיפול מסור.
אני רגיל לספר על השיטות השונות המקובלות כיום בתחום הנדסת הרקמות, ורגיל גם לתשובה שמיד יורים עליי: אז למה לא לנסות?
כן, מדפסות תלת-ממד עדיין לא יעילות מאד בהדפסת רקמות, אבל למה לא להשתמש בהן כדי להדפיס בכל זאת כלייה בסיסית, להשתיל בגוף ולקוות לטוב? למה לא לקחת אורגנואידים המכילים מיני-מוחות, לפרק אותם ולהשתיל אותם במוחותיהם של חולי אלצהיימר ופרקינסון, כדי שתאי העצב שהם מכילים ישקמו את המבנים המוחיים שאבדו ויתפסו את מקום התאים שמתו? למה לא לעשות דה-סלולריזציה לפיגומים המגיעים מבעלי-חיים, ופשוט – ובכן, לנסות?
את התשובה לשאלה קיבלנו בעשור האחרון, כאשר מנתח איטלקי בשם פאולו מצ'יאריני, הפך "לאחד הרופאים המפורסמים ביותר בעולם", כדברי ה- BBC. הוא עלה לגדולה בזכות פרוצדורה חדשה שפיתח להחלפת טרכיאה – קנה נשימה – ברקמה שרוקנה מתאיה ואוכלסה בתאי גזע. לאורך שלוש שנים, הוא ביצע את הפרוצדורה בתשעה חולים שאיבדו את התקווה לחיות חיים בריאים ללא סיוע צמוד ממכונת הנשמה. הניתוחים סוקרו באופן נרחב ואוהד על-ידי התקשורת, אבל התוצאות לא הצדיקו את ההייפ. מתוך תשעת המושתלים, שבעה מתו בשלוש השנים שלאחר ההשתלה, ואחד נותר בחיים רק לאחר שסולק קנה הנשימה המלאכותי שהושתל בגרונו[11].
בדיעבד הסתבר שהניסויים שביצע מצ'יאריני היו נגועים ברשלנות, ושהאיש פיתח מערכת יחסים של אהבה-אהבה עם הקהילה המדעית ועם התקשורת, שהרשתה לו להפריז בכזבים אודות תוצאות הניסויים והניתוחים החיוביות. אהבה מילולית, אגב, מכיוון שהמנתח גם גרם לכתבת להתאהב בו, שיקר לה שהוא גרוש, והבטיח לה חתונה של כוכבים, בה האפיפיור עצמו ייחתן את השניים ואלטון ג'ון ישיר להם סרנדות.
אפשר להסיק שלל מסקנות מהפרשיה. למשל, לא לשקר במדע. מסקנה אחרת שמדענים יודעים היטב, היא שכל תחום מדעי מסובך ומורכב הרבה יותר מכפי שהוא נראה מבחוץ, ושישנן הרבה יותר דרכים להיכשל מלהצליח. זה נכון במיוחד ברפואה.
מסקנה שלישית היא שלכל ניסוי ברפואה ישנן השלכות מתגלגלות, גם על הלך-הרוח הציבורי ובקרב הקהילה המדעית. בעקבות הסקנדל של מצ'יאריני, הקהילה המדעית כולה נתקפה בספקנות קשה לגבי ניתוחי השתלת קנה נשימה. כאשר דוקטור אריק גנדן התכוון לנסות להציל את חייה של אשה באמצעות החלפת קנה הנשימה שלה בתרומה, עמיתיו הזהירו אותו שלא לנסות אפילו להיכנס לשדה המוקשים הזה. הוא חשב שעבודתו –
"הפכה ללא-נחוצה, כך שאתה בעצם סוגר את המעבדה. אתה לא יכול להצדיק עריכת ניתוחים ניסיוניים… כשאתה רואה משהו אחר שנראה מושלם. כך שאתה מבין, וואו, שלא צריכים אותך."
בסופו של דבר, גנדן החליט לבצע את הפרוצדורה הרפואית, והשתיל חלק מקנה הנשימה של תורם באשה שלא הייתה מסוגלת לחיות עוד עם קנה הנשימה הפגום בו ניחנה. הניתוח עבר חלק, וכיום היא קיבלה בחזרה את חייה. אבל בהחלט ייתכן שאילולא הפרקטיקה של מצ'יאריני – שלמעשה ערך ניסויים חסרי-אחריות על גביהם של החולים – היא ואחרים היו יכולים ליהנות מקנה נשימה תקין הרבה לפני-כן. ברפואה, כמו במדע, אין קיצורי דרך.
כל זה לא בא לומר שאין צורך בניסויים נועזים או בפיתוח טכניקות חדשניות ויוצאות-דופן. אבל צריך תמיד לשמור על צניעות ולהבין שרב הנסתר על הגלוי, ושכל ניסיון לקפוץ למים העמוקים, יוביל כמעט-תמיד לטביעה. ובמקרה הגרוע ביותר התוצאה לא תהיה מותו של אדם אחד, אלא גם פגיעה בתחום כולו לאורך שנים ארוכות. פגיעה שכזו תביא, בסופו של דבר, לעיכוב הזמן שנדרש עד שמטופלים יוכלו לקבל רקמות שיופקו ויושתלו בדרכים בטוחות יותר.
בשנת 1908 התבצע הניסיון הראשון בהשתלת ראש שלם: ראשו של כלב אחד הועבר לצווארו של כלב שני. הניסוי נכשל ושני הכלבים מתו, אבל זו הייתה רק ההתחלה. הטכנולוגיה המשיכה להתפתח, ובשנות השבעים הצליח רוברט ווייט לבצע את השתלת הראש הראשונה בקופים. הקוף שראשו הועבר לגוף אחר הצליח לשרוד שמונה ימים, תוך שהוא מסוגל להניע את שרירי הפנים, וניחן בחוש הריח, הטעם והשמיעה. ניסויים דומים נערכו גם בעכברים ובחולדות, ובשנים האחרונות גם בגופות של בני-אדם.
בימים אלו קיימים כבר מנתחים המבטיחים שבעשור הקרוב הם יבצעו החלפת ראש מלאה. כשזה יקרה, הכל ישתנה. נוכל להעביר, הלכה למעשה, נפשות מגוף לגוף. כל עוד לאדם כלשהו יהיה מספיק כסף, הוא יוכל להשתמש בו כדי לרכוש גוף חדש, צעיר ורענן. או משומש קלות, ועדיין – עדיף על פני מוות מסרטן או מחלה קשה אחרת.
אם המחשבה נשמעת לכם מזעזעת, כדאי לזכור שהתגובה הציבורית המיידית גם להשתלות הלב הראשונות הייתה שהרופאים "משחקים בלהיות אלוהים" ומשתעשעים בהפרת חוקי הטבע. כדאי גם לזכור שעבור רוב מכריע של בני-האדם, הרעיון של השתלת לב או של הפריית מבחנה נראה גם הוא כמדע בדיוני, ממש עד הרגע בו הפרוצדורות האלו נוסו בהצלחה, ואז הם הפכו לחלק מדרך החיים הרגילה שלנו[12].
ובכל זאת, אי-אפשר להתעלם משאלה אתית גדולה וממשית בנושא השתלות ראש ומוח: האם הוגן להעניק גוף שלם כדי להציל את חייו של אדם יחיד, בזמן שאותו גוף מכיל מספר רב של רקמות אחרות שהיו יכולות לסייע לרבים אחרים? תורם אחד, אחרי הכל, יכול להעניק מעיניו, כליותיו, לבו, כבדו, עורו ועוד איברים אחרים. או שהוא יכול להעניק גוף אחד ויחיד ל- 'מותרם' אחד.
אני משוכנע שזוהי שאלה שעוד נצטרך להתמודד איתה בעתיד הנראה לעין, אבל היא לא תטריד אותנו במשך שנים רבות. הסיבה, במילה אחת, היא אוטומציה. ובשתי מילים – אילון מאסק.
אילון מאסק הקים את חברת נוירלינק בשנת 2016, במטרה לפתח ממשק שיתחבר למוחותיהם של בני-אדם ויאפשר להם לתקשר עם מכונות – ולמכונות לתקשר ישירות עם המוח. החברה רצה קדימה במהירות, וכבר הספיקה לעשות הרבה. או מעט. תלוי את מי שואלים.
אם תשאלו את הציבור הרחב, תגלו שאנשים מספרים לכם בעיניים פעורות שנוירלינק הצליחה לקרוא את גלי המוח של חזיר באמצעות אלקטרודות המחוברות למוחו. הם ידווחו לכם שהקופים של נוירלינק כבר יכולים לשחק במחשב מבלי להזיז את קצה הזנב שלא לדבר על האצבעות, אלא באמצעות מחשבה בלבד. הממשק קורא את הפעילות המוחית שלהם ומתרגם אותה לשליטה במחשב. אכן, נסים ונפלאות.
אם תגשו לנוירולוגים ותשאלו אותם אודות נוירלינק, תתקלו בגיחוך ידעני. כן, החברה באמת הצליחה לקרוא את הפעילות המוחית של קופים וחזירים, יאמרו לכם, ואז יוסיפו באגביות שאלו דברים שמדענים במעבדותיהם כבר עשו לפני עשרים שנים. במילים אחרות, אין חדש תחת השמש, מלבד יחסי-ציבור.
האמת היא ששניהם צודקים. נוירלינק עדיין רחוקה מלחדש בתחום מדעי המוח, אבל אנו צופים כאן בחברה שלמעשה מצליחה לקום מאפס ולשחזר ניסויים שנערכו בעבר במעבדות המתקדמות בעולם ומסתמכים על ידע סמוי עצום: איך לטפל בקופים ובחזירים, איך להחדיר אלקטרודות, איך לשמר את כולם בחיים, איך לעשות עיבוד אותות ועוד ועוד. אפשר לומר שעם הקוף היא כמעט סיימה לשחזר את מה שקורה במעבדות, ועכשיו יש לחוקרים שלה את המיומנות והניסיון הנדרשים כדי להמשיך הלאה.
שני דברים מעניינים אותי במיוחד בנוגע לנוירלינק, ולשניהם יכולה להיות השפעה עצומה על חיינו בעתיד. , ועל שניהם כדאי להתעכב לרגע.
הראשון הוא שנוירלינק מתכוונת – בסופו של דבר, כשהטכנולוגיה שלה תהיה מתקדמת מספיק – לספק לכולם דרך לשלוט באופן ישיר על המוח של עצמם. החזון של מאסק הוא של שכבה של אלקטרודות שתוחדר למוח הביולוגי באופן פשוט וללא סיבוכים רפואיים, ובאמצעותה נוכל להורות למוח מה עליו לעשות. לא צריך להתקדם לסיפורי – או סיוטי – מדע בדיוני שמבטיחים לנו יכולות מתקדמות של קריאת מחשבות. אפילו אם נוכל רק לשלוט על הפרשת הנוירוטרנסמיטרים – סרוטונין, דופאמין ואחרים – הרי שהעולם ישתנה בין-לילה.
דמיינו עולם עתידי בו אתם חוזרים הביתה עייפים וסחוטים מיום העבודה המפרך, אבל עדיין משתוקקים לכתוב את הספר שתמיד חלמתם עליו. בלחיצת כפתור, אתם מורים למוחותיכם להיות סקרנים יותר, נמרצים יותר, מוכנים יותר לשפיכת ידע על המקלדת. או אולי, בכפתור אחר, אתם מאפשרים לעצמכם להיפתח יותר לרגשות הפנימיים שלכם, להפוך לאמפתיים יותר ולהתחבר יותר לאשה ולילדים. כפתור שלישי ידכא את תחושת הרעב שלכם, או יגביר את יכולתכם לשלוט ביצריכם כדי לסייע לכם בדיאטה.
איך נשמע לכם עולם כזה? חלום? סיוט? גם וגם?
לטעמי, הגדולה בחזון הזה היא ביכולת הבחירה שהוא מקנה לכל אדם. אתם תצטרכו לבחור מה חשוב עבורכם יותר או פחות. אתם תצטרכו להחליט איך לחלק את הזמן, תשומת הלב והאהבה בין כל המטלות והישויות המקיפות אותנו. מאסק רוצה, למעשה, לתת לנו מוח-עליון שנוכל לקבל באמצעותו החלטות אודות דברים שבעבר היו כפופים במידה רבה לסביבה ולביולוגיה הבסיסית שלנו: רגשות ומצבי-רוח.
ושוב – חלום או סיוט? אתם תחליטו. כנראה שלא תצטרכו לקבל את ההחלטה הזו בעשור הקרוב, אבל יפתיע אותי אם בעוד עשרים שנים לא יהיו אנשים שייהנו כבר ממוח-עליון שכזה.
הנקודה המעניינת השנייה בנוגע לנוירלינק היא שהחברה פיתחה, לטענתה, רובוט המסוגל לבצע באופן אוטומטי את הפעולה המסובכת של החדרת האלקטרודות למוח. לפי הפרסומים – שיש להתייחס אליהם מאד בחשדנות – הרובוט מסוגל להחדיר כיום כמעט מאתיים אלקטרודות בדקה, באמצעות מחט דקיקה וחור שהוא פותח בגולגולת. כמובן שבסוף הניתוח הוא גם סוגר יפה את החור במעין 'פקק' בגודל של מטבע חצי-שקל, שמכיל גם משדר דרכו מתקשרות האלקטרודות עם הסביבה[13].

אפשר להגיד דברים רבים על מאסק – לא כולם טובים – אבל הוא מבין שאת העתיד יעצבו מספר רב של טכנולוגיות שונות שישתלבו זו בזו. רובוטים משוכללים, למשל, יוכלו למזער את עלויות השתלת האלקטרודות במוח ואת הסיכון הכרוך בפרוצדורה כזו. רובוטים שכאלו אינם בנמצא, עדיין, אבל מאסק כבר חוזה את קיומם, ואני מסכים איתו. רובוטים בעלי רמה כזו של יכולות אמורים להגיע לכדי מימוש בעשור הקרוב.
ועכשיו חשבו על רובוטים בעלי רמת יכולות דומה שיעבדו גם במעבדות ובבתי-החולים: רובוטים שיוכלו לקחת דגימות רקמה ממטופלים, לגדל את התאים ולדאוג להם במעבדות, להדפיס את הרקמות הביולוגיות – ובסוף גם להשתיל אותם בגוף המטופל.
האם העתיד הזה מוזר מדי עבורכם? נהיה שמרנים יותר: אפילו אם כל תפקידם של הרובוטים יסתכם 'רק' בגידול הרקמות האנושיות במעבדה, עדיין המשמעות תהיה שעלויות החלפת הרקמות ירדו משמעותית. האוטומציה – היכולת לייצר רקמות באופן אוטומטי-ברובו – תוודא שגם עניים יוכלו לקבל רקמות חלופיות, כל עוד הם חיים במדינה עם מערכת בריאות ורווחה מתפקדת.
אל תטעו: כל זה לא עומד לקרות בשנים הקרובות, וכנראה שבעשור הנוכחי לא נוכל עדיין לייצר מגוון רקמות לכל דורש. אבל בשביל הגשמת מטרה גדולה שכזו, שתקפיץ אותנו חצי-הדרך לחיי-הנצח המובטחים, אפשר לחכות גם שניים-או-שלושה עשורים. וגם אם אתם לא ממש יכולים לחכות, ובכן – אין ברירה.
מהנדסים ביו-רפואיים עובדים כבר עשרות שנים על היכולת להחליף רקמות ואפילו איברים שלמים בגוף האנושי. קיימות שיטות עם פוטנציאל גדול להחלפת רקמות, כאשר המרכזית מביניהן היא הדפסת הרקמות החלופיות בתלת-ממד לפני השתלתן בגוף. אנו גם רואים נכונות מצד קהילות המהנדסים והמטופלים, 'להרחיב אופקים' ולבחון חלקי-חילוף יוצאי-דופן לגוף, כמו לבלב מלאכותי שמורכב משלושה חלקים נפרדים – חיישנים, בינה מלאכותית ומשאבה להזרקת אינסולין. המחקר מתקדם במהירות, אבל המעבר לפרקטיקה הרפואית איטי יותר, כראוי בתחומים בהם כל טעות יכולה לעלות בחייהם של בני-אדם.
הבינה המלאכותית והרובוטיקה יכולות לעזור לנו להאיץ את קצב המחקר המדעי והיישום הממשי, אבל אפילו אז – אין ספק שעוד רבה וארוכה הדרך. ובכל זאת, אני משוכנע שעוד במאה הזו – וכנראה שכבר בעשורים הקרובים – יוכל כל אדם לזכות ברקמות ובאיברים שיחליפו את אלו עמם גדל מינקות. וכפי שאמר לי אותו פרופסור לרפואה: כאשר נוכל להחליף את הלב הכושל או הכבד הקורס, לחדש את העור ולהטליא את המוח בתאי עצבים צעירים – אז נוכל, למעשה, לעצור את ההזדקנות ולהשיב לכל אדם את נעוריו.
מי ייתן – במהרה בימינו.
[1] https://www.nature.com/news/2006/060403/full/news060403-3.html
[2] https://biofabexplorer.cast.org/case-stories/meet-luke
[3] https://journals.lww.com/jpojournal/FullText/2014/04000/Socket_Pressure_and_Discomfort_in_Upper_Limb.7.aspx
[4] https://www.hss.edu/condition-list_osseointegration.asp
[5] https://www.healthline.com/health-news/future-prosthetics-might-be-this-mind-controlled-bionic-arm#How-the-technology-works-compared-with-conventional-prostheses
[6] https://qz.com/2141720/modern-prosthetics-go-beyond-bionic-limbs-and-into-the-brain/
[7] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6928092/
[8] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4892160/
[9] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4892160/
[10] https://www.livescience.com/brain-organoid-optic-eyes.html
[11] https://www.bbc.com/news/magazine-37311038
[12] https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6511668/
[13] https://en.wikipedia.org/wiki/Neuralink
עוד בנושא באתר הידען:
