תוך שימוש בזבובי פירות בתור מודל, החוקרים בודדו גן השולט במקצב הביולוגי היומי הרגיל. הם הראו כי גן זה מקודד חלבון המצטבר בתאים במהלך שעות הלילה, ואז הוא מתפרק במהלך שעות היום. בעקבות כך, הם גילו רכיבי חלבונים נוספים המרכיבים את המערכת הזו, תוך חשיפת המנגנון השולט בשעון הביולוגי בתוך התאים עצמם

ג’פרי סי הול, מייקל רוסבאש ומייקל יאנג על גילוי המנגנונים המולקולאריים שבבסיס המקצב הצירקדי, מקצב שפועל במחזוריות של כ-24 שעות ונועד להתאים את פעילותו של היצור להשפעתה המשתנה של השמש לאורך היממה. מקצב זה קובע את השעון הביולוגי המרכזי של האורגניזם.
החיים על פני כדור הארץ מותאמים לסיבוב של הפלנטה שלנו. מזה שנים רבות שידוע כי יצורים חיים, לרבות בני האדם, מכילים בתוכם שעון ביולוגי פנימי המסייע להם לחזות ולהתאים את עצמם למקצב הרגיל של היממה. אולם כיצד שעון זה מתפקד בדיוק? שלושת חתני פרס הנובל לשנה זו הצליחו להציץ לתוך השעון הביולוגי שלנו ולהבין את רכיביו הפנימיים. התגליות שלהם מסבירות כיצד צמחים, בעלי-חיים ובני אדם מתאימים את המקצב הביולוגי שלהם כך שהוא מסונכרן עם סיבוב כדור הארץ על צירו.
תוך שימוש בזבובי פירות בתור מודל, החוקרים בודדו גן השולט במקצב הביולוגי היומי הרגיל. הם הראו כי גן זה מקודד חלבון המצטבר בתאים במהלך שעות הלילה, ומתפרק במהלך שעות היום. בעקבות כך, הם גילו רכיבי חלבונים נוספים המרכיבים את המערכת הזו, תוך חשיפת המנגנון השולט בשעון הביולוגי בתוך התאים עצמם.
השעון הפנימי שלנו, תוך דיוק ברמה הגבוהה ביותר, מתאים את הפיזיולוגיה שלנו לשלבים המשתנים תדיר בשעות היממה. השעון הזה מווסת תפקודים חיוניים כגון ההתנהגות שלנו, רמות ההורמונים בגוף, שינה, טמפרטורת הגוף ואת חילוף החומרים. הרווחה הפיזית שלנו מושפעת כאשר מתקיים חוסר איזון זמני בין הסביבה החיצונית שלנו לבין השעון הביולוגי הפנימי שלנו, למשל – כאשר אנו חוצים מספר אזורי זמן וחווים יעפת (ג’ט-לג). יש רמזים גם לכך שחוסר איזון כרוני בין אורח החיים שלנו לבין המקצב המוכתב על ידי השעון הפנימי שלנו קשור לסיכון מוגבר להתפרצותן של מגוון מחלות.
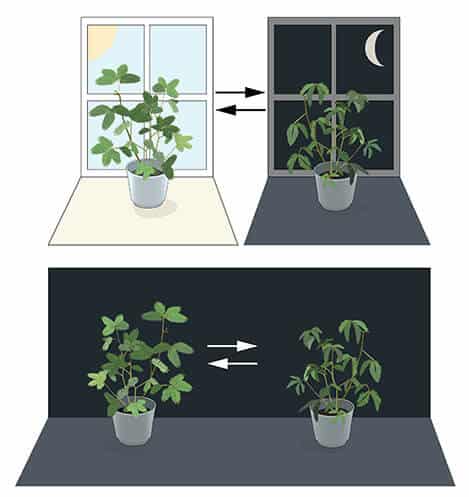
השעון הפנימי שלנו
מרבית היצורים החיים מצפים ומסתגלים לשינויים היומיים בסביבה. במהלך המאה השמונה עשרה, האסטרונום Jean Jacques d’Ortous de Mairan חקר את צמח המימוזה ומצא כי הצמח פורש את העלים שלו לכיוון השמש במהלך שעות היום ומקפל אותם בשעות החשיכה. הוא תהה מה יקרה לצמח אם הוא יימצא במצב קבוע של חשיכה. הוא גילה כי ללא תלות באור השמש היומי העלים המשיכו לדלג בין מצבם הפרוש למצבם המקופל, כפי שהורגלו מרגע בריאתם (איור 1). נראה כי לצמחים יש שעון ביולוגי משל עצמם.
חוקרים אחרים גילו כי לא רק צמחים, אלא גם בעלי חיים ואפילו בני אדם, הם בעלי שעון ביולוגי המסייע להם להתאים את הפיזיולוגיה שלהם בעקבות השינויים המתחוללים במהלך שעות היממה. ההתאמה הסדורה הזו מכונה בשם ‘המקצב הצירקדי’ (circadian rhythm) שמקורה במילים הלטיניות circa שמשמעותה ‘מסביב’ ומהמילה הלטינית dies שמשמעותה ‘יום’. אולם, כיצד בדיוק השעון הביולוגי הפנימי שלנו פועל נותר בגדר תעלומה.
גילוי הגן האחראי על פעילות השעון
במהלך שנות השבעים, החוקר סימור בנזר והסטודנט שלו Ronald Konopka תהו האם אפשר לזהות גנים האחראים למקצב הצירקדי בזבובי פירות. הם הדגימו כי הכנסת מוטציות לגן בלתי מזוהה גרמה לשיבוש בשעון הביולוגי של הזבובים. הם כינו את הגן הזה בשם ‘מחזוריות’. אולם הם עדיין לא הבינו כיצד הגן הזה משפיע על המקצב היומי.
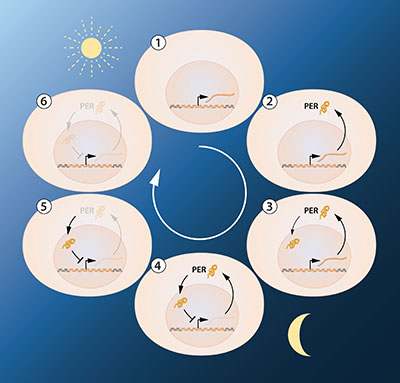
חתני פרס הנובל לשנת 2017, שגם הם חקרו זבובי פירות, התמקדו בגילוי מנגנון פעילותו של השעון הביולוגי. בשנת 1984, שני החוקרים Jeffrey Hall ו-Michael Rosbash, שעבדו בשיתוף פעולה הדוק באוניברסיטת בוסטון, יחד עם Michael Young, באוניברסיטת ניו יורק, הצליחו לבודד ולזהות את הגן. בשלב הבא הצליחו שני החוקרים Jeffrey Hall ו-Michael Rosbash לגלות את החלבון המקודד על ידי הגן הזה, חלבון PER. מסתבר כי חלבון זה מצטבר במהלך הלילה ומתפרק במהלך היום. כלומר – רמות החלבון PER עולות ויורדות במחסור של 24 שעות, בסנכרון מלא עם המקצב הצירקדי.
מנגנון של שעון המווסת את עצמו באופן עצמאי
היעד הבא במחקר היה להבין כיצד תנודות צירקדיות אלו מתקבלות ונעלמות. החוקרים Jeffrey Hall ו-Michael Rosbash שיערו כי חלבון ה-PER חוסם את פעילות של גן המחזוריות. הם סברו כי באמצעות מעגל משוב מסוג עיכוב, חלבון ה-EPR יכול למנוע את הסינתזה שלו עצמו ולפיכך לווסת בעצמו את רמות החלבון במסגרת מקצב מעגלי ורציף (איור 2A).
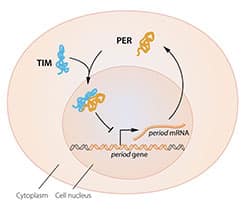
המודל הזה היה מפתה, אך עדיין היו חסרים מספר פיסות מהתצרף. בכדי לחסום את הפעילות של גן המחזוריות, חלבון ה-PER, הנוצר בציטופלזמה, צריך להגיע לגרעין התא, שם נמצא החומר הגנטי. שני החוקרים הראו כי החלבון מצטבר במהלך הלילה בגרעין התא, אולם הם לא ידעו להסביר כיצד הוא מגיע לשם. בשנת 1994 החוקר Michael Young גילה גן נוסף האחראי לשעון הביולוגי, שאותו הוא כינה בשם ‘נצחי’ (timeless), המקודד חלבון בשם TIM אשר נדרש לשם קיומו של מקצב צירקדי נורמלי. במהלך ניסוי אלגנטי ביותר, החוקר Michael Young הראה שכאשר שני החלבונים (TIM+PER) נקשרים יחדיו, הם מסוגלים לחדור לגרעין התא שם הם חוסמים את פעילותו של גן המחזוריות ויוזמים את רצף הפעולות של המשוב (איור 2B).
איור 2B חלבון ה-PER, האחראי לעיכוב הגן המקודד לו, מצליח לחדור לגרעין התא רק כאשר הוא מחובר לחלבון השני, חלבון TIM.
מנגנון משוב שכזה אכן מצליח להסביר את התנודות ברמות החלבון בתא, אולם עדיין נותרו מספר שאלות. מה שולט בתדירות התנודות? מייקל יאנג זיהה גן נוסף, גן ששמו doubletime, המקודד את החלבון DBT הגורם לשיהוי בקצב הצטברותו של חלבון ה-PER בגרעין התא. גילוי זה מספק את התובנות הנדרשות בכדי להבין כיצד התנודות מתאימות כמעט בדיוק למחזור של 24 שעות.
התגליות החדשניות של חתני פרס הנובל לפיזיולוגיה לשנת 2017 הולידו עקרונות מנגנוניים עיקריים הנמצאים בבסיסו של השעון הביולוגי. במהלך השנים שלאחר מכן, נתגלו רכיבים נוספים של מנגנון זה, רכיבים שהעמיקו את ההבנה בדבר יציבותו ואיתנותו של מנגנון זה. למשל, חתני פרס הנובל זיהו חלבונים נוספים הנדרשים לשפעול של גן המחזוריות, וכן חלבונים שבעזרתם אור יכול לסנכרן את השעון.
משגיחים על הפיזיולוגיה האנושית
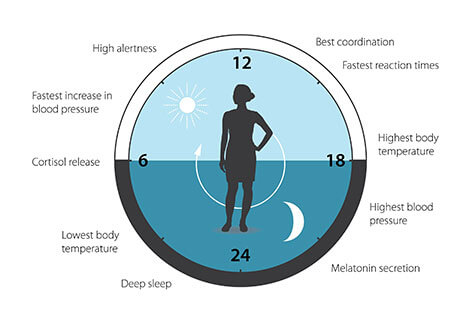
השעון הביולוגי מעורב בהיבטים רבים של הפיזיולוגיה המורכבת שלנו. כיום אנו יודעים כי כל היצורים הרב-תאיים, לרבות בני אדם, עושים שימוש באותו מנגנון על מנת לשלוט במקצב הצירקדי. מספר גדול מהגנים שלנו מווסת על ידי השעון הביולוגי, ובעקבות כך, מקצב צירקדי מכויל בקפדנות מתאים את הפיזיולוגיה שלנו לשלבים השונים במהלך היממה (איור 3). מאז התגליות של שלושת חתני פרס הנובל, התחום של ביולוגיה צירקדית התפתח לכדי תחום מחקר עצום ודינמי ביותר, עם השלכות לבריאות האדם ורווחתו האישית.

4 תגובות
צירקדי. אתקן
לא הבנתי, אז זה ציקרדי או צירקדי? כח פעם כתוב אחרת!
האם זה צריך להיות צירקרדי בכלל?
יהונתן, הטעות לא היתה של ד”ר משה נחמני אלא שלי בהעלאת הכתבה.
כתבה מאוד מעניינת. רוצה רק לתקן שאת הטקסט:
“מנגנון משוב שכזה אכן מצליח להסביר את התנודות ברמות החלבון בתא, אולם עדיין נותרו מספר שאלות. מה שולט בתדירות התנודות? מייקל יאנג זיהה גן נוסף, גן ששמו doubletime, המקודד את החלבון DBT הגורם לשיהוי בקצב הצטברותו של חלבון ה-PER בגרעין התא. גילוי זה מספק את התובנות הנדרשות בכדי להבין כיצד התנודות מתאימות כמעט בדיוק למחזור של 24 שעות.”
כתבת פעמיים אחד אחרי השני :).
בנוסף, מעניין אם הגוף שלנו מסוגל להסתגל לזמן אחר מ-24 שעות הסטנדרטיות שלנו ואיך אנחנו נגיב לכך.