הצ’יפ הגנטי הוא טכנולוגיה חדשנית לבדיקה מפורטת לאיתור חוסרים או עודפים זעירים בגנום ומשפר מאוד את יכולת האבחון
עידית מאיה ומרדכי שוחט | גליליאו
הגנטיקה הקלאסית מתחלקת לשתי זרועות עיקריות: הציטוגנטיקה, הגנטיקה ה”תאית”, המתייחסת לכלל המידע הגנטי באריזתו הבסיסית – הכרומוזומים; והגנטיקה המולקולרית, גנטיקת ה”צופן” (קוד), שבמסגרתה מפענחים את רצף חומצות הגרעין של הדנ”א (DNA) שהוא ה”אותיות” המקודדות את יחידת המידע הבסיסית, הגֶן.
בכל אחד מתאי גופנו המגורענים קיימים 23 זוגות של כרומוזומים (46 בסך הכול) שמתוכם 22 זוגות הזהים לזכרים ונקבות, וזוג אחד של כרומוזומי מין: שני כרומוזומי Xלנקבות וכרומוזום Xאחד ו-Yאחד לזכרים. סליל הדנ”א, רצף האותיות המהווה את המידע הגנטי שמקודד לבניית חלבונים, מקופל וארוז בתוך הכרומוזומים בצורה מסודרת ומדויקת, ומאפשר את תפקודו של כל אחד מתאי גופנו. אפשר להשוות את כלל המידע הגנטי שבכל אחד מתאי גופנו לאנציקלופדיה גדולה ובה 46 כרכים המכילים פרקים רבים וערכים רבים. כל כרך שכזה הוא כרומוזום ובתוכו מספר רב מאוד של אותיות מידע.
במאמר זה נתמקד בציטוגנטיקה ובשיטות השונות לאבחן חוסרים או עודפים של “כרכים” שונים או “פרקים” שונים בהם. נזכיר את השיטות הישנות והמוכּרות מחד גיסא, ומאידך גיסא נתמקד בשיטה ציטוגנטית חדישה הקרויה הצ’יפ הגנטי.
שיטת הקריוטיפ: ספירה וצביעה
בשיטה הקלאסית, הקרויה “קַריוֹטיפּ” והמוכּרת בגנטיקה מזה כ-50 שנים, מתבוננים בתא הנמצא בשלבי חלוקה ובו אפשר לראות את הכרומוזומים במיקרוסקופ אור. בשיטה זו סופרים את הכרומוזומים ובאמצעות צביעה מיוחדת, הקרויה צביעת גימזה, גם מסתכלים על המבנה הפנימי שלהם הנראה כמעין פספוס בשחור ולבן. בשיטה זו בודקים את כמות הכרומוזומים ואת המבנה שלהם, למשל בתאי דם לבנים שנלקחו בבדיקת דם רגילה, או מתאי עובּר המופקים בדיקור נוזל השפיר או בבדיקת סיסֵי שליה (CVS). שתי בדיקות אלו הן בדיקות חודרניות: בבדיקת סיסי שליה מגיעים דרך הנרתיק לאזור של השליה וממנו לוקחים דגימת תאים. בדיקור נוזל השפיר דוקרים את השק הקרומי (שק השפיר) שבו שוחה העובּר (ובדרך את דופן הבטן ודופן הרחם של האם) בכדי לשאוב דגימה של נוזל השפיר. מתוך דגימות אלו מסננים את תאי העובר, מגדלים אותם בתרבית במעבדה ובודקים אותם בשיטת הקריוטיפ באמצעות מיקרוסקופ האור בחיפוש אחר תאים הנמצאים בשלבי חלוקה (מיטוזה), שכן בתאים אלה אפשר לראות את הכרומוזומים. יש לזכור כי מדובר בהליך שאינו נטול סיכונים וידוע כי בעקבותיו קיים סיכון להפלה העומד על 1:300-1:500 בבדיקת נוזל שפיר וסביב 1:100 בבדיקת סיסי שליה.
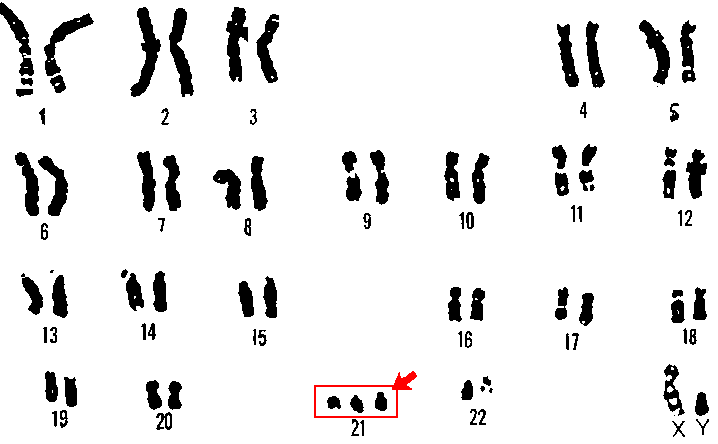
בדיקת קריוטיפ מאפשרת לאבחן תסמונות גנטיות הנובעות מחוסר או מעודף של כרומוזומים שלמים, או של מקטעים גדולים בתוך הכרומוזומים (של כמה מיליוני נוקלאוטידים לפחות). דוגמה לתסמונת המאובחנת בשיטה זו היא תסמונת דאון, טריזומיה 21 (שלישיה של כרומוזומים מספר 21 במקום זוג כרומוזומים). אפשר לאבחן תסמונת דאון ובעיות כרומוזומיות נוספות הן לאחר הלידה והן בבדיקת סיסי שליה או נוזל השפיר במהלך ההיריון. עוד אפשר לבצע בדיקת קריוטיפ גם בתאים סרטניים שמקורם במח העצם או באיברים שונים, בחיפוש אחר שינויים מבניים או כמותיים בכרומוזומים המעידים על מאפיינים קליניים שונים של הגידולים. לדוגמה, בסרטן שמקורו במח העצם הקרוי “לוקמיה מילוציטית כרונית” (Chronic Myelocytic Leukemia:CML) נפוץ שינוי מבני (טרנסלוקציה – העתקת קטע כרומוזום למיקום אחר) בתאי הסרטן, ובמקרה זה – חיבור בין כרומוזום 9 לכרומוזום 22. שינוי מבני זה גורם לגדילה לא מבוקרת של תאי מח העצם ולהופעת הגידול הממאיר. על פי שינויים אלו ואחרים הנצפים בתאי הגידול נוכל לעתים לאפיין את סוג הגידול ולעתים לבחור את הטיפול הכימותרפי המתאים ביותר.
הצ’יפ הגנטי: איתור שינויים נרחב
צ’יפּים (שבבים) גנטיים הם טכנולוגיה חדישה, המאפשרת לבדוק בבת אחת אזורים רבים (מאות אלפי אתרים) בחומר הגנטי של הנבדק. קיימים צ’יפים גנטיים מסוגים שונים; מהם שבודקים שינויים של בסיסים בודדים (SNP: Single Nucleotide Polymorphism), כלומר שינוי בין “אות” אחת לאחרת (בין נוקלאוטיד אחד לאחר) בתוך הקוד הגנטי, ומהם שבודקים הבדלים של מקטעים זעירים בין דגימת המטופל לדגימת בקרה. הצ’יפ הגנטי קרוי בשפה המדעית CMA(Chromosomal Micro-arrayAnalysis)או בשמו האחרArray Comparative Genomic Hybridization , ובקיצור Array CGH. זוהי שיטה ציטוגנטית חדשה, המאפשרת איתור של שינויים מבניים או כמותיים קטנים יותר מבדיקת הקריוטיפ הקלאסית. בשיטה זו מפרידים את כלל הכרומוזומים לכמה אלפי מקטעים זעירים ומשווים למקטעי בקרה. אם נמצא חוסר או עודף של מקטע זעיר כזה, אזי נוכל לברר את תכולת הגנים שבו וכך לדעת אם אפשר לשייך ממצא מעבדתי זה למכלול התסמינים אצל המטופל. בדיקה זו כבר נערכה עד כה לאלפי אנשים בריאים, וכך נוכל לדעת אילו מהשינויים הכמותיים הללו (חסר או עודף) שכיח באוכלוסייה וקיים בפרטים בריאים, ואילו שינויים הם נדירים ויכולים לגרום לפגיעות כגון פיגור שכלי או מומים מולדים. לרוב מתייחסים לממצא הקיים באחד מתוך מאה פרטים בריאים (כלומר בכ-1% מאוכלוסייה מסוימת) כאל ממצא שכיח ולממצא הקיים בשכיחות נמוכה יותר כנדיר.
באמצעות שיטת הצ’יפ הגנטי אפשר לאתר מאות תסמונות גנטיות ידועות כגון תסמונת חך-לב-פנים, המכונה גם תסמונת Velo-Cardiofacialאו תסמונת די-ג’ורג’ (ונובעת מחסר של מקטע זעיר בכרומוזום 22), או תסמונת ויליאמס (הנובעת מחסר של מקטע זעיר בכרומוזום 7; וראו: “סדקים פנימה”, גליליאו 43, ינואר-פברואר 2001). לעומת שיטת הקריוטיפ הקלאסית, הרזולוציה של בדיקה זו היא עד פי מאה גבוהה יותר ואפשר לאתר באמצעותה חוסרים או עודפים זעירים של כמה עשרות אלפי או מאות אלפי נוקלאוטידים. זאת ועוד, בשיטה הישנה אי אפשר לאבחן תסמונות הנובעות מחסר של מקטע קטן שכזה. מנגד, שינויים מבניים מאוזנים (כגון טרנסלוקציות מאוזנות) לא יאותרו בשיטת הצ’יפ הגנטי, מכיוון שאין חסר של רצף גנטי מסוים, אלא רק שינוי מיקום שלו על פני הגנום.
“לדוג” פגיעות כרומוזומים זעירות
זה שנים רבות קיימת טכנולוגיה ציטוגנטית אחרת המכוּנהFISH(Fluorescent in Situ Hybridization). בשיטה זו משתמשים בגלאים פלואורסצנטיים כדי לחפש בצורה ממוקדת חסר או עודף של מקטע זעיר במיקום מסוים בכרומוזום. לדוגמה, בתסמונת חך-לב-פנים (תסמונת די-ג’ורג’) משתמשים בגלאי ספציפי לזרוע הארוכה של כרומוזום 22, במקטע מספר 11, שידוע כי הוא חסר בחולים הלוקים בתסמונת זו. בדיקתFISH כזו נעשית בגלל חשד לקיום התסמונת, עקב מאפיינים קליניים בילד או בעובּר כגון מומי לב, חך ושפה שסועים או ליקוי חיסוני. לעומת בדיקה זו, היתרון הגדול של בדיקת הצ’יפ הגנטי נעוץ בעובדה שהוא מאתר מאות תסמונות כאלו במקביל, בלא צורך בגלאי ממוקד, ולמעשה בלי חשד קליני ספציפי. את בדיקת הצ’יפ אפשר לבצע גם במטופלים שאין אנו יודעים מה האבחנה הקלינית לגביהם, כגון מטופלים הסובלים מפיגור שכלי בלי מאפיינים קליניים נלווים (כגון פגיעה מולדת בכליות או בלב) או מטופלים הלוקים באוטיזם. כמו כן אפשר להשתמש בשיטה זו כחלק מאבחון טרום לידתי באמצעות בדיקת סיסי השליה או נוזל השפיר גם ללא ממצאים כלשהם בעובר.
קיימים צ’יפים שונים של חברות מתחרות המשתמשים בטכנולוגיה זו, למשל של החברות Blugnomeו-Signature Genomics. כולם מבוססים על אותו עיקרון, אך מחלקים את כלל החומר הגנטי הנבדק למספר אחר של מקטעי דנ”א. הרזולוציה בבדיקה זו תהיה גדולה יותר אם מקטעי הדנ”א קטנים ורבים יותר. בבואנו לחפש הסבר לתמונה קלינית במטופלים שבהם יש חשד לתסמונות גנטיות, נשתמש בצ’יפ עם רזולוציה גבוהה יותר. לעומת זאת, בבדיקת של עובּרים (אם מדגימה של תאי העובּר שהופקה בדיקור נוזל השפיר ואם מתאים שנלקחו מסיסי השליה) נוטים להשתמש בצ’יפים עם רזולוציה פחות מפורטת בכדי להקטין את הסיכוי שניאלץ להתמודד עם תשובה שמשמעותה הקלינית אינה ידועה בשלב זה. ככל שיתבצעו יותר בדיקות כאלו בארץ ובעולם, אצל פרטים הלוקים בפיגור שכלי כמו גם אצל פרטים בריאים באוכלוסיות שונות במוצאן, כך יצטבר מידע רב יותר ואז נוכל לדעת מה משמעותם של חוסרים או עודפים זעירים, של כמה עשרות אלפים או מאות אלפי נוקלאוטידים (חוסרים ועודפים כאלה הם שכיחים) על הבריאות של הנבדק. בעתיד, אם טכנולוגיה זו תיכנס לשימוש נרחב, אזי נוכל להשתמש גם בצ’יפים בעלי הרזולוציה הגבוהה בבדיקות של עוברים.
ניתוח תוצאות הבדיקה
קיימות שלוש אפשרויות לתוצאות של בדיקה זו, ואלה הן:
א. תוצאה תקינה: לא נמצא חוסר או עודף של מקטע כרומוזומי זעיר, או שנמצא חוסר או עודף של מקטע זעיר, שמוכר כ”ווריאציה נורמלית” בבריאים כך שלא צפויה בעיה רפואית.
ב. תוצאה לא תקינה: נפרט בהמשך מהן האפשרויות שמעלה תוצאה זו.
ג. תוצאה שמשמעותה הקלינית אינה ברורה לגמרי: נמצא חוסר או עודף של מקטע כרומוזומי זעיר, שמשמעותו היא ככל הנראה תקינה, אבל יכול להיות ספק קטן שאי אפשר להוכיחו בשלב זה בגלל מיעוט של מידע בספרות הרפואית.
אם התוצאה אינה תקינה, דהיינו – שנמצא עודף או חוסר של מקטע כרומוזומי זעיר, שברור כי יש לו משמעות רפואית – נמצאה הוכחה להסתמנות קלינית מסוימת. במקרה זה קיימות כמה אפשרויות:
א. נמצא חוסר או עודף של מקטע כרומוזומי זעיר שמשמעותו היא תסמונת גנטית קשה ו/או פיגור שכלי או אוטיזם קשה. אפשר לאשר את נוכחות החוסר או העודף במרבית המקרים באמצעות בדיקת ה-FISH הספציפית. מדובר בממצא בעל משמעות קלינית ברורה, הן אם הדגימה היא של מטופל והן אם היא של תאי עובר. אם מדובר בדגימת תאי עובר, אפשר להתלבט עם בני הזוג אם להפסיק את ההיריון או להמשיך בו. הימצאות השינוי הגנטי בבדיקת הצ’יפ אצל מטופל או עובר מאפשרת לבדוק את הוריו לנשאות של שינוי זה, בכדי לדעת כיצד להגדירו: האם הוא הופעה חדשה (de novo) או האם הוא כבר קיים באחד ההורים?שלב זה מבוצע באמצעות חיפוש ממוקד של החוסר או העודף אצל ההורים בבדיקת FISH. על פי נשאות ההורים יש אפשרות לתת ייעוץ גנטי מדויק בנוגע לסיכוי הישנות התסמונת בהיריונותיהם העתידיים של ההורים ושל בני משפחה נוספים, ואף להציע להם בדיקות אבחנתיות לאיתור החוסר או העודף.
ב. נמצא חוסר או עודף של מקטע כרומוזומי שמשמעותו היא ככל הנראה תסמונת גנטית קשה, והוודאות לגביה היא גדולה (מעל 30%) אך אינה מוחלטת. קיימים כמה קריטריונים שבהם אנו מתחשבים בבואנו לנתח משמעות קלינית של חוסר או עודף של מקטע כרומוזומי שכזה. הקריטריון הראשון והחשוב ביותר הוא מידע על מקרים קודמים בספרות הרפואית: האם הוא נמצא בקרב מטופלים עם תמונה קלינית מסוימת, ואז ניטה לפרש את השינוי הגנטי כפתולוגי וכבעל משמעות קלינית, או שהוא נמצא באוכלוסייה הבריאה ואז ניטה לפרש את השינוי הגנטי כנטול חשיבות? הסיבה שאין ודאות מוחלטת במקרים אלו היא שבנוגע למקרים קליניים עם שינויים זעירים מסוימים עדייןאין בידינו מידע מספק. במצבים אלו אנו מנתחים את הנתונים על פי גודל המקטע הגנטי החסר או העודף ותכולת הגנים בו. אם המקטע גדול מאוד, ומכיל גנים רבים שידועים כבעלי חשיבות בהתפתחות ובתפקוד איברים ומסלולים חיוניים, או שידועות תסמונות גנטיות מנדליות הנגרמות ממוטציה נקודתית ברצף של גנים אלו, אזי אנו מניחים כי חוסר מלא שלהם יגרום לתמונה קלינית כלשהי. המאפיין הרביעי שמובא בחשבון בניתוח תוצאות הצ’יפ הגנטי הוא נוכחות החוסר או העודף אצל ההורים. אמנם תוארו מקרים רבים של שונות בביטוי הקליני, כשהורה שאצלו קיים החוסר סובל מליקויי למידה בלבד, וצאצאיו עלולים לגרום לפגיעות החלמפגיעה קוגנטיבית קשה עד כדי פיגור שכלי, אך עדיין נוכחות של החוסר או העודף אצל אחד ההורים הבריאים ינחה אותנו לניתוח תוצאות הצ’יפ כתקינות.
חשוב להבין כי לנוכח תשובה לא תקינה מסוג זה אם מדובר בדגימת תאי עובר, אפשר להתלבט עם בני הזוג אם להפסיק את ההיריון או להמשיכו. גם נוכח תוצאה כזו, על פי תוצאות בדיקת ה-FISH בעבור ההורים נוכל להעריך סיכון הישנות בהיריונותיהם העתידיים.
ג. נמצא חוסר או עודף של מקטע כרומוזומי זעיר שהמשמעות הקלינית היא שינויים בריאותיים מוכּרים הניתנים לטיפול, לדוגמה נטייה לסוכרת בגיל המבוגר. לרוב שינויים בריאותיים אלו קיימים בקרב כמה בני משפחה, והממצא פשוט מסביר את קיום התופעות או התכונות הללו אצלם. אם הוא מתגלה בעובר לא נדרש להפסיק את ההיריון בעטיו.
תוצאות לא תקינות
מה הסיכוי למצוא בשיטת הצ’יפ הגנטי תוצאה לא תקינה בדגימת דם של נבדק? חשוב להבין שהסיכוי שנמצא תוצאה לא תקינה, כזאת שמעידה על אחת התסמונות הגנטיות שאפשר לאתר בטכנולוגיה זו, תלויה במקור הדגימה שנשלחה לבדיקת בצ’יפ הגנטי.
אם מדובר בדגימת דם של מטופל (ילד או מבוגר) עם איחור התפתחותי או פיגור שכלי, בצורה מבודדת (הקרוי פיגור שכלי לא תסמונתי), או בשילוב עם ממצאים גופניים נוספים (הקרוי פיגור שכלי תסמונתי), אזי הסיכוי למצוא ממצא חיובי נע בין 10-20%. חשוב להבין שנשלח דגימת הדם של המטופל לביצוע בדיקה זו במרבית המקרים לאחר שבוצעה בעבורו בדיקת קריוטיפ ושזו נמצאה תקינה; כך שממצא חיובי בצ’יפ הגנטי הוא התקדמות גדולה מבחינת יכולת האבחון (אף שעדיין אין לנו הסבר לחלק ניכר מהמקרים), יכולת אבחונית שלא עמדה לרשותנו אך לפני שנים ספורות. אם מדובר בדגימת דם של מטופל (ילד או מבוגר) הלוקה באוטיזם, הסיכוי על פי סדרות שונות נע בין 5-10%. כלומר בלמעלה מ-90% ממקרי האוטיזם, בעיקר במקרים הקלים יותר, לא נצליח למצוא שינויבבדיקת הצ’יפ הגנטי.
מה הסיכוי למצוא תוצאה לא תקינה בדגימת תאי עובר בצ’יפ הגנטי? הסיכוי למצוא חוסר או עודף של מקטע גנטי זעיר בצ’יפ הגנטי יורד בצורה ניכרת כשמדובר בדגימת תאי עובר (מדיקור נוזל שפיר או סיסי שליה) בהשוואה לסיכוי אצל מטופלים הלוקים מפיגור שכלי. סיכוי זה מושפע מדרגת החשד וגורמי הסיכון שהיו בהיריון לפני ביצוע הבדיקה, ומה היתה מלכתחילה הסיבה לביצוע הבדיקה החודרנית לאיסוף תאי העובר. בשיטת הצ’יפ הגנטי מפיקים דנ”א מתרבית התאים או מדגימה ישירה של נוזל השפיר.
אם דיקור נוזל השפיר בוצע עקב ממצא לא תקין, יחיד, באולטרסאונד (כגון ריבוי אצבעות, שקיפות עורפית לא תקינה, מום לב או עיוות מבני של הכליות או השלד), הסיכוילממצא לא תקין בבדיקת הצ’יפ הגנטי הוא כ-1:40, לאחר שנמצא כי הקריוטיפ תקין. ככל שדרגת החומרה של ממצאי האולטרסאונד גדולה יותר, כך הסיכוי למצוא חוסר או עודף של מקטע כרומוזומי זעיר עולה ויכולה להגיע עד כדי 10% (כשמדובר במומים מרובים במערכות ראשיות כגון הלב, הגפיים, הכליות והמוח).
אם הדיקור בוצע עקב סיפור משפחתי – אח או ילד עם פיגור שכלי או אוטיזם – הסיכוי לממצא לא תקין בצ’יפ הגנטי נע סביב 1:50-1:100. אם הדיקור בוצע עקב גיל אֵם מעל ל-35 שנים (הסיבה העיקרית לבדיקות נוזל שפיר בישראל) או מפני שנמצא סיכון מוגבר לתסמונת דאון בבדיקות מעקב ההיריון השגרתיות, כגון סקר ביוכימי השליש הראשון והשני של ההיריון, אזי הסיכוי לממצא לא תקין בצ’יפ נע סביב 1:50. חשוב להבין כי גם בהיריונות שבהם בוצע הדיקור בלי סיבה רפואית כלשהי, אלא עקב רצון ההורים בלבד, עדיין קיים סיכוי לממצא לא תקין בצ’יפ הגנטי, אך בהסתברות נמוכה יותר, סביב 1:100-1:200.
מתי מומלץ לעשות בדיקת צ’יפ גנטי כשידוע שהקריוטיפ הקלאסי אינו תקין? כאמור, בדיקת קריוטיפ מאתרת חוסרים, עודפים או שינויים מבנים גדולים בכרומוזומים. במרבית המקרים, התשובה של בדיקה זו היא חד-משמעית: תשובה תקינה או לא תקינה, כגון במקרים של טריזומיות כרומוזומים, כגון טריזומיה 21 הגורמת לתסמונת דאון, או טריזומיות אחרות: טריזומיה של כרומוזום 13 (תסמונת פאטו), טריזומיה 18 (תסמונת אדוארדס), טריזומיית כרומוזום המין X. קיימים מצבים שבהם נותר ספק בנוגע למשמעות הקלינית של הממצא בקריוטיפ, כגון במקרים של עודף מקטע כרומוזמי מבודד, שלא ברורה תכולת הגנים בו (ממצא הקרוי בשפה המקצועית “מַרקֶר”), או במקרים של החלפת מקטעי חומר גנטי בין שני כרומוזמים (ממצא הקרוי טרַנסלוֹקַציה). במקרים אלו בדיקת הצ’יפ הגנטי יכולה להוסיף מידע חיוני – אם קיים חסר או עודף של מידע גנטי אצל המטופל או העובר. ממצא של צ’יפ גנטי לא תקין יכול להסביר תמונה קלינית אצל מטופל, או לאשר את החשד כי התמונה הקלינית שנצפתה בעובר היא תוצאה של שינוי כרומוזומי וחוסר או עודף של גנים חיוניים. מצד שני, תשובת צ’יפ גנטי תקינה מגדילה את הביטחון שהמטען הגנטי של המטופל או העובר מאוזנים, וכי קרוב לוודאי שהממצא הכרומוזומי שניצפה בבדיקת הקריוטיפ הוא חסר חשיבות קלינית.
בדיקת הצ’יפ הגנטי: יתרונות וחסרונות
כזכור, מדובר בבדיקה שהרזולוציה שלה גבוהה לעומת בדיקת הקריוטיפ הקלאסית, עד כדי פי 100, ולכן בדיקת הצ’יפ מאבחנת חוסרים או עודפים שגודלם קטן מכדי להתגלות בבדיקה הישנה. שנית, היא כוללנית ומאבחנת שינויים בכלל המידע הגנטי שלנו, גם בלא חשד קליני לתסמונת ספציפית, בשונה מבדיקות ה-FISH הנקודתיות. נוסף על כך שיטה זו מסוגלת לאבחן גם שינויים הקיימים רק בחלק מתאי גופנו, במצב הקרוי “פסיפס” (מוזאיקה), אפילו כשמדובר ב-7% בלבד מתאי הגוף, ממצא שלא היה מאותר בבדיקת הקריוטיפ. כמו כן, זו בדיקה מהירה יחסית המתקבלת לאחר עשרה ימים עד שבועיים. תשובה מהירה חשובה בייחוד כשהבדיקה מבוצעת על דגימת תאי עובר כשמעוניינים בתשובה בשלב מוקדם ככל האפשר של ההיריון בכדי לאפשר להורים להחליט בעניין האפשרויות להפסקתו.
מומלץ לבצע בדיקת צ’יפ בכל מטופל הלוקה בפיגור שכלי או שיש חשד לתסמונת גנטית שלא נמצא לה הסבר באמצעות בדיקת קריוטיפ או בדיקות שגרתיות אחרות. אפשר לשקול את ביצוע הבדיקה במטופלים עם אוטיזם או בכאלו שאובחנו עם מספר מומים מולדים (כגון מום לב מולד). ההתוויות לביצוע בדיקת הצ’יפ גנטי פחות חד-משמעיות ומוסכמות כשמדובר בתאי עובר. קיימת הסכמה כי אם מאותרים באולטרסאונד במהלך היריון מומים מבניים באיברים השונים, מומלץ לבצעה: אך בנוגע לשאר ההיריונות, שבהם מבוצע דיקור נוזל שפיר מסיבות אחרות כגון גיל אימהי גבוה או בלי כל סיבה רפואית, לא ברור בשלב זה אם כדאי לבצע את הבדיקה ומה היחס עלות-תועלת מביצועה. ההחלטה של איגוד הרופאים הגנטיקאים בישראל בשלב זה היא לעדכן כל אישה שעוברת בדיקת חודרנית במהלך ההיריון על האפשרות לביצוע בדיקת צ’יפ גנטי בדגימת תאי העובּר, ולאפשר לה את הבחירה אם לבצעה. יש לזכור כי בשימוש בכל טכנולוגיה חדשה עלולות להיות טעויות בפיענוח התשובות; תוצאות שמפעונחות כיום כתקינות ייתכן שבעתיד יתבררו כמעידות על בעיות ולהפך: שינויים שכיום מפוענחים כלא תקינים ייתכן כי בעתיד ייתברר שהם שפירים.
אחד החסרונות הבולטים של שיטה זו, ואחד המעצורים בדרך לצבירת מידע בתחום זה, היא העלות הגבוהה של הבדיקה. בדיקה זו מבוצעת כיום במקצת מהמכונים הגנטיים בארץ וכן בכמה מעבדות קליניות פרטיות בעולם ועלותה המינימלית היא בסביבות 4,000 שקלים. המימון הוא מכיסו הפרטי של המטופל ומשפחתו, ורבים המטופלים שידם אינה משגת זאת ולכן נמנעת מהם הבדיקה.
סיכום
ייעוץ גנטי הוא הליך מורכב שחשוב למשפחות רבות. פיענוח בדיקת צ’יפ גנטי לאחר בדיקת גורם מוסמך יכול לתרום תרומה ניכרת להחלטות המשפחה וההורים לעתיד. בדיקת הצ’יפ הגנטי עדיין אינה מחליפה את בדיקת הקריוטיפ הסטנדרטית המבוצעת בדגימת דם או בנוזל שפיר. למרות ההסתייגויות בדיקת הצ’יפ הגנטי היא בדיקה חשובה, שכבר נצבר בה ניסיון רב, והיא מעלה את הרזולוציה ומגדילה את אחוזי הגילוי והאבחון. קרוב לוודאי שבעתיד הקרוב, כשיגדל הידע והניסיון, תהיה בדיקה זו לחלק מהבדיקות השגרתיות המבוצעות למטופלים ולדגימות תאים של עובּרים.
ד”ר עידית מאיה היא בוגרת בית הספר לרפואה של האוניברסיטה העברית בירושלים לתואר MD. מומחית ברפואה פנימית וכיום מתמחה בהתמחות-על בגנטיקה רפואית במכון הגנטי על שם רפאל רקנאטי, בית חולים בילינסון, מרכז רפואי רבין בפתח-תקווה.
פרופסור מרדכי (מוטי) שוחט הוא בוגר בית הספר לרפואה של אוניברסיטת תל-אביב לתואר MD. מומחה ברפואת ילדים ובגנטיקה רפואית ומנהל המכון הגנטי על שם רפאל רקנאטי בבית חולים בילינסון, מרכז רפואי רבין בפתח-תקווה. פרופסור לגנטיקה רפואית באוניברסיטת תל-אביב.

5 תגובות
אם אני מבינה נכון אז גם אצל אנשים בריאים יכולים להיות חוסרים או עודפים במקטעים מסוימים בכרומוזומים שלא יהיה להם שום ביטוי קליני?
או שיהיה להם ביטוי קליני ״קליל״ כמו נטיה לסכרת לדוגמא?
לא נראה לי…מה שימנע אולי פיתוחים וסלקציה זו חקיקה…אבל כנראה שחקיקה לא תמנע סלקציה שמונעת מחלות גנטיות. אז סלקציה כן תהיה, תראה מה קורה כבר היום עם בדיקות הריון, מתוך 200,000 הריונות בישראל, הופסקו 50,000 בגלל גילויים גנטיים או דפקות במהלך ההריון (שתכלס לא מבטיחים 100% דיוק) ישראל מקום ראשון בבדיקות הריון שלא בהכרח צריך למשל.
אם תהיה בדיקת DNA מהירה, זה אומר שכל זירעון יהיה אפשר לבדוק במהירות. אולי…
לגבי זיקנה, כנראה שגם שם מתישהו זה ישתנה, כבר מצאו דרך להאריך את הטלומרס, מדעית…
http://www.tasciences.com/ta-65/
שלא לדבר על גידול איברים, השתלות תאים לשיחזור איברים, כדורים שמדליקים את החלק בDNA אצלנו שכבוי שמאפשר עוד 30% בתוחלת החיים (יעני 100+ וקצת) וכו…
חפש על BBC.Horizon.S48E11.Dont.Grow.Old
שם מדובר על חלק מהדברים, וחלק אחר בתוכניות אחרות.
כמו שפעם חיו עד 30 שנה והיום זה כבר 80+ בממוצע
יכול להיות שאנחנו נגיע ב10-20 שנה הקרובות ליכולות שיפור של פי 2…עד 160 שיהיה לך
פרישה לפנסיה בגיל 120
🙂
אל תגאג, עומרי, האבולוציה האיטית והזקנה לא הולכת לשום מקום והיא עומדת להפתיע את כל המשופצרים למיניהם עם נבוט גדול בסיבוב.
מגניב, הסרט גטקה בקרוב…
הסוף לאבולוציה האיטית…
ככל שפיענוח הDNA יהיה מהיר, אפשר לבצע בחירה של צאצאים מהירה בין מיליונים זרעים..בדיוק כמו בסרט