אנגיוגנזה הינו התהליך בו נוצרים כלי דם חדשים ההכרחיים לגדילתם של התאים הסרטניים. המערכת של תלתן תוקפת תהליך זה
תלתן פארמה מודיעה היום על התחלת ניסוי קליני, שלב 2, של התרופה TL-118 לטיפול בסרטן הלבלב. TL-118 הינה תרופה אנטי-אנגיוגנית, כלומר תרופה המעכבת את אספקת הדם לגידולים הסרטניים, ועל ידי כך פוגעת בהם ומנטרלת אותם.
בעקבות קבלת אישור ממשרד הבריאות, תלתן פארמה החלה ניסוי שלב 2 בשלושה מרכזים אונקולוגיים מובילים: במרכז הרפואי תל-אביב ע”ש סוראסקי, במרכז הרפואי הדסה בירושלים ובקרוב במרכז הרפואי שיבא בתל-השומר. בניסוי ישתתפו 80 חולים שאובחנו בסרטן לבלב גרורתי וטרם קיבלו טיפול כימותרפי. החולים ישובצו לאחת משתי זרועות הניסוי שכל אחת תכלול 40 מטופלים. קבוצת הביקורת תטופל רק בטיפול הכימותרפי המקובל לסרטן הלבלב והקבוצה השנייה תטופל בנוסף לכימותרפיה גם ב-TL-118.
ד”ר דן גולדשטאוב, מנהל התפעול הראשי של תלתן פארמה, אמר, “אנו מרוצים מאוד מתוצאות הניסוי בחיות על סרטן הלבלב ומהתוצאות הראשוניות של בטיחות וסבילות שנצפו במספר חולי סרטן הלבלב שטופלו כבר ב- TL-118 במסגרת טיפולי חמלה. אנחנו מצפים לבסס את יעילותו של המוצר לטיפול בסרטן הלבלב בניסוי הקליני שהחל זה עתה”.
TL-118 נוסה במודל של סרטן לבלב בעכברים, שם טיפול בלעדי בתרופה עיכב את התפתחות הגידול הסרטני באופן משמעותי בהשוואה לטיפול הכימותרפי המקובל. יתרה מזאת, טיפול ב-TL-118 בשילוב עם הטיפול הכימותרפי המקובל העלים לגמרי את גידולי הלבלב בכל החיות המטופלות.
TL-118 מעכב יצירת כלי דם חדשים (אנגיוגנזה) בגידולים וכך מעכב את אספקת הדם אליהם ואת התפתחותם. המוצר ניתן בתמיסה לשתייה שנלקחת פעם ביום, ומהווה שילוב של מספר חומרים אשר כל אחד מהם מעכב את תהליך האנגיוגנזה באופן שונה ובלתי תלוי בשאר החומרים. כל החומרים הללו מאושרים על-ידי רשויות הרגולציה. מחזורי הטיפול מתוזמנים היטב על-מנת לאפשר נטילה ידידותית למשתמש ובו בזמן השפעה סינרגיסטית של חומרי התכשיר לקבלת טיפול בטוח ואפקטיבי בסרטן. עד כה למעלה מ-100 חולים טופלו ב- TL-118 לתקופה של עד 3 שנים.
בטיחותו של TL-118 נבחנה בניסוי קליני, שלב 1 במרכז הרפואי שיבא בתל-השומר. 30 חולים השתתפו בניסוי, ונמצא שהתכשיר בטוח לשימוש ובעל סבילות טובה בחולי סרטן ורוב תופעות הלוואי שנגרמו כתוצאה מהטיפול היו מינוריות.
במקביל, TL-118 נבחן גם כטיפול בסרטן הערמונית. עד כה, כ-50 חולים גויסו בארץ לניסוי שלב 2 , הנמצא תחת אישור IND פעיל שהוענק על-ידי ה-FDA.
תלתן פארמה צפויה להיכלל כאחת מחברות הפורטפוליו של אינטגרה הולדינגס, עם השלמת הקמתה. אינטגרה הולדינגס הינה חברת אחזקות חדשה שיישום, חברת מסחור הטכנולוגיות של האוניברסיטה העברית, מקימה בתחום הביוטכנולוגיה.
אודות טיפול אנטי-אנגיוגני
אנגיוגנזה הינו התהליך בו נוצרים כלי דם חדשים ההכרחיים לגדילתם של התאים הסרטניים. טיפולים אנטי-אנגיוגניים שמטרתם “להרעיב” את הגידול הסרטני על ידי ניתוק אספקת הדם מהווים אסטרטגיה מבטיחה ביותר לעיכוב צמיחה והתפשטות של גידולים סרטניים, מכיוון שכל הגידולים הסרטניים המוצקים נסמכים על תהליך אגרסיבי של אנגיוגניזה על מנת להתפתח. בניגוד לגידולים סרטניים, אנגיוגנזה פעילה אינה מתרחשת ברקמות בריאות, דבר המדגיש את הפוטנציאל הטיפולי ואת ההיתכנות של התהליך האנטי-אנגיוגני. TL-118 תוכנן במטרה לעכב מספר מנגנונים מקבילים שאינם חופפים המשתתפים באנגיוגנזה.
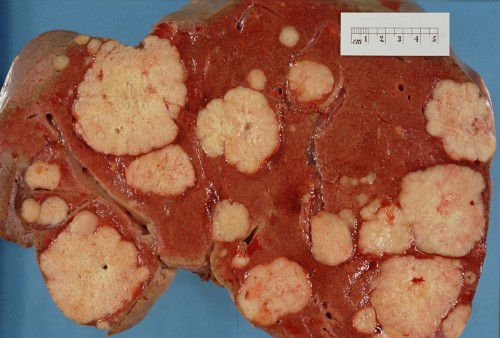
אודות סרטן הלבלב
6% ממקרי התמותה הנגרמים מסרטן בארה”ב נגרמים כתוצאה מסרטן הלבלב. זהו גורם המוות הרביעי ממחלה סרטנית בנשים ובגברים בארה”ב. ההערכות לשנת2011 הן כי אובחנו 44,000 מקרים חדשים של סרטן הלבלב בארה”ב, ומספר דומה של מקרי תמותה התרחשו בארה”ב בשנה זו כתוצאה מסרטן הלבלב. ההישרדות הכללית ל-5 שנים לכל שלבי המחלה הוא רק 6% והצפי לחולי סרטן לבלב מתקדם הוא אף מועט מכך.
אודות תלתן פארמה
תלתן פארמה היא חברה ביוטכנולוגית שמטרתה לפתח ולמסחר את הפלטפורמה האנטי-אנגיוגנית שלה לטיפול בסרטן ולמטרות נוספות. החברה היא בבעלות משותפת של יישום, החברה לפיתוח המחקר של האוניברסיטה העברית בירושלים, יזמי החברה, משקיעים ישראליים ותאגיד קנדי. למידע נוסף כתובת אתר החברה www.tiltanpharma.com

9 תגובות
שמי שיראל כהן, לאמא שלי התגלה לפני חודשיים סרטן בלבלב עם חשש לנגיעות לריאות. אשמח לדעת עוד דברים הקשורים למחקר. ואיך ניתן להצטרף אליו.
תודה. זה הנייד שלי 0524054578
שמי רומנו דניאל, בהתאם לסי טי שערכו לי קבעו כי יש לי סרטן בלבלב בזנב עם גלישה לגוף וגרורות בכבד.אשמח לדעת כל דבר הקשור למחקר שלכם, ואם יש אפשרות לקחת בו חלק. אודה לכם אם תצרו קשר למייל הרשום , באתר באנגלית רשמנו גם את הטלפון. תודה רומנו דניאל
אבי חולה בסרטן הלבלב עם גרורות לכבד. אשמח לקבל עדכונים שוטפים.
גיל:
אולי תשנה את שמך לברוך ג’מילי?
http://www.youtube.com/watch?v=ZtymP0Qzsts&context=C360a41aADOEgsToPDskKE22L-zfjRJzEeBXjx-u_c
עד עכשיו טיפולים אנגיוגיונים נכשלו ולא עברו FDA בטיפול בסרטן
אולם הצליחו בטיפול בניוון רישתית מקולרי שהוא שוק גדול פי 3 למרות שההד התקשורתי שלו נמוך.
מאחלת לכם המון הצלחה
האם צורף לניסוי החולה בסרטן הלבלב המפורסם – הרב יעקב יוסף?
מצטרף לשאלה של דני,
האם ניתן לטפל בסוגים אחרים של סרטן באמצעות אנטי-אנגיוגנזה?
בהצלחה!
במידה והשלב הזה מצליח, מהם השלבים הבאים הנדרשים כדי שהטיפול יהיה נגיש לציבור?