באמצעות תוכנת מחשב חדשה, הצליחו מדענים ממכון ויצמן לתכנן חלבון מלאכותי אשר מעורר תגובה חיסונית המעכבת את טפיל המלריה. ייתכן שהשיטה אף תוכל לסייע להילחם במחלות זיהומיות מסוג זיקה ואבולה.
מלריה היא אחת המחלות הזיהומיות הקשות בעולם. היא פוגעת במאות מיליוני אנשים, ומדי שנה מתים בעטיה כחצי מיליון בני-אדם, רובם ילדים במדינות טרופיות עניות. הטפיל שגורם את המחלה הוא אמן התחמקות שעובר מספר גלגולים, גם בחולה וגם ביתושה המעבירה אותו מאדם לאדם. בכל אחד מהגלגולים משנה הטפיל את פני השטח שלו, והופך למטרה נעה במהירות שמקשה על המערכת החיסונית ״להינעל״ עליו. אולם, לטפיל זה יש גם עקב אכילס – חלבון ייחודי הקרוי RH5, אשר מאפשר לו לעגון על תאי הדם האדומים של החולה ולפלוש אליהם. לפיכך, עיכוב של החלבון זה בולם את המחלה.
בשנים האחרונות, נעשה מאמץ לייצר את החלבון הזה בתצורה ובכמויות הגדולות הנחוצות כדי להשתמש בו כבתרכיב חיסון. אלא שבדומה לחלבוני חיסון ממחלות זיהומיות אחרות, גם RH5 הוא חלבון לא יציב, אשר מתפרק בטמפרטורה גבוהה, ואפשר להפיקו אך ורק במערכות תאיות מורכבות ויקרות. היות שחיסון נגד מלריה נדרש בעיקר במדינות עניות, שבהן אמצעי קירור אינם נגישים, ספק רב אם אפשר להשתמש ב-RH5 כבחיסון יעיל באזורים אלה.
כדי להתגבר על קושי זה החליטו תלמידת המחקר עדי גולדנצוייג וד”ר שראל פליישמן, מהמחלקה למדעים ביומולקולריים במכון ויצמן למדע, לשפר את יציבותו של RH5. כדי לעשות זאת פיתחה גולדנצוייג תוכנת מחשב חדשה לתכנון חלבוני חיסון ממחלות זיהומיות. היות שחלבונים אלה נתונים להתקפה מתמדת של המערכת החיסונית, הם משתנים במהירות בכל דור ודור. התוכנה של גולדנצוייג מנצלת את כל המידע הקיים בידינו ביחס לתצורות החלבון בטפילים שונים כדי לחשב מוטנט שיחזק את חלבון המטרה מבלי לפגוע בפעילותו. מסבירה גולדנצוייג: ״הטפיל משטה במערכת החיסון באמצעות צבירת מוטציות על פני חלבוני השטח שלו. וכך, באופן פרדוקסלי, ככל שהטפיל מצליח יותר לחמוק מהמערכת החיסונית, כך הוא נותן בידינו יותר רמזים שיאפשר לנו לייצר חיסון מלאכותי מוצלח״.
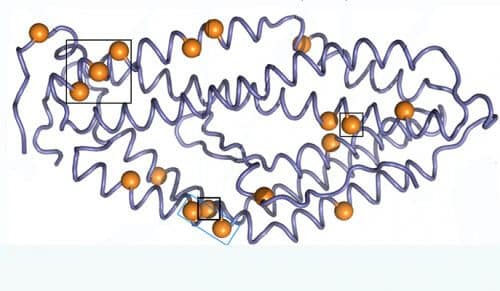
גולדנצוייג שלחה את החלבונים שהיא חישבה לקבוצת מחקר באוקספורד המתמחה בפיתוח חיסון למלריה, בראשות פרופ׳ מת׳יו היגינס ופרופ׳ סיימון דרייפר, והתוצאות המרשימות לא איחרו להגיע. בעוד שאת החלבון הטבעי אי-אפשר ליצור במערכות תאיות פשוטות וזולות, את החלבון שפיתחה אפשר ליצור בכמויות גדולות, ובכך להוזיל משמעותית את הפקת תרכיב החיסון. החלבון המתוכנן גם יציב בטמפרטורות של עד 50 מעלות צלזיוס, ובכך פותר את הבעיה המרכזית בשינוע ערכות החיסון במדינות טרופיות. וחשוב מכל, ניסויים בחיות הראו שאכן, החלבון מעורר תגובה חיסונית אשר מעכבת את הטפיל. מוסיף ד״ר פליישמן: ״השיטה שעדי פיתחה היא כללית לחלוטין. כלומר, הראינו שהיא מצליחה גם היכן שנכשלות שיטות אחרות בגלל תכונות המטרה (למשל, הטפיל). היות שֶקַל כל כך ליישם את השיטה, היא תוכל לסייע להילחם במחלות זיהומיות ‘חדשות’, שבדומה לזיקה ולאבולה נחוץ מענה מקיף ומהיר להן״.
באמצעות סדרת ניסויים חדשה מקווים המדענים לבחון אסטרטגיית פעולה אחרת נגד טפיל המלריה – שתתבסס על חסימה פיסית-כימית של חלבון העגינה הטפילי. חסימה זו עשויה להתבצע, למשל, באמצעות תכנון של חלבון מלאכותי שיקשור בחוזקה את חלבון RH5 – ובכך יבלום ישירות את ההדבקה.
#מספרי_מדע
כ-40% מהאנושות חיה באזורים מוכי מלריה.

3 תגובות
מציאת חיסון למלריה היא הישג אדיר.
כל הכבוד
מסכים לחלוטין עם האנונימי
היהודים תמיד עשו טוב לעולם !!!!!!!!
פרס נובל לעדי גולדנצוייג וד”ר שראל פליישמן